- A. Neutron, photon.
- B. Electron, neutron.
- C. Proton, photon.
- D. Proton, neutron.
- A. Acid.
- B. Base.
- C. Chất lưỡng tính.
- D. Muối.
- A. Chủ yếu tồn tại dạng nguyên tử.
- B. Chỉ tồn tại trong các hợp chất.
- C. Cả dạng đơn chất và hợp chất.
- D. Chủ yếu tồn tại dạng NOx trong không khí.
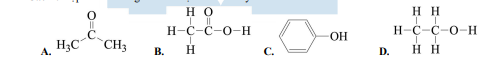
- A. H3C-C(=O)-CH3
- B. H-C(=O)-O-H
- C. C6H5-OH
- D. CH3-CH2-OH (Hình D)
- A. Methyl propionate.
- B. Ethyl acetate.
- C. Ethyl propionate.
- D. Methyl acetate.
- A. CaCO3(s) → CaO(s) + CO2(g).
- B. FeCl3(aq) + 3AgNO3(aq) → Fe(NO3)3(aq) + 3AgCl(s).
- C. CuSO4(aq) + 2NaOH(aq) → Cu(OH)2(s) + Na2SO4(aq).
- D. SO2(g) + 2H2S(g) → 3S(s) + 2H2O(l).
- A. NO.
- B. NO2.
- C. N2O.
- D. N2O5.
- A. Aldehyde.
- B. Alkyne.
- C. Phenol.
- D. Alcohol.
- A. Glucose và fructose.
- B. Chỉ có fructose.
- C. Chỉ có glucose.
- D. Glucose và maltose.
- A. -2.
- B. +2.
- C. +1.
- D. 0.
- A. NH3(g) + HCl(g) → NH2Cl(s) + H2(g).
- B. NH3(g) + HCl(g) → NH4Cl(s).
- C. 2NH3(g) + 2HCl(g) → N2(g) + Cl2(g) + 4H2(g).
- D. NH3(g) + 3HCl(g) → NCl3(s) + 3H2(g).
- A. Ca(HCO3)2(s) --t°--> CaCO3(s) + CO2(g) + H2O(g).
- B. CaCO3(s) --t°--> CaO(s) + CO2(g).
- C. CaO(s) + CO2(g) --t°--> CaCO3(s).
- D. CaCO3(s) + CO2(g) + H2O(g) --t°--> Ca(HCO3)2(s).
- A. Ethene và pentan-1-ol.
- B. Ethane và pentanoic acid.
- C. Ethanol và pentanoic acid.
- D. Ethanoic acid và pentan-1-ol.
- A. -[CH2-CH(CH3)]n-
- B. -[CH2=CH-CH3]n-
- C. -[CH2-CH-CH3]n-
- D. -[CH2=CH(CH3)]n-
- A. Khoảng 1836 lần.
- B. Khoảng 5,4 lần.
- C. Khoảng 1,8.10^(-53) lần.
- D. Khoảng 0,0005 lần.
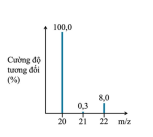
- A. 20,15.
- B. 21,82.
- C. 34,64.
- D. 21,00.
Fluorine (F2): Nhiệt độ nóng chảy -220 °C, Nhiệt độ sôi -188 °C.
Chlorine (Cl2): Nhiệt độ nóng chảy -101 °C, Nhiệt độ sôi -35 °C.
Bromine (Br2): Nhiệt độ nóng chảy -7 °C, Nhiệt độ sôi 59 °C.
Iodine (I2): Nhiệt độ nóng chảy 114 °C, Nhiệt độ sôi 184 °C.
Phương án nào dưới đây là đúng?
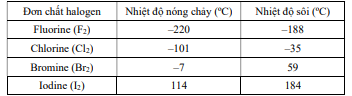
- A. Do tạo được liên kết hydrogen giữa các phân tử, nên F2 có nhiệt độ nóng chảy và nhiệt độ sôi thấp nhất.
- B. Do khối lượng phân tử và năng lượng liên kết trong phân tử tăng dần từ F2 đến I2, nên nhiệt độ nóng chảy và nhiệt độ sôi của các đơn chất halogen tăng dần.
- C. Do tương tác van der Waals giảm dần từ F2 đến I2, nên nhiệt độ nóng chảy và nhiệt độ sôi của các đơn chất halogen tăng dần.
- D. Do khối lượng, kích thước phân tử và số lượng electron trong các phân tử tăng từ F2 đến I2, nhiệt độ nóng chảy và nhiệt độ sôi của các đơn chất halogen tăng dần.
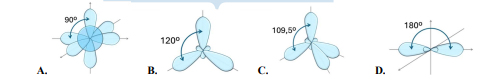
- A. Hình A (90°).
- B. Hình B (120°).
- C. Hình C (109,5°).
- D. Hình D (180°).
- A. 6, 6.
- B. 3, 3.
- C. 3, 6.
- D. 6, 3.
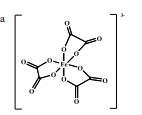
- A. Đúng
- B. Sai
Thí sinh chọn các phương án đúng theo yêu cầu từ câu 21 đến câu 25.
Câu 21: Tiến hành thí nghiệm theo các bước sau:
Rót dung dịch sodium chloride (NaCl) bão hòa vào cốc 1, cốc 2, cốc 3; dầu nhờn (bản chất là hỗn hợp các hydrocarbon) vào cốc 4.
Cho một đinh thép vào cốc 1 và cốc 4, cho đinh thép được quấn bởi dây kẽm (Zn) vào cốc 2, cho đinh thép được quấn bởi dây đồng (Cu) vào cốc 3 (các đinh thép là thép carbon thường và đã được làm sạch bề mặt).
Dự đoán hiện tượng nào dưới đây phù hợp với lí thuyết về sự ăn mòn kim loại khi để 4 cốc trong không khí sau 5 ngày?
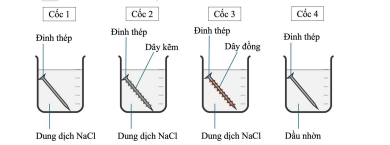
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
Câu 22: Một ống nghiệm chứa chất lỏng X. Biết rằng X có thể là hexane hoặc hex-1-yne. Cách làm nào dưới đây xác định được chất X?
Cho X vào dung dịch bromine (Br2), nếu dung dịch Br2 nhạt màu thì chứng tỏ chất lỏng là hexane.- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
Câu 23: Khi tìm hiểu về các yếu tố ảnh hưởng đến tốc độ phản ứng, để trả lời cho câu hỏi “Nồng độ chất tham gia ảnh hưởng đến tốc độ phản ứng như thế nào?”, học sinh đã tiến hành thí nghiệm theo các bước:
Bước 1: Chuẩn bị 2 cốc thuỷ tinh 250 mL được đánh dấu A và B.
Bước 2: Rót 50 mL dung dịch hydrochloric acid (HCl) 1 M vào cốc A; 50 mL dung dịch HCl 2 M vào cốc B.
Bước 3: Cho 1 gam bột kẽm (Zn) vào mỗi cốc. Quan sát hiện tượng xảy ra ở 2 cốc.
Phát biểu nào sau đây đúng?
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Phát biểu trên đúng hay sai?
- B. Đúng
- C. Sai
Câu 24. Một học sinh thực hiện thí nghiệm chuẩn độ để xác định nồng độ dung dịch hydrochloric acid (HCl) bằng dung dịch chuẩn sodium hydroxide (NaOH) 0,100 M với chỉ thị methyl orange (MO). Biết rằng MO sẽ có màu đỏ trong môi trường có pH < 3,2, màu vàng trong môi trường có pH > 4,4, và màu cam trong khoảng pH từ 3,2 đến 4,4. Để thực hiện chuẩn độ, học sinh đổ dung dịch NaOH 0,100 M (từ burette) từ từ vào bình tam giác chứa sẵn 100,0 mL dung dịch HCl 3,3 g dung dịch MO, đến khi dung dịch vừa chuyển sang màu cam thì dừng chuẩn độ. Biết rằng dung dịch chứa sodium chloride (NaCl) thì có pH bằng 7.
Có thể cho chất chỉ thị MO vào dung dịch NaOH trong burette thay vì cho vào bình tam giác.- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
Câu 25. Để xác định tên của một muối sodium halide (NaX, với X là nguyên tố halogen), người ta pha lượng muối này vào nước cất, khuấy đều, thu được dung dịch A. Nhỏ dung dịch silver nitrate (AgNO₃) dư vào dung dịch A thấy không xuất hiện kết tủa.
Có thể kết luận X là nguyên tố fluorine.- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
- A. Đúng
- B. Sai
Dựa vào dữ liệu dưới đây, thí sinh lựa chọn một phương án đúng theo yêu cầu của câu 26 và câu 27.
Chất hữu cơ A và B là đồng phân của nhau. Trong đó, chất A là một ester có tên là vinyl acetate. Trung hợp chất A thu được polymer X, là một loại keo dán thông dụng cho các vật liệu xốp như gỗ, giấy và vải.
Chất hữu cơ B bền trong dung dịch sulfuric acid loãng, B có thể phản ứng với thuốc thử Tollens (dung dịch AgNO₃ trong NH₃ dư). Ngoài ra, khi cho B tác dụng với dung dịch iodine (I₂) trong môi trường kiềm thì xuất hiện kết tủa vàng.
Mỗi mắt xích trong polymer X có bao nhiêu nguyên tử carbon?- A. 2.
- B. 3.
- C. 4.
- D. 5.
(a) Khi hòa tan chất B bằng LiAlH₄ thu được chất hữu cơ có thể hòa tan copper(II) hydroxide (Cu(OH)₂) tạo dung dịch màu xanh lam.
(b) Chất B phản ứng với thuốc thử Tollens tạo kết tủa Ag với tỉ lệ mol B : Ag = 1 : 2.
(c) Kết tủa vàng là hợp chất hữu cơ có phần trăm khối lượng carbon nhỏ hơn 10%.
(d) 1 mol chất B tác dụng được tối đa với 2 mol hydrogen cyanide (HCN).
- A. 1.
- B. 2.
- C. 3.
- D. 4.
Dựa vào dữ liệu dưới đây, thí sinh lựa chọn một phương án đúng theo yêu cầu từ câu 28 đến câu 30.
Nitrogen là nguyên tố dinh dưỡng quan trọng cho sinh vật, tuy nhiên hàm lượng nitrogen cao có thể gây ô nhiễm nước. Một nghiên cứu xác định hàm lượng ammonium (NH₄⁺) trong nước bề mặt ở Đồng bằng Sông Cửu Long và so sánh với tiêu chuẩn hàm lượng NH₄⁺ < 3 mg L⁻¹ theo quy định sau:
– Chuẩn bị mẫu thử bằng cách pha loãng mẫu nước 10 lần.
– Ion NH₄⁺ được chuyển thành indophenol qua các phản ứng:
NH₄⁺ + ClO⁻ → NH₂Cl + H₂O
NH₂Cl + phenol → indophenol
Indophenol (dung dịch A)
– Cường độ màu (đậm/nhạt) của dung dịch A tỉ lệ thuận với lượng indophenol trong dung dịch.
Khi đo máy đo cường độ màu có thể tính toán được hàm lượng indophenol, từ đó tính được hàm lượng NH₄⁺ trong nước. Kết quả cho thấy hàm lượng NH₄⁺ trong mẫu thử là 1,44 mg L⁻¹.
– Các phản ứng cảm ứng diễn ra ở điều kiện pH trong khoảng từ 4 đến 13. Thể tích dung dịch mẫu nước được dùng là 0,26 mL cho mẫu nước có hàm lượng NH₄⁺ cần đo là 10,30 mg L⁻¹.
(Tham khảo G.-J. Wilbers, M. Becker, L. T. Ng, Z. Sebesvari, and F. G. Renaud, “Spatial and temporal variability of surface water pollution in the Mekong Delta, Vietnam”, Science of the Total Environment, vol. 485–486, pp. 653–665, Jul. 2014, doi: 10.1016/j.scitotenv.2014.03.049)
Câu 28: Trước khi tiến hành đo cường độ màu, để kiểm tra pH người ta nhúng giấy quỳ tím vào mẫu thử, nhận thấy giấy quỳ tím không đổi màu. Kết luận nào sau đây là đúng?- A. pH của mẫu thử phù hợp để tiến hành đo.
- B. pH của mẫu thử chưa phù hợp, cần lấy mẫu thử ở vị trí khác.
- C. pH của mẫu thử chưa phù hợp, cần điều chỉnh bằng acid hoặc kiềm.
- D. Chưa thể kết luận gì vì bước này không có ý nghĩa trong phép đo.
(a) Hàm lượng nguyên tố nitrogen trong nước có thể dẫn đến hiện tượng phú dưỡng, làm tăng nồng độ oxygen (O₂) hòa tan trong nước và gây ô nhiễm.
(b) Hàm lượng nguyên tố nitrogen tồn tại ở dạng NH₄⁺ trong mẫu thử trên là 1,12 mg L⁻¹.
(c) Kết quả nghiên cứu cho thấy lượng NH₄⁺ trong nước có nguồn gốc từ phân bón trên các đồng ruộng lân cận.
(d) Kết quả trên khẳng định được nitrogen trong nước không tồn tại ở dạng nitrate (NO₃⁻).
Phát biểu nào đúng?
- A. (a) và (b).
- B. (b).
- C. (a), (c), và (d).
- D. (b) và (d).
(a) Mục đích của thí nghiệm là để kiểm tra hàm lượng ion NH₄⁺ trong nước bề mặt có nằm ngoài tiêu chuẩn cho phép hay không.
(b) Hàm lượng NH₄⁺ trong mẫu nước ban đầu là 1,44 mg L⁻¹.
(c) Nồng độ NH₄⁺ trong mẫu thử càng lớn thì cường độ màu của dung dịch A càng yếu.
(d) Việc pha loãng mẫu nước này thành ammonium (NH₃) khi tiếp xúc với kiềm.
(e) Có thể kết luận rằng mẫu nước này không bị ô nhiễm NH₄⁺.
Có bao nhiêu phát biểu đúng trong các phát biểu trên?
- A. 1.
- B. 2.
- C. 3.
- D. 5.
Thí sinh điền đáp án hoặc ký hiệu của phương án vào ô trống theo yêu cầu từ câu 31 đến câu 40.
Câu 31. Một mẫu nước được thí nghiệm định tính để xác định sự có mặt của một số ion. Mẫu nước được cho vào 4 ống nghiệm, sau đó nhỏ mỗi loại thuốc thử vào mỗi ống nghiệm và ghi nhận hiện tượng như bảng dưới đây:
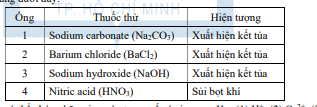
Mẫu nước trên có thể chứa những ion nào trong số các ion sau đây:
(1) H⁺; (2) Ca²⁺; (3) SO₄²⁻; (4) HCO₃⁻; (5) CO₃²⁻.
Đáp án:
(47)
Câu 32. Khi đặt carbon trong điều kiện thiếu oxygen (O₂), khí carbon dioxide (CO₂) sinh ra có thể phản ứng với carbon theo phản ứng thuận nghịch sau:
CO₂(g) + C(s) ⇌ 2CO(g)
Khi phản ứng trên đạt trạng thái cân bằng, các tác động nào dưới đây làm cân bằng chuyển dịch theo chiều thuận? (Liệt kê phát biểu đúng theo kí hiệu)
(1) Tăng nồng độ khí CO₂.
(2) Tăng áp suất cân bằng các chất khí.
(3) Cho thêm carbon.
(4) Giảm nồng độ khí carbon monoxide (CO).
Đáp án: (48)
Câu 33. Một học sinh cần điều chế một lượng nhỏ khí acetylene từ calcium carbide để thực hiện thí nghiệm tính chất. Nhận từ lọ calcium carbide có trong phòng thí nghiệm ghi các thông tin sau:

Học sinh này cần thu 12,4 mL khí acetylene ở điều kiện chuẩn để thực hiện thí nghiệm. Nếu xem hiệu suất phản ứng là 100%, học sinh này cần sử dụng tối thiểu x mg calcium carbide. Xác định giá trị của x (làm tròn đến một chữ số thập phân).
Đáp án: (48)
Câu 34. Methanol (CH₃OH) được tổng hợp từ khí hydrogen (H₂) và carbon monoxide (CO) theo phản ứng sau:
2H₂(g) + CO(g) ⇌ CH₃OH(g)
Trong một khảo sát, ban đầu H₂ và CO được nạp vào bình phản ứng theo tỉ lệ mol 2:1, nhiệt độ phản ứng là 473 K, áp suất ban đầu là 100 bar và có mặt chất xúc tác Cu–Zn–Al₂O₃. Sau 300 giây, nồng độ CH₃OH là 1,8 mol L⁻¹. Cho các phát biểu sau:
(1) Tốc độ trung bình của phản ứng tạo thành CH₃OH trong thời gian trên là 6,0×10⁻³ mol L⁻¹ s⁻¹.
(2) Nếu thực hiện phản ứng ở nhiệt độ là 373 K thì tốc độ của phản ứng sẽ thấp hơn so với trường hợp trên.
(3) Trong phản ứng này, chất xúc tác làm cân bằng dịch chuyển theo chiều thuận.
(4) Thực hiện phản ứng ở áp suất cao sẽ tăng tốc độ phản ứng.
Liệt kê phát biểu đúng theo kí hiệu.
Đáp án: (49)
Câu 35. Dichlorodiphenyltrichloroethane (DDT) là một trong những loại thuốc trừ sâu rất hiệu quả cao, tuy nhiên nhiều nghiên cứu đã chỉ ra rằng DDT là chất có độc tính cao và phân hủy rất chậm, do đó đã bị cấm sử dụng. Một nghiên cứu thiết lập mối quan hệ giữa nồng độ DDT trong đất với thời gian như sau:
C = C₀ – 0,0018t – 1,6162
Trong đó: C và C₀ lần lượt là hàm lượng sau và hàm lượng ban đầu của DDT trong đất (đơn vị là μg g⁻¹), t là thời gian (đơn vị tính bằng ngày).
Người ta xác định được 20 g một mẫu đất nông nghiệp có lượng DDT là 41,6 μg. Dựa trên dữ liệu của nghiên cứu trên, sau bao nhiêu ngày hàm lượng DDT trong mẫu đất trên sẽ giảm còn 0,1 μg g⁻¹? (làm tròn đến hàng đơn vị)
Đáp án: (50)
Câu 36. Sulfuric acid (H₂SO₄) là hóa chất quan trọng, được sản xuất trong công nghiệp bằng phương pháp tiếp xúc qua ba giai đoạn:
(a) S(s) + O₂(g) → SO₂(g)
(b) 2SO₂(g) + O₂(g) ⇌ 2SO₃(g) ΔH°₂₉₈ = –197,6 kJ
(c) nSO₃(g) + H₂SO₄(aq) → H₂SO₄·nSO₃(l)
Cho các phát biểu sau:
(1) Ở giai đoạn (b), dùng xúc tác để cân bằng chuyển dịch sang phải, giảm lượng SO₂ trong khí thải.
(2) Ở giai đoạn (b), khi giảm nhiệt độ thì cân bằng chuyển về phía tạo thành SO₃.
(3) Nhiệt độ ở giai đoạn (b) không được quá thấp vì ảnh hưởng đến tốc độ phản ứng.
(4) Sử dụng nhiên liệu hóa thạch để cung cấp năng lượng cho quá trình sản xuất H₂SO₄ có thể gây ô nhiễm môi trường.
(5) Ở giai đoạn (c), người ta dùng nước để hấp thụ SO₃ để thu được dung dịch H₂SO₄ loãng.
Liệt kê phát biểu đúng theo kí hiệu.
Đáp án: (51)
Câu 37. Ammonia (NH₃) là sản phẩm trung gian để sản xuất phân bón, đóng vai trò quan trọng trong nền kinh tế nông nghiệp của thế giới. NH₃ trong công nghiệp được sản xuất từ hydrogen (H₂) và nitrogen (N₂). Trong đó, H₂ được sản xuất chủ yếu từ methane (CH₄) theo phản ứng (1):
CH₄(g) + 2H₂O(g) → CO₂(g) + 4H₂(g) ΔH°₂₉₈
Để cung cấp cho phản ứng tổng hợp NH₃, người ta tiến hành đốt cháy CH₄:
CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g) (2)
Xét các quá trình ở điều kiện chuẩn, biết ΔH°₂₉₈ của các chất như sau:
![]()
Quá trình này sinh ra lượng lớn CO₂, gây ô nhiễm môi trường. Để tạo ra 1 tấn khí H₂ thì tổng lượng khí CO₂ sinh ra từ phản ứng (1) và (2) là x tấn. Giả sử hiệu suất các quá trình là 100%, lượng nhiệt sinh ra ở phản ứng (2) dùng để cung cấp cho phản ứng (1).
Tính x (làm tròn đến một chữ số thập phân).
Đáp án: (52)
Câu 38. Trong công nghiệp chlorine–kiềm, dung dịch sodium chloride (NaCl) bão hòa có nồng độ khoảng 300 g L⁻¹ được điện phân một phần thành “nước muối nghèo” có nồng độ 220 g L⁻¹. “Nước muối nghèo” sau đó được đưa ra khỏi bể điện phân, trong khi nước muối bão hòa mới được bơm vào. Việc này giúp hạn chế sự tạo thành các sản phẩm không mong muốn của quá trình điện phân. Trong bể điện phân, nồng độ dung dịch NaOH (xút) thu được tăng theo dòng điện khoảng 32% (quy đổi theo thiết bị), các xút sản xuất có nồng độ mong muốn, ví dụ 45%, 50%. Giả sử xút không bị thất thoát trong quá trình điện phân. Để sản xuất được một mẻ xút 50% trong phòng thí nghiệm là 10 L thì cần tối thiểu y kg dung dịch NaCl bão hòa.
Biết rằng khối lượng riêng của dung dịch NaCl bão hòa là 1,52 g mL⁻¹. Xác định giá trị của y (làm tròn đến một chữ số thập phân).
Đáp án: (53)
Câu 39. Khí thải từ các phương tiện giao thông là một trong các nguyên nhân gây ô nhiễm không khí, đe dọa sức khỏe con người. Tiêu chuẩn Euro 6 đã quy định giới hạn phát thải của phương tiện giao thông cá nhân như trong bảng dưới đây:

Dựa vào thông tin từ bảng trên, một học sinh đưa ra các phát biểu:
(1) Khí CO có độc tính thấp nên Euro 6 cho phép phát thải CO ở nồng độ cao.
(2) NOₓ sinh ra từ phản ứng nhiên liệu với nitrogen (N₂) trong không khí.
(3) Nếu xe phát thải lượng hydrocarbon vượt quá 100 mg/km thì không đạt tiêu chuẩn Euro 6.
(4) Khí thải phương tiện giao thông chứa khí carbon dioxide (CO₂) góp phần gây hiệu ứng nhà kính.
(5) Người ta sử dụng xăng E5 (chứa 95% xăng thường và 5% ethanol) để giải quyết vấn đề ô nhiễm, do khí thải sẽ không có khí CO.
Liệt kê phát biểu đúng theo kí hiệu.
Đáp án: (54)
Câu 40. Một học sinh sử dụng các thanh kim loại, dây dẫn, bóng đèn nhỏ và các quả chanh để lắp ráp các hệ thống như hình dưới đây:
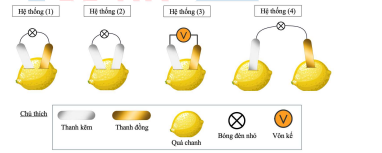
Ở các hệ thống (1), (2), (3), khi lắp ráp không để hai thanh kim loại chạm nhau.
Cho các phát biểu sau:
(1) Các bóng đèn ở hệ thống (1) và (2) đều phát sáng do có dòng điện chạy qua.
(2) Ở hệ thống (2), nếu thay hai thanh kẽm bằng hai thanh đồng (Cu) thì đèn vẫn sáng.
(3) Ở hệ thống (3), giá trị đo được trên vôn kế chính là sức điện động của pin Zn–Cu.
(4) Bóng đèn ở hệ thống (4) sáng hơn hệ thống (1) do sử dụng nhiều chất điện li hơn.
(5) Ở hệ thống (3), giá trị đo được trên vôn kế sẽ giảm theo thời gian.
Liệt kê phát biểu đúng theo kí hiệu.
Đáp án: (55)



