Đề tham khảo môn Hóa học năm 2025 – Bám sát đề thi minh họa là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Đề tham khảo này được xây dựng dựa trên định hướng chính thức từ Bộ Giáo dục và Đào tạo, nhằm giúp học sinh lớp 12 có cái nhìn tổng quan và sát thực tế nhất về cấu trúc, độ khó và các dạng câu hỏi có thể xuất hiện trong kỳ thi tốt nghiệp THPT môn Hóa học năm 2025. Đây là tài liệu lý tưởng để luyện đề, đánh giá năng lực và điều chỉnh chiến lược học tập hiệu quả.
Các kiến thức trọng tâm cần nắm trong đề gồm:
- Hóa học lớp 12 (chiếm phần lớn số câu): Este – Lipit, Amin – Amino axit – Protein, Polime, Đại cương kim loại, Kim loại kiềm – kiềm thổ, Nhôm, Sắt và hợp chất, điện phân, bài toán nhận biết – phân biệt chất.
- Hóa học lớp 11: Các kiến thức nền tảng về axit – bazơ – muối, phản ứng trao đổi ion, oxi hóa – khử, dung dịch, sự điện li, pH.
- Kỹ năng giải đề hiệu quả: Áp dụng bảo toàn (nguyên tố, khối lượng, e), nhận diện hiện tượng hóa học, đồ thị hóa học, tư duy chuỗi phản ứng, mẹo tính nhanh – suy luận logic.
Đề tham khảo 2025 không chỉ là tài liệu giúp học sinh ôn luyện toàn diện mà còn là “bản nháp chính thức” giúp các sĩ tử chuẩn bị tâm lý, kỹ năng và kiến thức vững vàng cho kỳ thi quan trọng phía trước.
Hãy cùng Dethitracnghiem.vn tìm hiểu chi tiết về đề thi này và bắt đầu luyện tập ngay hôm nay để chạm đến mục tiêu điểm số mong muốn!
- Số trang: 4 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THAM KHẢO MÔN HÓA HỌC 2025 – BÁM SÁT ĐỀ THI MINH HỌA




PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn 1 phương án.
Câu 1: Phát biểu nào sau đây đúng khi nói về nguyên tử?
A. Nguyên tử được cấu thành từ các hạt cơ bản là proton và electron.
B. Hạt nhân nguyên tử được cấu thành từ các hạt neutron.
C. Khối lượng của nguyên tử tập trung chủ yếu ở nhân.
D. Nguyên tử có cấu trúc rỗng, gồm vỏ nguyên tử và hạt nhân nguyên tử.
Câu 2: Một kim loại M có cấu hình electron là [Ar]4s¹. Vị trí M trong bảng hệ thống tuần hoàn là
A. ô 19, chu kì 4, nhóm IA.
B. ô 20, chu kì 4, nhóm IB.
C. ô 19, chu kì 4, nhóm IA. (Lưu ý: Đáp án A và C giống hệt nhau, đều đúng. Chọn C theo thứ tự)
D. ô 18, chu kì 3, nhóm VIIIB.
Câu 3: Fructose là một loại monosaccharide có nhiều trong mật ong, có vị ngọt đậm. Công thức phân tử của fructose là
A. C₆H₁₂O₆.
B. (C₆H₁₀O₅)n.
C. C₂H₄O₂.
D. C₁₂H₂₂O₁₁.
Câu 4: Biogas là một loại khí sinh học, được sản xuất bằng cách ủ kín các chất thải hữu cơ trong chăn nuôi, sinh hoạt. Biogas được dùng để đun nấu, chạy máy phát điện sinh hoạt gia đình. Thành phần chính của biogas là
A. N₂.
B. CO₂.
C. CH₄.
D. NH₃.
Câu 5: Quá trình Haber điều chế ammonia được biểu diễn bằng phương trình:
N₂(g) + 3H₂(g) ⇌ 2NH₃(g) ΔrH⁰ = −92kJ·mol⁻¹
Điều kiện nào sau đây sẽ làm tăng tốc độ phản ứng và tăng lượng ammonia tạo thành lúc cân bằng?
A. Giảm nhiệt độ phản ứng.
B. Tăng áp suất hệ phản ứng.
C. Tăng lượng xúc tác.
D. Tăng nhiệt độ phản ứng.
Câu 6: Ester nào sau đây có mùi thơm của chuối chín?
A. Isoamyl acetate.
B. Propyl acetate.
C. Isopropyl acetate.
D. Benzyl acetate.
Câu 7: Chất giặt rửa tổng hợp thường có thành phần chính là
A. muối sodium alkylsulfate (R–OSO₃Na), sodium alkylbenzene sulfonate (R–C₆H₄–SO₃Na).
B. glycerol và ethanol.
C. saponin trong bồ hòn và bồ kết.
D. muối sodium hoặc potassium của acid béo (thường là các gốc acid béo no).
Câu 8: Polysaccharide X là chất rắn, ở dạng bột vô định hình, màu trắng và được tạo thành trong cây xanh nhờ quá trình quang hợp. Thủy phân X, thu được monosaccharide Y. Phát biểu nào sau đây đúng?
A. Y hòa tan được Cu(OH)₂.
B. X có phản ứng tráng bạc.
C. Phân tử khối của X là 162.
D. X dễ tan trong nước lạnh.
Câu 9: Chất nào sau đây là amine bậc một?
A. (CH₃)₂CHNH₂.
B. (CH₃)₂NH.
C. (C₂H₅)₃N.
D. (C₂H₅)₂NH.
Câu 10: Phát biểu nào sau đây là sai khi nói về tính điện di của amino acid?
A. Trong dung dịch, dạng tồn tại chủ yếu của amino acid chỉ phụ thuộc vào pH của dung dịch.
B. Ở pH thấp, amino acid tồn tại chủ yếu ở dạng anion (tích điện âm), di chuyển về điện cực dương trong điện trường.
C. Ở pH cao, amino acid tồn tại chủ yếu ở dạng anion (tích điện âm), di chuyển về điện cực dương trong điện trường.
D. Tính điện di của amino acid là khả năng di chuyển khác nhau trong điện trường tùy thuộc và pH của môi trường.
Câu 11: Loại polymer nào sau đây được điều chế bằng phản ứng trùng ngưng?
A. PVC
B. Cao su buna
C. PS
D. Nylon-6,6
Câu 12: Cho các cặp oxi hoá – khử và thế điện cực chuẩn tương ứng: Phản ứng nào sau đây đúng?
Phản ứng nào sau đây đúng?
A. Zn + Cr³⁺ → Zn²⁺ + Cr²⁺.
B. Ni + Cr³⁺ → Zn²⁺ + Cr. (Typo: Should be Ni²⁺)
C. Zn + Cr²⁺ → Zn²⁺ + Cr.
D. Ni + Cr²⁺ → Ni²⁺ + Cr²⁺. (Typo: Should be Cr)
Câu 13: Điện phân dung dịch MSO₄ (M là kim loại) với điện cực trơ, cường độ dòng điện không đổi. Sau thời gian t giây, thu được a mol khí ở anode. Nếu thời gian điện phân là 2t giây thì tổng số mol khí thu được ở cả hai điện cực là 2,5a mol. Giả sử hiệu suất điện phân là 100%, khí sinh ra không tan trong nước. Phát biểu nào sau đây sai?
A. Tại thời điểm 2t giây, có bọt khí ở cathode.
B. Tại thời điểm t giây, ion M²⁺ chưa bị điện phân hết.
C. Dung dịch sau điện phân có pH < 7.
D. Khi thu được 1,8a mol khí ở (Incomplete sentence – assumes typo from previous exam Q13 with alternative value? Based on 2.5a derivation, C is incorrect)
Câu 14: Kim loại có những tính chất vật lí chung nào sau đây?
A. Tính dẻo, tính dẫn điện, nhiệt độ nóng chảy cao.
B. Tính dẻo, tính dẫn điện, có khối lượng riêng lớn và có ánh kim.
C. Tính dẻo, tính dẫn điện, tính dẫn nhiệt và có ánh kim.
D. Tính dẻo, có ánh kim, rất cứng.
Câu 15: Cho bột Fe vào dung dịch AgNO₃ và Cu(NO₃)₂. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X gồm hai muối và chất rắn Y gồm hai kim loại. Hai muối trong X và hai kim loại trong Y lần lượt là:
A. Cu(NO₃)₂; Fe(NO₃)₂ và Cu; Fe.
B. Cu(NO₃)₂; Fe(NO₃)₂ và Ag, Cu.
C. Fe(NO₃)₂; Fe(NO₃)₃ và Cu; Ag.
D. Cu(NO₃)₂; AgNO3 và Cu; Ag.
Câu 16: Trong phòng thí nghiệm, kim loại Na được bảo quản bằng cách ngâm trong chất lỏng nào sau đây?
A. Nước.
B. Dầu hỏa.
C. Giấm ăn.
D. Cồn.
Câu 17: Cho sơ đồ chuyển hóa sau:![]() Biết X, Y, Z, E, G là các hợp chất khác nhau, mỗi mũi tên ứng với một phương trình hóa học của phản ứng xảy ra giữa hai chất tương ứng. Các chất E,G trong sơ đồ trên lần lượt là
Biết X, Y, Z, E, G là các hợp chất khác nhau, mỗi mũi tên ứng với một phương trình hóa học của phản ứng xảy ra giữa hai chất tương ứng. Các chất E,G trong sơ đồ trên lần lượt là
A. Na₂SO₄, NaOH.
B. NaHCO₃, BaCl₂.
C. CO₂, NaHSO₄. (Based on previous analysis of this exact question)
D. Na₂CO₃, HCl.
Câu 18: Nhận xét nào sau đây là đúng?
A. Sắt thuộc nhóm kim loại nặng và có nhiệt độ nóng chảy cao nhất trong dãy kim loại chuyển tiếp thứ nhất.
B. Trong số các kim loại chuyển tiếp dãy thứ nhất, chromium có nhiệt độ nóng chảy cao nhất.
C. Chromium có độ cứng cao nên được dùng mạ lên các thiết bị để chống mài mòn.
D. Các đơn chất kim loại có khối lượng riêng lớn sẽ có độ cứng cao.
PHẦN II. Câu hỏi trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu thí sinh chọn đúng hoặc sai.
Câu 1: Cho sơ đồ phản ứng sau: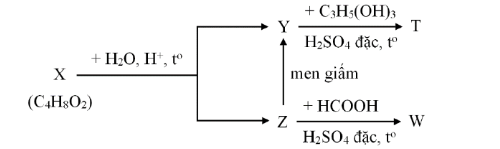 Biết rằng X, Y, Z, T, W là các hợp chất hữu cơ khác nhau; T chỉ chứa một loại nhóm chức.
Biết rằng X, Y, Z, T, W là các hợp chất hữu cơ khác nhau; T chỉ chứa một loại nhóm chức.
a) Từ CH₃OH có thể điều chế trực tiếp được Y.
b) Z có trong thành phần của nước rửa tay khô có tác dụng diệt khuẩn.
c) Phần trăm khối của O trong T là 36,36%.
d) Công thức phân tử của W là C₂H₄O₂.
Câu 2: Tiến hành thí nghiệm phản ứng màu biuret của lòng trắng trứng (protein) theo các bước sau đây:
Bước 1: Cho vào ống nghiệm 2 giọt dung dịch CuSO₄ 2% và 1 mL dung dịch NaOH 30%.
Bước 2: Lắc nhẹ, gạn lớp dung dịch để giữ kết tủa.
Bước 3: Thêm 4 mL dung dịch lòng trắng trứng vào ống nghiệm, lắc đều.
a) Cần lấy dư dung dịch NaOH để đảm bảo môi trường cho phản ứng tạo phức.
b) Có thể thay thế dung dịch lòng trắng trứng bằng dung dịch Gly–Ala–Val.
c) Sau bước 1, trong ống nghiệm xuất hiện kết tủa màu xanh.
d) Sau bước 3, kết tủa bị hoà tan và dung dịch có màu xanh lam.
Câu 3: Tinh luyện đồng (Cu) bằng phương pháp điện phân được tiến hành như sau:
Các khối đồng có độ tinh khiết thấp được gắn với cực dương của nguồn điện;
Các tấm đồng mỏng có độ tinh khiết cao được gắn với cực âm của nguồn điện.
Dung dịch điện phân là dung dịch CuSO₄.
a) Tại anode chủ yếu xảy ra quá trình oxi hoá H₂O thành khí O₂ và H⁺.
b) Các tạp chất không bị điện phân sẽ được giữ lại và bám vào anode.
c) Nồng độ ion Cu²⁺ trong dung dịch không đổi trong quá trình điện phân.
d) Khối lượng Cu tan ra từ anode bằng khối lượng Cu bám vào cathode.
Câu 4: Cho kim loại M và các hợp chất X, Y, Z thỏa mãn các phương trình hóa học sau:
(1) 2M + 3Cl₂ —(t⁰)→ 2MCl₃ (2) 2M + 6HCl → 2MCl₃ + 3H₂
(3) 2M + 2X + 2H₂O → 2Y + 3H₂ (4) Y + CO₂ + 2H₂O → X + KHCO₃
a) X có thể là NaOH hoặc KOH
b) Các chất Y, Z lần lượt là: KAlO₂, Al(OH)₃. (Z not defined in reactions)
c) Trong công nghiệp, kim loại M được sản xuất bằng phương pháp điện phân nóng chảy oxide. Biết hiệu suất của quá trình chuyển hóa M₂O₃ thành M là 95,4%. Để sản xuất 5,4 tấn M cần sử dụng 10,7 tấn nguyên liệu M₂O₃.
d) Hấp thụ hoàn toàn 3,7185 lít khí CO₂ (đkc) vào dung dịch chứa 0,15 mol X và 0,1 mol Ba(OH)₂, thu được 29,55 gam kết tủa
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
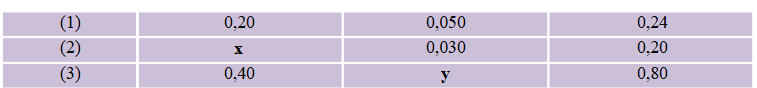
Câu 1: Xét phản ứng hóa học đơn giản giữa hai chất A và B theo phương trình: A + B → C. Từ thông tin đã cho, Tính giá trị của y trong bảng dưới đây (làm tròn đến hàng phần trăm):![]()
 Câu 2: Ester X có công thức phân tử C₄H₆O₂. Cho X tác dụng với dung dịch NaOH, thu được sản phẩm có hai muối. Có bao nhiêu công thức cấu tạo của X thỏa mãn tính chất trên?
Câu 2: Ester X có công thức phân tử C₄H₆O₂. Cho X tác dụng với dung dịch NaOH, thu được sản phẩm có hai muối. Có bao nhiêu công thức cấu tạo của X thỏa mãn tính chất trên?
Câu 3: Cho các chất: saccharose, glucose, fructose, ethyl formate, formic acid và aldehyde acetic. Trong các chất trên, số chất vừa có khả năng tham gia phản ứng tráng bạc vừa có khả năng phản ứng với Cu(OH)₂ ở điều kiện thường là bao nhiêu?
Câu 4: Dung dịch X gồm CuSO₄ và NaCl. Tiến hành điện phân dung dịch X với điện cực trơ, màng ngăn xốp, cường độ dòng điện 0,5A, hiệu suất điện phân là 100%. Lượng khí sinh ra từ bình điện phân và lượng kim loại Cu sinh ra ở cathode theo thời gian điện phân được cho ở bảng sau: Số mol NaCl trong X là?
Số mol NaCl trong X là?
Câu 5: Paracetamol (còn có tên gọi khác là acetaminophen) là hoạt chất giúp giảm đau và hạ sốt… được sử dụng nhiều trong y học. Thuốc paracetamol được tổng hợp từ phenol qua nhiều giai đoạn, trong đó giai đoạn tạo ra paracetamol từ p-amino phenol và acetic anhydride xảy ra theo phương trình hóa học sau: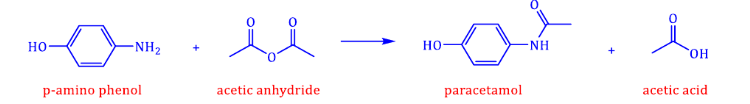 Để sản xuất 4530 hộp thuốc paracetamol 500 mg (mỗi hộp gồm 10 vỉ, mỗi vỉ gồm 10 viên, mỗi viên chứa 500 mg paracetamol) cần dùng tối thiểu m kg p-amino phenol. Biết hiệu suất phản ứng tính theo p-amino phenol là 80%. Giá trị của m bằng bao nhiêu? (Kết quả làm tròn đến hàng đơn vị).
Để sản xuất 4530 hộp thuốc paracetamol 500 mg (mỗi hộp gồm 10 vỉ, mỗi vỉ gồm 10 viên, mỗi viên chứa 500 mg paracetamol) cần dùng tối thiểu m kg p-amino phenol. Biết hiệu suất phản ứng tính theo p-amino phenol là 80%. Giá trị của m bằng bao nhiêu? (Kết quả làm tròn đến hàng đơn vị).
Câu 6: Một vết nứt trên đường ray tàu hỏa có thể tích 10, 633 m³. Dùng hỗn hợp tecmit (Al và Fe₂O₃ theo tỉ lệ mol tương ứng 2:1 ) để hàn vết nứt trên. Biết: lượng Fe cần hàn cho vết nứt bằng 79% lượng Fe sinh ra; khối lượng riêng của sắt là 7,9gam / cm³ ; chỉ xảy ra phản ứng khử Fe₂O₃ thành Fe với hiệu suất của phản ứng bằng 96%. Khối lượng của hỗn hợp tecmit (g) tối thiểu cần dùng là? (làm tròn đến hàng đơn vị)
Mục đích tổ chức kỳ thi Tốt nghiệp THPT năm 2025 là gì?
Căn cứ theo các văn bản chỉ đạo và hướng dẫn của Bộ Giáo dục và Đào tạo, kỳ thi Tốt nghiệp THPT năm 2025 được tổ chức nhằm các mục đích chính sau:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo chương trình giáo dục phổ thông mới.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ cho các cơ sở giáo dục đại học, cao đẳng tuyển sinh.
– Góp phần đánh giá chất lượng giáo dục tại các địa phương và trên toàn quốc, từ đó làm cơ sở để điều chỉnh nội dung chương trình và phương pháp dạy học trong các nhà trường.
Thí sinh thi tốt nghiệp THPT năm 2025 có bắt buộc phải thi môn Hóa học không?
Theo quy định hiện hành của Bộ GD&ĐT, thí sinh dự thi Tốt nghiệp THPT năm 2025 phải tham gia 3 bài thi bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
Bên cạnh đó, thí sinh chọn một trong hai bài thi tổ hợp:
– Tổ hợp Khoa học Tự nhiên (KHTN): gồm các môn Vật lí, Hóa học, Sinh học.
– Tổ hợp Khoa học Xã hội (KHXH): gồm các môn Lịch sử, Địa lí, Giáo dục công dân (áp dụng đối với học sinh học chương trình GDPT).
Trong bài thi tổ hợp KHTN, môn Hóa học là một trong ba môn thành phần. Tuy nhiên, thí sinh không bắt buộc phải thi môn Hóa học nếu không chọn bài thi tổ hợp KHTN. Việc thi môn Hóa học là cần thiết trong trường hợp thí sinh lựa chọn tổ hợp KHTN để xét tốt nghiệp hoặc để phục vụ mục tiêu xét tuyển vào đại học, cao đẳng ở các ngành yêu cầu điểm môn Hóa học.
Vì vậy, Đề tham khảo tốt nghiệp THPT năm 2025 môn Hóa học là tài liệu quan trọng do Bộ Giáo dục và Đào tạo công bố nhằm hỗ trợ học sinh trong quá trình ôn luyện. Đề giúp các em tiếp cận cấu trúc và dạng thức đề thi, đánh giá năng lực bản thân, củng cố kiến thức và rèn luyện kỹ năng làm bài, từ đó chuẩn bị tốt nhất cho kỳ thi chính thức.




