Đề thi thử Đại học 2025 lần 1 môn Hóa học Sở GD Bắc Giang là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Đề thi được thiết kế bám sát cấu trúc đề minh họa 2025 của Bộ GD&ĐT, đảm bảo độ phủ kiến thức toàn diện theo chương trình Hóa học lớp 12, đồng thời có sự phân loại rõ rệt để đánh giá năng lực học sinh. Các chuyên đề trọng tâm xuất hiện trong đề gồm: Este – Lipit, Cacbohidrat, Amin – Amino axit – Protein, Polime, Đại cương kim loại, Kim loại nhóm IA – IIA – Al, phản ứng điện phân, bài toán đồ thị và câu hỏi thực tiễn.
Điểm nổi bật của đề thi đến từ Sở GD Phú Thọ là việc kết hợp linh hoạt giữa lý thuyết cơ bản và bài tập vận dụng cao, có nhiều câu hỏi thiên về bản chất hóa học và phân tích tình huống thực tế – điều này giúp học sinh vừa rèn luyện tư duy vừa nâng cao kỹ năng làm bài nhanh và chính xác.
Hãy cùng Dethitracnghiem.vn tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 4 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 SỞ GD BẮC GIANG





PHẦN I. CÂU TRẮC NGHIỆM NHIỀU PHƯƠNG ÁN LỰA CHỌN. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1: Cho các phát biểu sau:
(1) Hầu hết các muối kim loại đều dễ tan trong nước;
(2) Ion NH4+ tác dụng với dung dịch acid tạo kết tủa màu trắng;
(3) Muối ammonium tác dụng với dung dịch base thu được khí có mùi khai;
(4) Hầu hết muối ammonium đều bền nhiệt.
Phát biểu đúng là
A. (2) và (3)
B. (1) và (2)
C. (3)
D. (2) và (4).
Câu 2: Hợp chất hữu cơ X có công thức cấu tạo như sau: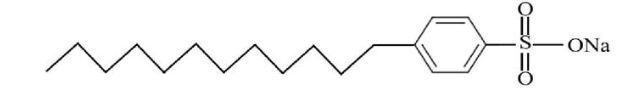
Phát biểu nào sau đây không đúng?
A. X được sử dụng để sản xuất xà phòng.
B. X thuộc loại muối sodium alkylbenzenesulfonate.
C. X có đầu ưa nước và đuôi kị nước.
D. X có công thức phân tử là C15H25SO3Na.
Câu 3: Tiến hành điện phân dung dịch NaCl bão hoà với điện cực trơ, không sử dụng màng ngăn xốp. Bố trí thí nghiệm như hình vẽ sau:
Phát biểu nào sau đây đúng?
A. Quá trình xảy ra tại anode là: 2H2O + 2e → H2 + 2OH–.
B. Thí nghiệm trên được sử dụng để điều chế kim loại Na trong công nghiệp.
C. Dung dịch thu được sau điện phân có khả năng tẩy màu.
D. Quá trình xảy ra tại cathode là: 2H2O → O2 + 4H+ + 4e.
Câu 4: Dung dịch amine nào sau đây không làm quỳ tím chuyển sang màu xanh?
A. Aniline.
B. Ethylamine.
C. Methylamine.
D. Dimethylamine.
Câu 5: Thí nghiệm nào sau đây không xảy ra phản ứng?
A. Cho kim loại Cu vào dung dịch HNO3.
B. Cho kim loại Fe vào dung dịch FeCl3.
C. Cho kim loại Zn vào dung dịch CuSO4.
D. Cho kim loại Ag vào dung dịch HCl.
Câu 6: Ester X được tạo bởi methyl alcohol và acetic acid. Công thức của X là
A. HCOOCH3.
B. CH3COOCH3.
C. CH3COOC2H5.
D. CH3COOCH3.
Câu 7: Cation R3+ có cấu hình electron ở phân lớp ngoài cùng là 2p6. Cấu hình electron của nguyên tử R là
A. 1s22s22p6.
B. 1s22s22p63s23p1.
C. 1s22s22p63s2.
D. 1s22s22p5.
Câu 8: Trong phân tử chất nào sau đây có 2 nhóm amino (-NH2) và 1 nhóm carboxyl (-COOH)?
A. Glutamic acid.
B. Formic acid.
C. Lysine.
D. Alanine.
Câu 9: Polymer X có công thức: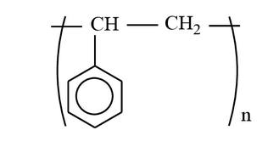
Tên của X là
A. poly(vinyl chloride).
B. poly(methyl methacrylate).
C. polyethylene.
D. polystyrene.
Câu 10: Tinh bột thuộc loại polysaccharide, là một trong những chất dinh dưỡng cơ bản của người và động vật. Phân tử tinh bột được tạo thành từ nhiều đơn vị
A. α-fructose.
B. β-fructose.
C. β-glucose.
D. α-glucose.
Câu 11: Bradykinin là một peptide có trong huyết tương, có vai trò quan trọng trong phản ứng viêm (gây giãn mạch máu, tăng tính thấm mao mạch và gây đau). Bradykinin có trật tự sắp xếp các amino acid như sau: Arg-Pro-Pro-Gly-Phe-Ser-Pro-Phe-Arg.
Cho các nhận định sau:
(a) Bradykinin thuộc loại nonapeptide.
(b) Thuỷ phân hoàn toàn bradykinin thu được 5 amino acid.
(c) Thuỷ phân không hoàn toàn bradykinin thu được tối đa 7 dipeptide.
(d) Bradykinin phản ứng với Cu(OH)2 trong môi trường kiềm tạo dung dịch màu xanh lam.
Các nhận định đúng là
A. (a), (d).
B. (b), (c).
C. (b), (c).
D. (a), (d).
Câu 12: Ethyl propionate là ester có mùi thơm của dứa. Công thức của ethyl propionate là
A. HCOOC2H5.
B. C2H5COOC2H5.
C. C3H7COOCH3.
D. CH3COOCH3.
Câu 13: Cho thứ tự sắp xếp một số cặp oxi hoá – khử của kim loại trong dãy điện hoá: Mg2+/Mg; Zn2+/Zn; Fe2+/Pb; Pb2+/Hg2+/Hg.
Ion kim loại có tính oxi hoá yếu nhất trong dãy là
A. Mg2+.
B. Mg2+.
C. Pb2+.
D. Zn2+.
Câu 14: Sự ăn mòn kim loại gây ảnh hưởng, phá huỷ dần dần máy móc, thiết bị, các phương tiện giao thông vận tải, nhà cửa, cơ sở hạ tầng,… Trong quá trình ăn mòn kim loại, kim loại bị ăn mòn đóng vai trò là chất
A. proton.
B. electron.
C. nhân electron.
D. nhân proton.
Câu 15: Cho phổ khối lượng của chất X như sau: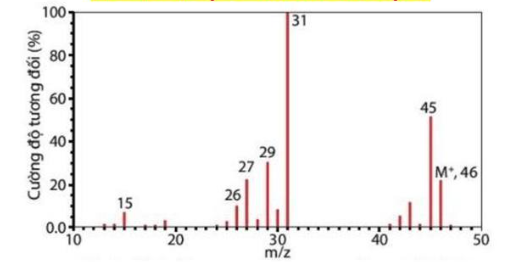
Chất X có thể là
A. acetic acid.
B. benzene.
C. methyl acetate.
D. ethanol.
Câu 16: Polymer dùng để sản xuất cao su buna-N được tổng hợp bằng phản ứng trùng hợp hợp chất nào sau đây với buta-1,3-diene?
A. Styrene.
B. Acrylonitrile.
C. Isoprene.
D. Caprolactam.
Câu 17: Cho sơ đồ pin Galvan Zn-Cu ở điều kiện chuẩn như hình vẽ sau: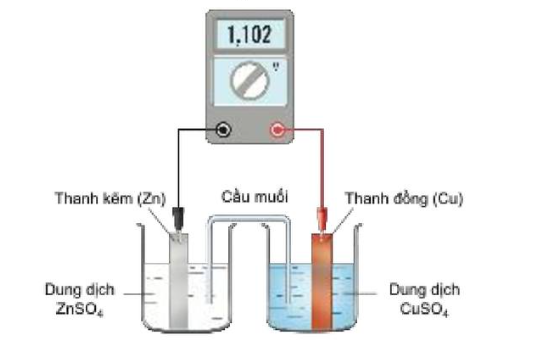
Phát biểu nào sau đây đúng?
A. Thế điện cực chuẩn của cặp Cu2+/Cu có giá trị bằng 1,102 V.
B. Dòng điện trong pin có chiều từ điện cực Zn sang điện cực Cu.
C. Tại cathode của pin xảy ra quá trình Cu2+ → Cu + 2e.
D. Phản ứng xảy ra tại anode xảy ra là Zn + Cu2+ → Zn2+ + Cu.
Câu 18: Điểm chớp cháy là nhiệt độ thấp nhất ở áp suất khí quyển mà một chất lỏng hoặc vật liệu dễ bay hơi tạo thành lượng hơi đủ để bốc cháy trong không khí khi tiếp xúc nguồn lửa. Điểm chớp cháy được sử dụng để phân biệt chất lỏng dễ cháy với chất lỏng có thể gây cháy, chất lỏng có điểm chớp cháy nhỏ hơn 37,8 °C được gọi là chất lỏng dễ cháy, chất lỏng có điểm chớp cháy lớn hơn 37,8 °C được gọi là điểm cháy (oC). Cho bảng số liệu sau: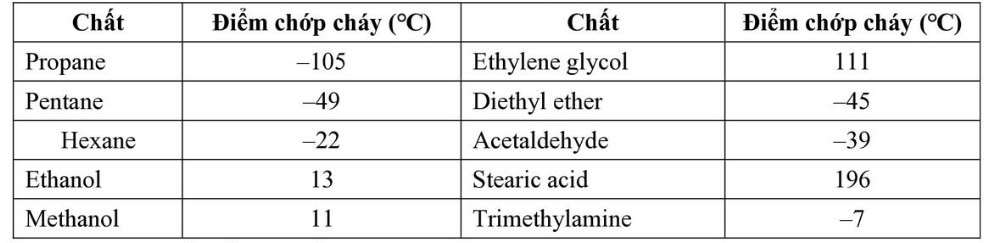
Trong bảng trên, số chất lỏng dễ cháy là
A. 7.
B. 6.
C. 8.
D. 9.
PHẦN II. CÂU HỎI TRẮC NGHIỆM ĐÚNG SAI. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu thí sinh chọn đúng hoặc sai.
Câu 1. Saccharose monolaurate được tổng hợp bằng phản ứng ester hoá giữa saccharose (đường mía hoặc đường củ cải) với lauric acid, một acid béo no có nhiều trong dầu dừa. Saccharose monolaurate được sử dụng như một chất nhũ hoá và chất hoạt động bề mặt trong thực phẩm và mỹ phẩm. Saccharose monolaurate được đánh giá an toàn và thân thiện với môi trường. Công thức cấu tạo của saccharose monolaurate như sau: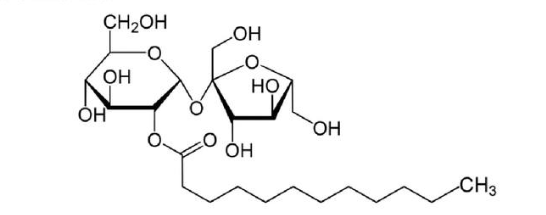
Câu 2. Aspirin là một hợp chất chức sử dụng làm giảm đau, hạ sốt. Sau khi uống, aspirin bị thuỷ phân trong cơ thể sẽ tạo thành acid salicylic. Salicylic acid ức chế quá trình sinh tổng hợp prostaglandin (chất gây đau, sốt và viêm khi nồng độ trong máu cao hơn mức bình thường).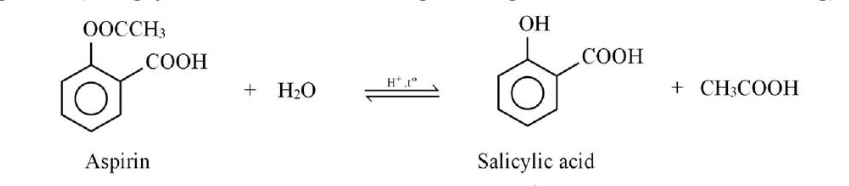 a) Thủy phân aspirin trong môi trường base thu được muối carboxylate và alcohol.
a) Thủy phân aspirin trong môi trường base thu được muối carboxylate và alcohol.
b) Công thức phân tử của aspirin là C9H8O4.
c) 1 mol salicylic acid tác dụng tối đa với 2 mol NaOH trong dung dịch.
d) Trong một phân tử aspirin có chứa 4 liên kết π.
Câu 3. Hai nhóm học sinh tiến hành thí nghiệm điện phân dung dịch CuSO4 với một điện cực than
chì và một điện cực bằng đồng (bỏ qua sự thay đổi thể tích của dung dịch khi điện phân).
Nhóm 1: Nối điện cực than chì với cực dương và điện cực đồng với cực âm của nguồn điện.
Nhóm 2: Nối điện cực than chì với cực âm và điện cực đồng với cực dương của nguồn điện.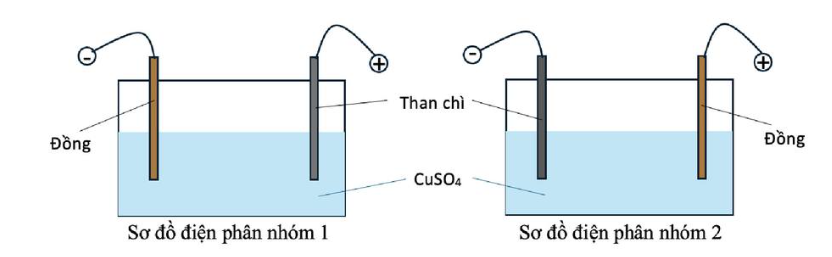 Hai nhóm đều đưa ra giả thuyết sau: trong quá trình điện phân, nồng độ ion Cu2+ giảm dần ứng với
Hai nhóm đều đưa ra giả thuyết sau: trong quá trình điện phân, nồng độ ion Cu2+ giảm dần ứng với
màu xanh của dung dịch nhạt dần.
a) Ở nhóm thứ hai, tại anode xảy ra quá trình oxi hoá đồng.
b) Đối với cả hai nhóm đều có kim loại đồng bám vào cathode.
c) Ở nhóm thứ nhất, pH của dung dịch điện phân giảm dần.
d) Giả thuyết đúng với nhóm thứ nhất và sai với nhóm thứ hai.
Câu 4. Polymer là các hợp chất cao phân tử có vai trò quan trọng trong cuộc sống và công nghiệp.
Tuỳ theo thành phần và cấu trúc mà polymer có thể có tính dẻo, tính đàn hồi, … Dựa vào sự biến đổi
khác nhau khi bị đun nóng, polymer có thể được chia thành polymer nhiệt dẻo và polymer nhiệt rắn.
a) Polymer nhiệt rắn bị nóng chảy khi đun nóng.
b) PE và PVC là các polymer có tính dẻo và thuộc loại polymer nhiệt dẻo.
c) Hầu hết polymer tan được trong nước và có nhiệt độ nóng chảy xác định.
d) Tính chất vật lí của polymer phụ thuộc vào cấu tạo.
PHẦN III. CÂU TRẮC NGHIỆM TRẢ LỜI NGẮN. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Thuỷ phân hoàn toàn m gam triglyceride X bằng 48 gam dung dịch NaOH 30% đun nóng (dùng dư 20% so với lượng phản ứng), thu được glycerol và 89,0 gam hỗn hợp muối của acid béo. Khối lượng mol của X có giá trị bằng bao nhiêu?
Câu 2. Trong công nghiệp, nhôm (aluminium) được sản xuất bằng phương pháp điện phân nóng chảy aluminium oxide (có tên cryolite) với các điện cực đều làm bằng than chì (carbon graphite). Trong quá trình này, kim loại Al được tạo thành ở cathode, khí oxygen sinh ra tại anode, phản ứng với than chì tạo CO, CO2 và làm giảm khối lượng anode. Trong một quá trình sản xuất nhôm, tại cathode thu được 5,4 kg Al, tại anode thu được hỗn hợp x kg gồm CO2 và CO (trong đó CO chiếm 70% về thể tích) và khối lượng anode giảm m kg. Biết rằng các tạp chất đều trơ (không tham gia quá trình điện điện cực và phản ứng), toàn bộ oxygen sinh ra đều phản ứng với than chì. Giá trị của m bằng bao nhiêu (làm tròn kết quả đến hàng phần trăm)?
Câu 3. Gang là hợp kim của sắt (iron) với carbon và một số nguyên tố khác. Gang được sản xuất từ nguyên liệu là quặng hematite (thành phần chính là Fe2O3) và carbon, với hiệu suất chuyển hóa từ Fe2O3 thành sắt là 95%. Để sản xuất được 5,9 tấn gang (chứa 95% Fe về khối lượng) cần dùng m tấn quặng hematite (chứa 80% Fe2O3 về khối lượng, các tạp chất khác không chứa Fe). Giá trị của m bằng bao nhiêu (làm tròn kết quả đến hàng phần mười)?
Câu 4. Cho các phân tử: tinh bột, cellulose, saccharose, maltose, fructose và glucose. Số phân tử có chứa liên kết glycoside là bao nhiêu?
Câu 5. Ở một lò nung vôi công nghiệp, cứ sản xuất được 1 000 kg vôi sống cần dùng m kg than đá làm nhiên liệu. Biết rằng: – Than đá chứa 84% carbon về khối lượng, còn lại là các tạp chất trơ.
– Có 50% lượng nhiệt tỏa ra từ nhiên liệu được hấp thụ để phân huỷ đá vôi.
– Nhiệt tạo thành của các chất được cho trong bảng sau: Giá trị của m bằng bao nhiêu (làm tròn kết quả đến hàng đơn vị)?
Giá trị của m bằng bao nhiêu (làm tròn kết quả đến hàng đơn vị)?
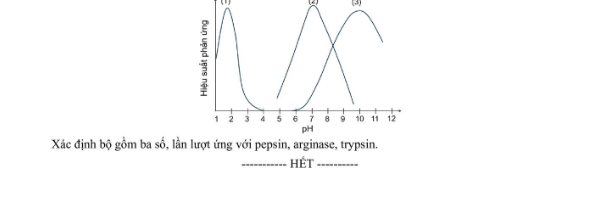
Câu 6. Enzyme là các protein xúc tác sinh học, giúp tăng tốc độ các phản ứng sinh hoá trong cơ thể như quá trình trao đổi, chuyển hoá năng lượng,…
Trong cơ thể, trypsin là enzyme được tiết vào ruột non giúp thuỷ phân các peptide thành amino acid ở hoạt động tối ưu pH khoảng 7,5 – 8,5; arginase là enzyme xúc tác quá trình thuỷ phân arginine (chủ yếu diễn ra ở gan) thành ornithine và hoạt động tối ưu ở pH khoảng 9,5; pepsin là enzyme có trong dạ dày, xúc tác quá trình phân giải protein thành các peptide ngắn, hoạt động tối ưu ở môi trường acid với pH khoảng 1,5 – 2,0.
Hiệu suất xúc tác của các enzyme trypsin, arginase, pepsin (được đánh số ngẫu nhiên từ 1 đến 3) theo ảnh hưởng pH của môi trường được minh họa ở đồ thị sau.
Mục đích tổ chức kỳ thi Tốt nghiệp THPT năm 2025 là gì?
Căn cứ theo các văn bản chỉ đạo và hướng dẫn của Bộ Giáo dục và Đào tạo, kỳ thi Tốt nghiệp THPT năm 2025 được tổ chức nhằm các mục đích chính sau:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo chương trình giáo dục phổ thông mới.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ cho các cơ sở giáo dục đại học, cao đẳng tuyển sinh.
– Góp phần đánh giá chất lượng giáo dục tại các địa phương và trên cả nước, làm cơ sở để điều chỉnh nội dung, phương pháp dạy học trong các nhà trường.
Thí sinh thi tốt nghiệp THPT năm 2025 có bắt buộc phải thi môn Hóa học không?
Theo quy định hiện hành của Bộ GD&ĐT, thí sinh dự thi Tốt nghiệp THPT năm 2025 phải tham gia 3 bài thi bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
Ngoài ra, thí sinh chọn một trong hai bài thi tổ hợp:
– Tổ hợp Khoa học Tự nhiên (KHTN): gồm các môn Vật lí, Hóa học, Sinh học.
– Tổ hợp Khoa học Xã hội (KHXH): gồm các môn Lịch sử, Địa lí, Giáo dục công dân (đối với học sinh chương trình GDPT).
Trong bài thi tổ hợp KHTN, môn Hóa học là một trong ba môn thành phần. Tuy nhiên, thí sinh không bắt buộc phải thi môn Hóa học, trừ khi chọn bài thi tổ hợp KHTN để xét tốt nghiệp hoặc phục vụ mục tiêu xét tuyển đại học, cao đẳng vào các ngành có yêu cầu môn Hóa học.
Vì vậy, Đề thi thử tốt nghiệp THPT 2025 lần 1 môn Hóa học do Sở Giáo dục và Đào tạo Bắc Giang ban hành là tài liệu luyện tập quan trọng dành cho thí sinh chọn tổ hợp KHTN. Đề giúp học sinh ôn tập, củng cố kiến thức, đánh giá năng lực bản thân và nâng cao kỹ năng làm bài, từ đó chuẩn bị tốt nhất cho kỳ thi chính thức sắp tới.




