Đề thi thử Đại học 2025 môn Hóa học – Đề 1 là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Đề 1 trong bộ đề thi thử năm 2025 được biên soạn nhằm mô phỏng sát nhất cấu trúc và độ khó của đề thi tốt nghiệp THPT môn Hóa học chính thức. Với thời lượng 50 phút và hình thức 40 câu trắc nghiệm, đề kiểm tra toàn diện các nội dung trọng tâm của chương trình Hóa học THPT, đặc biệt là kiến thức lớp 12.
Những kiến thức cần nắm vững để giải tốt đề này bao gồm:
- Hóa học vô cơ: Dãy điện hóa, phản ứng oxi hóa – khử, kim loại tác dụng với dung dịch muối, phản ứng nhiệt luyện – điện phân.
- Hóa học hữu cơ: Các loại hợp chất như ankan, anken, ankin, ancol, este, axit cacboxylic, amin, amino axit và peptit.
- Kỹ năng giải bài tập: Tính toán theo phương trình hóa học, đồ thị, so sánh hiệu suất, bài toán hỗn hợp nhiều chất.
- Câu hỏi thực tiễn – nhận biết hóa chất – phân biệt dung dịch – xử lý số liệu thí nghiệm.
Đề này phù hợp cho các bạn học sinh muốn kiểm tra năng lực hiện tại, tìm ra điểm yếu cần khắc phục và chuẩn bị kỹ lưỡng hơn cho kỳ thi thật sắp tới.
Hãy cùng Dethitracnghiem.vn cùng tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 – ĐỀ SỐ 1






PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18 . Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Kim loại nào sau đây điều chế được bằng phương pháp thủy luyện?
A. Au.
B. Ca.
C. Na.
D. Mg.
Câu 2. Đun nước lâu ngày thấy xuất hiện lớp cặn bám vào đáy ấm đun nước. Để loại bỏ lớp cặn có thể dùng dung dịch nào sau đây?
A. Cồn
B. Giấm ăn.
C. Nước vôi.
D. Muối ăn.
Câu 3. Loại polymer nào sau đây có chứa nguyên tố nitrogen?
A. Polystyrene.
B. Poly(vinyl chloride).
C. Polyisoprene.
D. Nylon-6,6.
Câu 4. Kim loại tungsten (W) được sử dụng làm dây tóc bóng điện. Ứng dụng này được dựa trên cơ sở tính chất vật lí nào sau đây của tungsten?
A. Tính dẫn nhiệt.
B. Tỉ trọng nhỏ.
C. Tính dẻo.
D. Nhiệt độ nóng chảy
Câu 5. Thành phần dịch vị dạ dày gồm 95% là nước, enzyme và hydrochloric acid. Sự có mặt của hydrochloric acid làm cho pH của dịch vị trong khoảng từ 2 – 3. Khi độ acid trong dịch vị dạ dày tăng thì dễ bị ợ chua, ợ hơi, ói mửa, buồn nôn, loét dạ dày, tá tràng. Để làm giảm bớt lượng acid dư trong dịch vị dạ dày người ta thường uống thuốc muối dạ dày “Nabica” từng lượng nhỏ và cách quãng. Phát biểu nào sau đây là sai?
A. Công thức hoá học của thuốc muối “Nabica” là NaHCO₃.
B. Khi uống từng lượng nhỏ và cách quãng thuốc muối “Nabica” thì pH của dịch vị dạ dày sẽ tăng từ từ.
C. Khi uống thuốc muối “Nabica” thì sẽ sinh ra khí carbon dioxide.
D. Nếu có 10 mL dịch vị dạ dày và coi pH của dạ dày hoàn toàn do hydrochloric acid gây ra, để nâng pH của dạ dày từ pH=1 lên pH=2 ta cần dùng hết 0,0756 gam thuốc muối Nabica (với giả thiết Nabica là nguyên chất).
Câu 6. Một mẫu nước được thử nghiệm định tính để xác định sự có mặt của một số ion. Mẫu nước được cho vào 4 ống nghiệm, sau đó nhỏ mỗi loại thuốc thử vào mỗi ống nghiệm và ghi nhận hiện tượng như bảng dưới đây: Mẫu nước trên có thể chứa những ion nào trong số các ion sau đây: (1) H⁺; (2) Ca²⁺; (3) SO₄²⁻; (4) HCO₃⁻; (5) CO₃²⁻?
Mẫu nước trên có thể chứa những ion nào trong số các ion sau đây: (1) H⁺; (2) Ca²⁺; (3) SO₄²⁻; (4) HCO₃⁻; (5) CO₃²⁻?
A. (1), (2), (3).
B. (2), (3), (4).
C. (3), (4), (5).
D. (2), (3), (5).
Câu 7. Hai monosaccharide liên kết nhau bởi liên kết nào sau đây?
A. Liên kết peptide.
B. Liên kết glycoside.
C. Liên kết hydrogen.
D. Liên kết phosphodiester.
Câu 8. Có bao nhiêu loại phối tử có trong phân tử phức chất cho sau đây?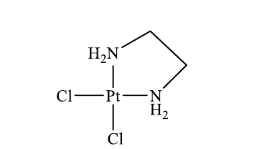 A. 1.
A. 1.
B. 2.
C. 3.
D. 4.
Câu 9. Hiện tượng phú dưỡng là một biểu hiện của môi trường ao, hồ bị ô nhiễm do dư thừa các chất dinh dưỡng. Sự dư thừa dinh dưỡng chủ yếu do hàm lượng các ion nào sau đây vượt quá mức cho phép?
A. Sodium, potassium.
B. Calcium, magnesium.
C. Nitrate, phosphate.
D. Chloride, sulfate.
Câu 10. Cho từ từ dung dịch ethylamine vào ống nghiệm đựng dung dịch nitrous acid (hoặc dung dịch hỗn hợp acid HCl + NaNO₂) ở nhiệt độ thường. Hiện tượng quan sát được trong ống nghiệm là
A. có kết tủa màu trắng.
B. có bọt khí không màu thoát ra.
C. có kết tủa màu vàng.
D. có khí màu nâu thoát ra.
Câu 11. Công thức nào sau đây có thể là công thức của chất béo?
A. C₁₅H₃₁COOCH₃.
B. (C₁₅H₃₁COO)₂C₂H₄.
C. CH₃COOCH₂C₆H₅.
D. (C₁₇H₃₅COO)₃C₃H₅.
Câu 12. Thuỷ phân saccharose, thu được hai monosaccharide X và Y. Chất X có nhiều trong quả nho chín nên còn được gọi là đường nho. Phát biểu nào sau đây đúng ?
A. Y không tan trong nước.
B. X không có phản ứng tráng bạc.
C. Y có phân tử khối bằng 342 amu.
D. X có tính chất của alcohol đa chức
Câu 13. Linalyl acetate là một trong những của tinh dầu cam và mùi thơm của hoa oải hương. Cho công thức khung phân tử của linalyl acetate như sau: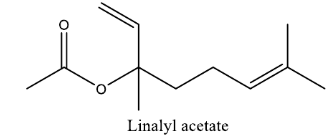 Phát biểu nào sau đây là đúng?
Phát biểu nào sau đây là đúng?
A. Linalyl acetate là ester no, đơn chức.
B. Linalyl acetate có đồng phân hình học.
C. Linalyl acetate có vùng hấp thụ trong phổ hồng ngoại (IR) ở khoảng sóng với peak đặc trưng với số sóng có giá trị từ 3650 – 3200 cm⁻¹.
D. Hydrogen hóa linalyl acetate bằng H₂(xt, t°, p) thu được ester có công thức phân tử C₁₂H₂₄O₂.
Câu 14. Phản ứng Würtz là một trong những phản ứng thuộc phương pháp làm tăng mạch carbon của các hydrocarbon thường dùng để điều chế các alkane đối xứng. Chất tham gia phản ứng Würtz là một dẫn xuất mono halogen của một hydrocarbon no và sodium. Dung môi được sử dụng là ether khan, phương trình tổng quát mô tả như sau: 2R−X+2Na⟶R−R+2NaX
Alkane (X) được nhà hóa học Edward Frankland phát hiện vào năm 1849. Nó được tìm thấy hòa tan trong dầu thô vào năm 1864 bởi Edmund Ronalds. X có trong khí dầu mỏ, khí thiên nhiên, khí chế biến dầu và được điều chế bằng cách cho ethyl bromide tác dụng với Na kim loại (phản ứng Würtz).
Cho các phát biểu sau:
(a). Alkane X có tên gọi thay thế là butane.
(b). Alkane X có 2 đồng phân dạng (n)và dạng (iso). Trong đó dạng (iso) có nhiệt độ cao hơn dạng (n).
(c). Khi cho dạng iso của X tác dụng với chlorine ở 25°C có chiếu sáng chỉ thu được một sản phẩm thế.
(d). Nếu cho tỷ lệ khả năng phản ứng tương đối của nguyên tử H bậc I và bậc III trong phản ứng chlorine ở ý (c) là 1: 5 thì phần trăm sản phẩm chính sẽ chiếm khoảng 64% (cho phép làm tròn kết quả đến hàng đơn vị).
Cho biết tỷ lệ % các sản phẩm thế phụ thuộc vào số lượng nᵢ nguyên tử H cùng một loại và khả năng phản ứng rᵢ của những nguyên tử H đó Theo công thức sau: \( \% = \dfrac{100 r \eta}{\sum r_i \eta_i} \)
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 15. Dãy gồm các kim loại phản ứng với nước ở nhiệt độ thường là
A. Na, Fe, K.
B. Na, Cr, K.
C. Be, Na, Ca.
D. Na, Ba, K.
Câu 16. Arginine là hợp chất có tác dụng giãn mạch nên được sử dụng để điều trị cho những người bị suy tim mãn tính, người có nồng độ cholesterol cao,… Công thức của arginine được cho ở hình bên dưới.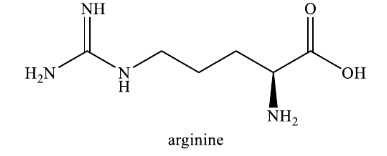 Cho các phát biểu sau:
Cho các phát biểu sau:
(a) Arginine tham gia phản ứng với dung dịch KOH theo tỉ lệ mol 1:1.
(b) Dung dịch arginine làm quỳ tím chuyển sang màu đỏ.
(c) Phần trăm khối lượng của nguyên tố N trong arginine là 40,2%.
(d) Trong một phân tử arginine có 2 liên kết π.
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 17. Cho biết: E⁰(Fe³⁺/Fe) = –0,440 V; E⁰(Cu²⁺/Cu) = +0,340 V . Sức điện động chuẩn của pin điện hoá Fe-Cu là
A. 0,920 V.
B. 1,660 V.
C. 0,100 V.
D. 0,7 V
Câu 18. Cho các phản ứng sau:
(1) X + 2Z³⁺⟶ 3X²⁺ +
(2) X²⁺ + Y⁺⟶ X³⁺ + Y
Sự sắp xếp đúng với chiều tăng dần tính oxi hoá của các cation là
A. X³⁺, Z³⁺, Y⁺.
B. X²⁺, Y⁺, X³⁺.
C. X²⁺, Z³⁺, Y⁺.
D. Y⁺, X²⁺, X³⁺.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4 . Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Cho sơ đồ (1) biểu diễn sự điện phân dung dịch CuSO₄(aq) với điện cực trơ, sơ đồ (2) biểu diễn quá trình tinh luyện đồng (Cu) bằng phương pháp điện phân. Trong sơ đồ (2), khối đồng có độ tinh khiết thấp được gắn với một điện cực của nguồn điện, thanh đồng mỏng có độ tinh khiết cao được gắn với một điện cực của nguồn điện. Dung dịch điện phân là dung dịch CuSO₄.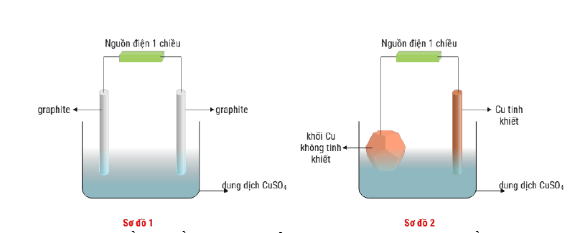 a. Khi điện phân xảy ra ở sơ đồ (2), nồng độ ion Cu²⁺ trong dung dịch sẽ giảm dần theo thời gian.
a. Khi điện phân xảy ra ở sơ đồ (2), nồng độ ion Cu²⁺ trong dung dịch sẽ giảm dần theo thời gian.
b. Khi điện phân xảy ra ở sơ đồ (1), thì ban đầu ở cực âm xảy ra quá trình khử ion Cu²⁺ và ở cực dương xảy ra quá trình oxi hóa H₂O.
c. Trong sơ đồ (1), điện cực âm được gọi là cathode và điện cực dương gọi là anode.
d. Muốn tinh luyện Cu như sơ đồ (2) thì khối Cu không tinh khiết phải được nối vào anode, còn thanh Cu tinh khiết được nối vào cathode, khi đó khối lượng Cu tan ra từ anode bằng khối lượng Cu bám vào cathode.
Câu 2. Amylose và cellulose đều là polysaccharide được kí hiệu C, D ngẫu nhiên. Cho cấu tạo của polysaccharide C và D dưới đây: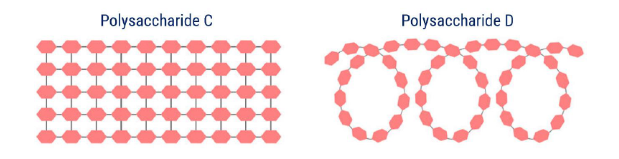 Cho các phát biểu biểu về C và D sau:
Cho các phát biểu biểu về C và D sau:
a. Polysaccharide D chứa liên kết α-1,4-glycoside.
b. Con người không thể tiêu hóa được polysaccharide C.
c. Polysaccharide D được lưu trữ trong gan và cơ.
d. Polysaccharide C bao gồm các đơn vị α-glucose.
Câu 3. Hợp chất E được điều chế từ alcohol X và carboxylic acid Y (biết Y là hợp chất tạp chức chứa vòng benzene). E có trong thành phần của một số thuốc giảm đau, xoa bóp, cao dán, … dùng để điều trị đau lưng, căng cơ, bong gân,…
Thành phần về khối lượng các nguyên tố trong E như sau: 63,16%C; 5,26%H và 31,58%O. Phân tích E bằng phổ IR của E cho kết quả sau:
+ peak đặc trưng của liên kết C = O (số sóng 1750-1735 cm⁻¹),
+ liên kết C – O (số sóng 1300 –1000cm⁻¹)
+ peak đặc trưng của liên kết O – H (số sóng 3650 – 3200cm⁻¹).
Từ phổ MS , xác định được E có phân tử khối là 152 amu .
Cho các phát biểu sau:
a. X là methyl alcohol.
b. Tổng số nguyên tử trong phân tử E là 20 .
c. Y có nhóm -OH và -COOH.
d. Nếu lấy 1 mol Y tác dụng NaOH thì số mol NaOH cần để phản ứng vừa đủ là 2 mol.
Câu 4. Cho các quá trình tạo phức chất sắt diễn sau:
Fe³⁺(aq) + 6H₂O(l) ⇌ [Fe(OH₂)₆]³⁺(aq) (I)
[Fe(OH₂)₆]³⁺(aq) + SCN⁻ (aq) ⇌ [Fe(OH₂₎₅(SCN)]²⁺(aq) + H₂O(l) Kc = 1,4.10² (II)
[Fe(OH₂)₆]³⁺(aq) + F⁻ (l) ⇌ [Fe(OH₂)₅F]²⁺(aq) + H₂O(l) Kc = 2,0.10⁵ (III)
Biết dung dịch [Fe(OH₂)₆]³⁺ có màu vàng nâu, dung dịch [Fe(OH₂)₅(SCN)]²⁺ có màu đỏ, dung dịch [Fe(OH₂)₅F]²⁺ và các anion SCN⁻, F⁻ đều không có màu.
Cho các phát biểu sau:
a. Quá trình (I) xảy ra khi hoà tan iron(III) chloride trong nước. Kết thúc quá trình này thu được dung dịch có chứa lượng lớn cation Fe³⁺và phức chất aqua [Fe(OH₂)₆]³⁺.
b. So với anion F⁻, anion SCN⁻ dễ thay thế phối tử H₂O trong [Fe(OH₂)₆]³⁺ hơn.
c. Khi cho từ từ dung dịch KSCN vào dung dịch ở quá trình (III) thì dung dịch này sẽ có màu.
d. Trong các quá trình (I), (II) và (III), mỗi phân tử H₂O hoặc anion SCN⁻ hay anion F⁻ đều sử dụng số cặp electron hoá trị riêng như nhau để cho vào orbital trống của cation Fe³⁺.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6 .
Câu 1. Một sinh viên thực hiện điện phân theo sơ đồ như hình bên.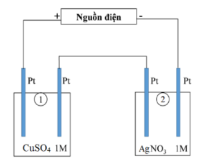
Bình (1) chứa 100 ml dung dịch CuSO₄ 1M.
Bình (2) chứa 100 ml dung dịch AgNO₃ 1M.
Sau thời gian t giây, sinh viên quan sát thấy ở cathode bình (2) bắt đầu xuất hiện khí. Biết trong hệ điện phân nối tiếp, số điện tử truyền dẫn trong các bình là như nhau. Nguyên tử khối của Cu và Ag lần lượt là 64 và 108 đvC.
Coi như nhiệt độ ở 2 bình là không thay đổi và bỏ qua các quá trình phụ.
Tính số gam Cu bám lên điện cực trong bình (1) tại thời điểm t giây.
Câu 2. Trong công nghiệp cellulose triacetate và cellulose diacetat được dùng hỗn hợp hoặc riêng rẽ để sản xuất phim ảnh và tơ acetat. Hòa tan hai ester trên trong hỗn hợp acetone và ethanol rồi bơm dung dịch thu được qua những lỗ nhỏ thành chùm tia đồng thời thổi không khí nóng (55 – 70 °C) qua chùm tia đó để làm bay hơi acetone sẽ thu được những sợi mảnh khảnh gọi là tơ acetate. Tơ acetate có tính đàn hồi, bền bỉ và đẹp. Vải Acetate cũng được dùng để tạo nhiều sản phẩm khác như là khăn trải giường, rèm cửa, áo phu xe ho…
Cho cellulose phản ứng với anhydride acetic (CH₃CO)₂O với H₂SO₄ đặc thu được 6,6 gam acetic acid và 11,1 gam hỗn hợp X gồm cellulose triacetate và cellulose diacetate.
Tính % khối lượng cellulose triacetate trong hỗn hợp. (làm tròn đáp án đến hàng phần mười)
Câu 3. Cho các chất: cellulose (1), saccharose (2), aniline (3), tristearin (4), alanine (5). Có bao nhiêu chất bị thủy phân trong môi trường acid ở điều kiện thích hợp?
Câu 4. Thực hiện đo pH của dung dịch methylamine cho kết quả như sau: Cho phương trình sau: CH₃NH₂ + H₂O ⇌ CH₃NH₃⁺ + OH⁻ Kb
Cho phương trình sau: CH₃NH₂ + H₂O ⇌ CH₃NH₃⁺ + OH⁻ Kb
Với hằng số base Kb tính theo CT sau: Kb = ([CH₃NH₃⁺][OH⁻] / [CH₃NH₂]) , bỏ qua sự điện li của nước . Hãy tính giá trị của x (làm tròn đến hàng phần trăm)
Câu 5. Nescafe đã sản xuất thành công lon coffee tự làm nóng. Để làm nóng coffee, chỉ cần ấn nút (trên lon) để trộn nguyên liệu gồm dung dịch KOH hoặc NaOH rất loãng và CaO; 210 mL coffee trong lon sẽ được hâm nóng đến khoảng 40 °C. Giả sử nhiệt dung riêng của coffee là 4,18 J/g.K (Nhiệt dung riêng là nhiệt lượng cần cung cấp để 1 gam chất tăng lên 1 °C). Cho ΔfH⁰₂₉₈ (kJ.mol⁻¹) của CaO, H₂O(l), Ca(OH)₂ lần lượt là -635; -286; -985; các giá trị này không đổi trong khoảng nhiệt độ đang xét. Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%.
Tính khối lượng CaO cần cung cấp để làm nóng 210 mL coffee từ 10 °C đến 40 °C (d = 1,0 g/ml). (làm tròn đến phần nguyên).
Câu 6. Cyanide (CN⁻) là một loại chất độc hại được tìm thấy trong nước thải của các công ty khai thác quặng kim loại. Cyanide có khả năng tạo phức mạnh với kim loại, các công ty khai thác mỏ đã kiếm được lợi nhuận khổng lồ từ việc sử dụng cyanide để chiết xuất Au từ quặng của nó.
Hàm lượng ion cyanide có thể xác định bằng phương pháp chuẩn độ Liebig: dùng dung dịch AgNO₃ 0,1 M làm chất chuẩn.
Phương trình chuẩn độ: 2 CN⁻ + Ag⁺ ⇌ Ag(CN)₂⁻
Tại điểm tương đương: Ag(CN)₂⁻ + Ag⁺ ⇌ Ag[Ag(CN)₂]
Thực hiện xác định độ tinh khiết của 0,4723 gam mẫu KCN với dung dịch AgNO₃ 0,1 M. Chuẩn độ 3 lần thì cho kết quả như sau:
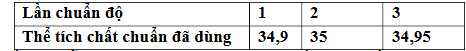 Xác định độ tinh khiết của mẫu KCN trên. (làm trong đáp án đến hàng phần mười)
Xác định độ tinh khiết của mẫu KCN trên. (làm trong đáp án đến hàng phần mười)
Mục đích tổ chức kỳ thi Tốt nghiệp THPT năm 2025 là gì?
Căn cứ theo các văn bản chỉ đạo và hướng dẫn của Bộ Giáo dục và Đào tạo, kỳ thi Tốt nghiệp THPT năm 2025 được tổ chức nhằm những mục tiêu chính sau:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo chương trình giáo dục phổ thông mới.
– Dùng kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh cho các cơ sở giáo dục đại học, cao đẳng.
– Góp phần phản ánh chất lượng giáo dục ở từng địa phương cũng như toàn quốc, từ đó làm cơ sở để điều chỉnh nội dung và phương pháp dạy học trong các nhà trường.
Thí sinh thi tốt nghiệp THPT năm 2025 có bắt buộc phải thi môn Hóa học không?
Theo quy định hiện hành của Bộ Giáo dục và Đào tạo, thí sinh dự thi Tốt nghiệp THPT năm 2025 bắt buộc phải tham gia 3 bài thi chính: Toán, Ngữ văn và Ngoại ngữ.
Ngoài ra, thí sinh lựa chọn thêm một trong hai bài thi tổ hợp sau:
– Tổ hợp Khoa học Tự nhiên (KHTN): gồm các môn Vật lí, Hóa học, Sinh học.
– Tổ hợp Khoa học Xã hội (KHXH): gồm các môn Lịch sử, Địa lí, Giáo dục công dân (dành cho học sinh học chương trình GDPT hiện hành).
Nếu thí sinh chọn bài thi tổ hợp KHTN thì môn Hóa học sẽ là một trong ba môn thành phần của bài thi. Do đó, thí sinh không bắt buộc phải thi môn Hóa, trừ khi chọn tổ hợp KHTN để xét tốt nghiệp hoặc sử dụng kết quả môn Hóa học để xét tuyển vào các ngành học có yêu cầu.
Vì vậy, Đề thi thử tốt nghiệp THPT 2025 môn Hóa học – Đề 1 là tài liệu luyện tập cần thiết dành cho học sinh lựa chọn tổ hợp KHTN. Đề thi giúp các em làm quen với cấu trúc đề thi chính thức, rèn luyện kỹ năng giải bài và đánh giá đúng năng lực hiện tại để có sự chuẩn bị vững vàng cho kỳ thi sắp tới.




