Đề thi thử Đại học 2019 lần 1 môn Hóa học Bộ GD&ĐT là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Đề thi thử lần 1 năm 2019 vẫn giữ nguyên hình thức trắc nghiệm khách quan với 40 câu, thời gian làm bài 50 phút. Cấu trúc đề thi được xây dựng khoa học, có tính phân hóa tốt với tỷ lệ cân bằng giữa các mức độ: nhận biết – thông hiểu – vận dụng – vận dụng cao. Đây là cơ hội để học sinh đánh giá đúng năng lực bản thân và điều chỉnh chiến lược ôn luyện phù hợp.
Các kiến thức cần biết để giải đề trải đều toàn bộ chương trình lớp 12, bao gồm: este – lipit, amin – amino axit – peptit – protein, polime, phản ứng oxi hóa – khử, bài toán điện phân, nhận biết chất, kim loại tác dụng với axit – muối, cùng với một số câu hỏi nâng cao vận dụng kiến thức lớp 11 (như phản ứng trao đổi ion, tính chất oxi hóa – khử).
Các trọng tâm cần nắm để làm tốt đề thi là kỹ năng xử lý nhanh và chính xác các bài toán hóa học thông qua các phương pháp: bảo toàn khối lượng, bảo toàn nguyên tố, bảo toàn electron, quy đổi, phương pháp đường chéo và trung bình. Ngoài ra, khả năng phân tích số liệu và chọn đáp án đúng trong thời gian ngắn là yếu tố then chốt để đạt điểm cao.
Hãy cùng Dethitracnghiem.vn cùng tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 4 trang
- Hình thức: 100% trắc nghiệm
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2019




Câu 41: Ở điều kiện thường, kim loại nào sau đây phản ứng với bột lưu huỳnh?
A. Fe.
B. Hg.
C. Cr.
D. Cu.
Câu 42: Dung dịch chứa Ala-Gly-Ala không phản ứng được với dung dịch nào sau đây ?
A. HCl.
B. Mg(NO3)2.
C. KOH.
D. NaOH.
Câu 43: Kim loại nào sau đây là kim loại kiềm thổ ?
A. Na.
B. Ca.
C. Al.
D. Fe.
Câu 44: Poli(vinyl clorua) (PVC) là chất cách điện tốt, được dùng làm vật liệu cách điện, ống dẫn nước,… Monome được dùng để điều chế PVC là
A. CF2=CF2.
B. CH2=CH-Cl.
C. CH2=CHCl.
D. CH2=CCl2.
Câu 45: Trong công nghiệp đường, chất khí X được dùng để tẩy màu cho dung dịch nước đường trong quy trình sản xuất saccarozo. X là
A. CO2.
B. CO.
C. SO2.
D. Cl2.
Câu 46: Etyl isovalerat là este có mùi thơm của táo. Công thức cấu tạo thu gọn của etyl isovalerat là
A. CH3CH2CH2COOC2H5.
B. (CH3)2CHCOOC2H5.
C. (CH3)3CCOOCH3.
D. C2H5COOCH2CH(CH3)2.
Câu 47: Nhỏ dung dịch NaOH loãng vào bình đựng dung dịch chất X, thu được kết tủa màu xanh nhạt, khi thêm tiếp dung dịch NaOH vào bình, thấy kết tủa tan dần tạo thành dung dịch màu lục nhạt. X là
A. CrCl3.
B. AlCl3.
C. CuCl2.
D. ZnCl2.
Câu 48: Đốt cháy hoàn toàn amin X no, đơn chức, mạch hở, thu được 8,96 lít CO2 (đktc) và 0,1 mol N2. Công thức phân tử của X là
A. C3H9N.
B. C4H11N.
C. C3H7N.
D. C4H9N.
Câu 49: Kim loại nhôm không tan được trong dung dịch nào sau đây?
A. NaOH.
B. H2SO4 đặc nguội.
C. HCl.
D. Ba(OH)2.
Câu 50: Chất nào sau đây thuộc loại đisaccarit ?
A. Saccarozơ.
B. Xenlulozơ.
C. Tinh bột.
D. Glucozơ.
Câu 51: Oxit nào sau đây phản ứng với nước ở điều kiện thường?
A. Fe2O3.
B. CrO3.
C. SiO2.
D. N2O5.
Câu 52: Cho các chất sau: đimetylamin, axit glutamic, phenyl amoni clorua, natri axetat. Số chất phản ứng được với dung dịch HCl là
A. 3.
B. 4.
C. 2.
D. 1.
Câu 53: Kim loại nào sau đây có thể điều chế được bằng phương pháp nhiệt luyện?
A. Na.
B. Al.
C. Ca.
D. Fe.
Câu 54: Trong các chất sau, chất nào là chất rắn, không màu, dễ tan trong nước, kết tinh ở điều kiện thường?
A. C6H5NH2.
B. H2NCH2COOH.
C. Mg(OH)2.
D. (C6H10O5)n.
Câu 55. X và Y là hai kim loại phản ứng được với dung dịch HCl nhưng không tác dụng được với dung dịch Fe(NO3)2. X, Y là
A. Mg, Zn
B. Mg, Fe
C. Fe, Cu
D. Fe, Ni.
Câu 56: Chất nào sau đây có chất béo, chất nào có trạng thái thể khí ở các điều kiện thường ?
A. Amyl axetat
B. Alanin
C. axit glutamic
D. Valin
Câu 57: Thạch cao nung được dùng để bó bột, đúc tượng do có hiện tượng giãn nở thể tích khi đông cứng. Công thức phân chính của thạch cao nung chứa
A. CaSO4
B. CaSO4.½H2O.
C. CaSO4.H2O.
D. Ca(HCO3)2.
Câu 58: Chất hữu cơ X mạch hở, có công thức phân tử C4H10O. Khi X đun với dung dịch KOH thu được muối Y, biết MY < MX. Số công thức cấu tạo của X là
A. 5.
B. 3.
C. 4.
D. 6.
Câu 59: Cho 16,8 gam Fe vào 200 ml dung dịch CuSO4 0,75M. Sau một thời gian, lấy thanh sắt ra cân nặng 17,6 gam. Khối lượng đồng bám trên thanh sắt là
A. 19,2.
B. 6,4.
C. 0,8.
D. 9,6.
Câu 60: Lên men m gam glucozơ (hiệu suất 75%), thành ancol etylic và khí CO2. Dẫn toàn bộ lượng CO2 này vào bình nước vôi trong với lượng thấy tách ra 40 gam kết tủa và dung dịch X. Thêm từ từ dung dịch NaOH vào dung dịch X đến khi lượng kết tủa tối đa thì dừng lại và sử dụng hết 0,04 mol dung dịch NaOH. Giá trị của m là
A. 45,0.
B. 52,8.
C. 57,6.
D. 43,2.
Câu 61: X là dung dịch HCl nồng độ x(M). Y là dung dịch Na2CO3 nồng độ y(M). Nhỏ từ từ 100 ml dung dịch X vào 100 ml dung dịch Y, thu được V1 lít CO2 (đktc). Nhỏ từ từ 100 ml dung dịch Y vào 100 ml dung dịch X, thu được V2 lít CO2 (đktc), biết tỉ lệ V1:V2 = 3:5. Tỉ lệ x:y là
A. 5:3
B. 10:7
C. 7:5
D. 7:3
Câu 62: Hai chất P, Q có công thức phân tử lần lượt C3H9N2O3 và C3H9NO3. Khi cho P, Q phản ứng với dung dịch HCl cùng tạo ra khí Z; còn với dung dịch NaOH cùng cho khí Y. Nhận xét nào sau đây đúng
A. MY < MZ.
B. Khí Z làm xanh giấy quỳ ẩm.
C. MY > MZ.
D. Khí Y làm đỏ giấy quỳ tím ẩm.
Câu 63: Cho một lượng hợp kim Ba-Na vào 200 gam dung dịch X gồm HCl 0,1M và CuCl2 0,1M. Kết thúc các phản ứng, thu được 0,448 lít khí (đktc) và m gam kết tủa. Giá trị của m là
A. 1,28
B. 0,64
C. 0,98
D. 1,96
Câu 64. Đốt cháy hoàn toàn V lít hỗn hợp X gồm H2, CH4, C2H6, C3H6, C4H10 thu được 7,84 lít khí CO2 và 9,36 gam nước, các khí đều đo ở đktc. Giá trị của V là
A. 3,36
B. 4,48
C. 5,6
D. 6,72
Câu 65. Thực hiện các thí nghiệm sau ở nhiệt độ thường
(1) Cho bột Al vào dung dịch NaOH.
(2) Cho bột Fe vào dung dịch AgNO3.
(3) Cho CaO vào dung dịch CH3COOH.
(4) Cho dung dịch Na2CO3 vào dung dịch AlCl3.
Số thí nghiệm có xảy ra phản ứng là
A. 4
B. 2
C. 3
D. 1
Câu 66: Cho 10 ml dung dịch C6H5NH2 46o vào bình đựng Na dư, sau khi phản ứng xong thu được V lít khí H2 (đktc), biết khối lượng riêng của ancol etylic và nước lần lượt là 0,8 g/ml và 1,0 g/ml. Giá trị của V là
A. 0,896
B. 3,36
C. 1,95
D. 4,256
Câu 67: Cho các chất rắn sau: Cr2O3, Fe3(NO3)2, Al(OH)3, Mg. Số chất tan được trong dung dịch HCl loãng nguội (dư) là
A. 1.
B. 3.
C. 2.
D. 4.
Câu 68: X là axit đơn chức, mạch hở; Y là ancol đơn chức, mạch hở. Đun hỗn hợp X, Y với H2SO4 đặc thu được este Z. Biết trong Z có chứa 54,54% khối lượng cacbon. Số cặp chất phù hợp với X, Y là
A. 4.
B. 2.
C. 3.
D. 1.
Câu 69: Cho V lít đktc hỗn hợp khí gồm CO và H2 phản ứng với một lượng dư hỗn hợp rắn gồm CuO và Fe2O3 nung nóng. Sau các phản ứng xảy ra hoàn toàn, khối lượng hỗn hợp rắn giảm 0,32 gam. Giá trị V là
A. 0,224
B. 0,448
C. 0,112
D. 0,560.
Câu 70: Hợp chất hữu cơ A có công thức phân tử C5H8O4 thỏa mãn các phương trình hóa học sau: 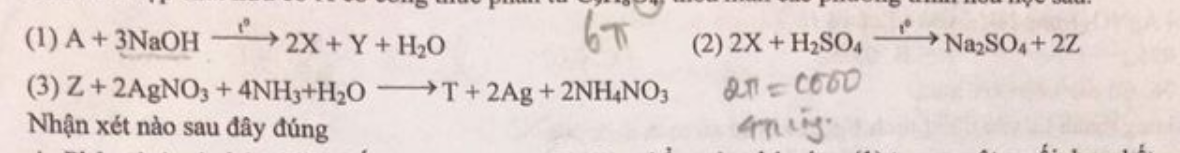
A. Phân tử A có chứa 4 liên kết π.
B. Sản phẩm của phản ứng (1) tạo ra một muối duy nhất.
C. Phân tử của Y có 7 nguyên tử cacbon.
D. Phân tử Y có chứa 3 nguyên tử oxi
Câu 71: Hỗn hợp X gồm ba triglixerit được tạo bởi axit oleic và axit linoleic (có tỉ lệ mol tương ứng của hai axit là 2:1). Đốt cháy hoàn toàn a gam X thu được 37,752 gam CO2 và 13,77 gam nước. Mặt khác, hiđro hóa hoàn toàn a gam X thu được chất hữu cơ Y. Đun Y với dung dịch KOH (vừa đủ) thu được glixerol và m gam muối. Giá trị của m là
A. 3,77.
B. 13,65.
C. 13,23.
D. 13,25.
Câu 72. Mô hình thí nghiệm dùng để điều chế chất khí Z: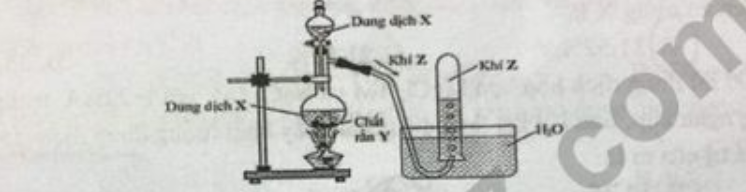
Phương trình hóa học nào sau đây phù hợp với mô hình trên ?
A. CaC2 + 2H2O → Ca(OH)2 + C2H2↑.
B. Al4C3 + 12HCl → 4AlCl3 + 3CH4↑.
C. H2SO4 đặc + NaCl rắn → SO2↑ + Na2SO4 + H2O.
D. CH3COONarắn + NaOH rắn → CH4↑ + Na2CO3.
Câu 73: Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau: Mẫu thử Thuốc thử Hiện tượng
 Dung dịch X, Y, Z, T lần lượt là
Dung dịch X, Y, Z, T lần lượt là
A. Hồ tinh bột, lòng trắng trứng, phenyl amoni clorua, fructozo.
B. Lòng trắng trứng, phenyl amoni clorua, hồ tinh bột, fructozo.
C. Hồ tinh bột, lòng trắng trứng, fructozo, phenyl amoni clorua.
D. Hồ tinh bột, fructozo, lòng trắng trứng, phenyl amoni clorua.
Câu 74: Cho m gam hỗn hợp Al và BaO vào nước thu được dung dịch X và V lít khí H2 (đktc). Khi nhỏ từ từ dung dịch HCl vào dung dịch X, kết quả thí nghiệm được biểu diễn trên đồ thị sau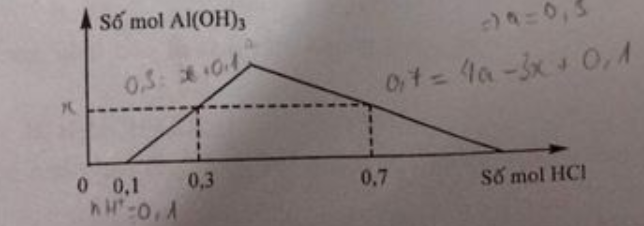 Giá trị của m là
Giá trị của m là
A. 61,2
B. 38,25
C. 38,7
D. 45,9.
Câu 75: Đốt cháy hoàn toàn m gam anđehit đơn chức mạch hở X (phân tử chứa không quá 4 nguyên tử cacbon), thu được 6,72 lít CO2 (đktc) và 1,8 gam nước. Mặt khác, khi cho 1,7 gam X phản ứng tối đa với a mol AgNO3 trong NH3. Giá trị của a là
A. 0,025.
B. 0,05.
C. 0,075.
D. 0,1.
Câu 76. Có các nhận xét sau:
(1) Nhúng thanh Fe vào dung dịch FeCl3 xảy ra ăn mòn điện hóa.
(2) Sục khí H2S vào dung dịch CuSO4, thấy xuất hiện kết tủa xanh nhạt.
(3) Nhỏ dung dịch Na2CO3 vào dung dịch FeCl3 thấy có kết tủa đỏ nâu và thoát khí.
(4) Nhúng thanh nhôm vào dung dịch NaOH loãng nguội, thấy thanh nhôm tan dần.
(5) Đốt dây sắt trong khí clo thấy hình thành muối sắt (II) clorua bám trên thanh sắt.
Số nhận xét đúng là
A. 1
B. 2
C. 3
D. 4.
Câu 77: Hỗn hợp X gồm metyl acrylat, vinyl axetat, buta-1,3-đien và vinyl axetilen. Để đốt cháy hoàn toàn 0,5 mol hỗn hợp X cần dùng 54,88 lít O2 (đktc) thu được khí CO2 và 23,4 gam H2O. Phần trăm khối lượng của vinyl axetilen có trong X là
A. 30,50%.
B. 31,52%.
C. 21,55%.
D. 33,35%.
Câu 78: Điện phân 200 ml dung dịch hỗn hợp MgCl2 1M và NaCl 1M, với I=2,68A, trong thời gian 3 giờ với điện cực trơ, màng ngăn xốp. Sau khi kết thúc điện phân thấy khối lượng dung dịch giảm m gam so với dung dịch ban đầu. Giá trị của m là
A. 10,65
B. 14,25
C. 19,65
D. 22,45
Câu 79. Hỗn hợp X gồm alanin và đipeptit (Gly-Val). Cho m gam X vào 100 ml dung dịch hỗn hợp H2SO4 0,25M và HCl 0,25M, thu được dung dịch Y. Cho toàn bộ Y phản ứng vừa đủ với 240 ml dung dịch gồm NaOH 0,3M và KOH 0,2M đun nóng, thu được dung dịch chứa 10,9155 gam muối trung hòa. Phần trăm khối lượng của alanin trong X là
A. 43,88%.
B. 56,12%.
C. 16,98.
D. 76,72.
Câu 80. Hòa tan hết 8,976 gam hỗn hợp X gồm FeS2, FeS, Cu2S và Cu trong 864 ml dung dịch HNO3 1M đun nóng, sau khi kết thúc các phản ứng thu được dung dịch Y và 0,186 mol một chất khí thoát ra. Cho Y tác dụng với lượng dư dung dịch BaCl2 thu được 11,184 gam kết tủa. Mặt khác, dung dịch Y phản ứng tối đa với m gam Fe, biết trong các quá trình trên, sản phẩm khử duy nhất của NO3– là NO. Giá trị của m là
A. 16,464.
B. 8,4.
C. 17,304.
D. 12,936.
Mục đích tổ chức kỳ thi THPT quốc gia năm 2019 là gì?
Căn cứ theo Quy chế thi THPT quốc gia và xét công nhận tốt nghiệp trung học phổ thông được ban hành kèm theo Thông tư số 04/2017/TT-BGDĐT và được sửa đổi, bổ sung tại Thông tư số 03/2019/TT-BGDĐT, mục đích tổ chức kỳ thi THPT quốc gia năm 2019 là:
– Đánh giá kết quả học tập của học sinh theo chuẩn kiến thức, kỹ năng của chương trình giáo dục phổ thông.
– Làm căn cứ để xét công nhận tốt nghiệp trung học phổ thông (THPT).
– Cung cấp dữ liệu tin cậy để các cơ sở giáo dục đại học, giáo dục nghề nghiệp sử dụng trong tuyển sinh theo tinh thần tự chủ.
– Góp phần đánh giá chất lượng giáo dục của các cơ sở giáo dục và công tác quản lý giáo dục của địa phương và toàn ngành.
Thí sinh thi THPT quốc gia năm 2019 có bắt buộc thi môn Hóa học không?
Căn cứ theo Quy chế thi THPT quốc gia năm 2019, Bộ Giáo dục và Đào tạo quy định:
Thí sinh dự thi 04 bài thi, gồm:
02 bài thi bắt buộc: Toán và Ngữ văn.
– 01 bài thi Ngoại ngữ: thí sinh chọn một trong các thứ tiếng (Anh, Nga, Pháp, Trung Quốc, Đức, Nhật).
– 01 bài thi tổ hợp tự chọn, trong đó có 2 lựa chọn:
+ Bài thi Khoa học Tự nhiên (KHTN): gồm 03 môn thành phần là Vật lí, Hóa học, Sinh học.
+ Bài thi Khoa học Xã hội (KHXH): gồm các môn Lịch sử, Địa lí, Giáo dục công dân (đối với thí sinh học chương trình THPT); hoặc Lịch sử, Địa lí (đối với thí sinh học chương trình GDTX).
Thí sinh chỉ phải chọn một bài thi tổ hợp duy nhất (KHTN hoặc KHXH) để xét tốt nghiệp, nhưng có thể thi cả hai bài nếu có nguyện vọng dùng kết quả để xét tuyển đại học, cao đẳng.
Như vậy, kỳ thi THPT quốc gia năm 2019 không bắt buộc thí sinh phải thi môn Hóa học.
Việc thí sinh có thi môn Hóa học hay không phụ thuộc vào lựa chọn bài thi tổ hợp. Nếu chọn bài thi Khoa học Tự nhiên thì Hóa học là một trong ba môn thành phần bắt buộc trong bài thi này. Nếu chọn bài thi Khoa học Xã hội thì thí sinh không cần thi môn Hóa học.




