Đề thi thử Đại học 2025 lần 1 môn Hóa học Bộ GD&ĐT là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Trong xu hướng đổi mới giáo dục hiện nay, đề thi thử lần 1 năm 2025 tiếp tục duy trì 40 câu hỏi trắc nghiệm trong 50 phút, nhưng có sự điều chỉnh về mặt nội dung và tư duy ra đề: tăng tỷ lệ câu hỏi gắn với thực tiễn, nâng cao mức độ tích hợp liên môn và đánh giá năng lực toàn diện. Câu hỏi được thiết kế bám sát chuẩn kiến thức – kỹ năng của chương trình lớp 12, đồng thời lồng ghép một số nội dung trọng tâm từ lớp 11.
Các kiến thức cần biết để giải đề gồm: tính chất hóa học và ứng dụng của este – lipit – amin – amino axit – peptit – polime, phản ứng oxi hóa – khử, điện phân, bài toán hỗn hợp kim loại – muối – dung dịch axit, bazơ, câu hỏi nhận biết chất và biến hóa vô cơ – hữu cơ, cùng một số câu hỏi mang tính ứng dụng thực tiễn trong đời sống và công nghiệp.
Các trọng tâm cần nắm là: vận dụng thành thạo các phương pháp giải nhanh như bảo toàn khối lượng, bảo toàn nguyên tố, bảo toàn electron, phương pháp quy đổi, trung bình, đường chéo, đồng thời rèn luyện kỹ năng đọc hiểu tình huống, phân tích dữ kiện bảng – biểu đồ – sơ đồ phản ứng, là xu hướng quan trọng trong đề thi năm 2025.
Hãy cùng Dethitracnghiem.vn cùng tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 4 trang
- Hình thức: 100% trắc nghiệm
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025




Câu 1: Glucose là một trong hai dạng monosaccharide phổ biến trong đời sống. Dưới đây là các dạng cấu tạo thường gặp của glucose: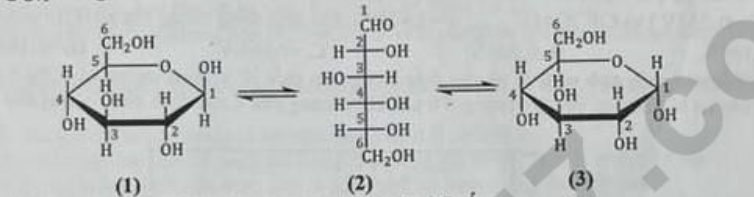 Ở dạng mạch vòng, nhóm –OH hemiacetal của glucose ở vị trí C số…
Ở dạng mạch vòng, nhóm –OH hemiacetal của glucose ở vị trí C số…
A. 2.
B. 3.
C. 1.
D. 6.
Câu 2: Tinh bột là sản phẩm quang hợp của cây xanh và được dự trữ trong các loại hạt, củ, quả… Trong các loại nông sản: hạt gạo, hạt lúa mạch, củ khoai lang, củ sắn, loại nào có chứa hàm lượng tinh bột cao nhất?
A. Củ sắn.
B. Củ khoai lang.
C. Hạt lúa mạch.
D. Hạt gạo.
Câu 3: Đình sắt bị ăn mòn điện hóa học khi gắn với kim loại nào sau đây trong môi trường chất điện ly?
A. Mg.
B. Al.
C. Cu.
D. Zn.
Câu 4: Loại polymer nào sau đây dễ bị thuỷ phân trong môi trường kiềm?
A. Cao su buna.
B. Polystyrene.
C. Nylon-6,6.
D. Polyethylene.
Câu 5: Chất béo là
A. trieste của glycerol với acid béo.
B. diester của acid hữu cơ và glycerol.
C. hợp chất hữu cơ chứa C, H, N, O.
D. ester của acid béo và alcohol đa chức.
Câu 6: Một tripeptide X được cấu thành từ 1 phân tử Ala và 2 phân tử Gly. Công thức cấu tạo của X có thể là
A. Ala-Ala-Gly.
B. Ala-Gly-Ala.
C. Gly-Ala-Gly.
D. Gly-Ala-Ala.
Câu 7: Ester E được tạo thành từ phản ứng ester hoá giữa CH3COOH và CH3OH có công thức nào sau đây?
A. C3H7COOCH3.
B. CH3COOCH3.
C. CH3COOC2H5.
D. CH3COOC2H5.
Câu 8: Thí nghiệm nào sau đây không xảy ra phản ứng?
A. Cho kim loại Cu vào dung dịch HNO3.
B. Cho kim loại Ag vào dung dịch HCl.
C. Cho kim loại Zn vào dung dịch CuSO4.
D. Cho kim loại Cu vào dung dịch FeCl2(SO4)3.
Câu 9: Để sản xuất được 1 triếc chiếu chạc gang có hàm lượng Fe là 95% thì cần dùng tối thiểu x tấn quặng magnetite chứa 80% Fe3O4. Biết rằng mỗi chiếc chiếu nặng 3,0 kg và lượng Fe bị hao hụt trong quá trình là 20%. Giá trị của x là bao nhiêu? (làm tròn kết quả đến hàng đơn vị)
A. 4373.
B. 6150.
C. 6473.
D. 4919.
Câu 10: Cho những phát biểu về chất sodium hydrogencarbonate sau đây: Số phát biểu đúng là:
Số phát biểu đúng là:
A. 4.
B. 3.
C. 1.
D. 2.
Câu 11: Ở dãy điện thế theo chiều tăng dần của bảng nhôm aluminium (Al) là do Al
A. Là kim loại dẫn điện tốt nhất.
B. Thường có nhiều hợp chất.
C. Là kim loại dẫn điện tốt và nhẹ.
D. Có tính trơ về mặt hoá học.
Câu 12: Ki hiệu cặp oxi hoá – khử ứng với quá trình khử: Fe3+ + 2e → Fe là
A. Fe2+/Fe.
B. Fe3+/Fe2+.
C. Fe3+/Fe.
D. Fe3+/Fe2+.
Câu 13: LDPE là một chất dẻo dễ tạo màng, có tính dai bền nên được sử dụng làm túi nylon, màng bọc, bao gói thực phẩm. Trên các bao bì làm từ LDPE thường được in kí hiệu như hình dưới đây : LDPE được tổng hợp từ monomer nào sau đây?
LDPE được tổng hợp từ monomer nào sau đây?
A. CH2=CH2.
B. CH2=CH-CH3.
C. C3H6CH=CH2.
D. CH2=CHCl.
Câu 14: Thiết lập pin điện hóa ở điều kiện chuẩn gồm hai điện cực tạo bởi các cặp oxi hóa – khử Ni2+/Ni (EoNi2+/Ni = -0,257V) và Cd2+/Cd (EoCd2+/Cd = -0,403V). Sức điện động chuẩn của pin điện hóa trên là:
A. -0,146 V.
B. 0,000 V.
C. +0,660 V.
D. +0,146 V.
Câu 15: Kết quả phân tích nguyên tố cho thấy trong hợp chất X: carbon chiếm 61,02%; hydrogen chiếm 15,25%; còn lại là nitrogen về khối lượng. Tỉ phổ khối lượng của X xác định được giá trị m/z của peak [M+] bằng 59.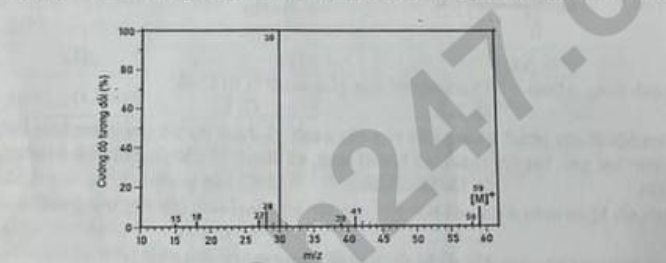 Công thức phân tử của X là
Công thức phân tử của X là
A. C4H11N.
B. C3H9N2.
C. C3H9N.
D. C3H7N.
Câu 16: Phương pháp nào sau đây có thể tách được sodium kim loại?
A. Điện phân nước muối.
B. Điện phân muối sodium chloride nóng chảy.
C. Nung nóng mạnh quặng sodium trong không khí.
D. Nung nóng quặng sodium với carbon.
Câu 17: Chuẩn độ dung dịch NaOH chưa biết chính xác nồng độ (biết nồng độ trong khoảng gần với 0,1 M) bằng dung dịch chuẩn HCl 0,1 M với chỉ thị phenolphtalein. Hãy sắp xếp các bước tiến hành theo đúng thứ tự: A. (1), (2), (3), (4), (5).
A. (1), (2), (3), (4), (5).
B. (5), (2), (3), (4), (1).
C. (5), (3), (2), (1), (4).
D. (1), (3), (2), (5), (4).
Câu 18: Khi tham gia phản ứng hóa học, mỗi nguyên tử kim loại nhóm IIA đều thể hiện khuynh hướng
A. Nhường 2 electron.
B. Nhận 1 electron.
C. Nhận 2 electron.
D. Nhường 1 electron.
PHẦN II. CÂU TRẮC NGHIỆM ĐÚNG SAI. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19: Mẫu thiếc nguyên dạng đĩa tròn mỏng có đường kính 5,00 cm được mạ với lớp phủ gold (Au) dày 0,02 mm từ dung dịch Au3+.
Cho biết :
Khối lượng riêng của Au = DAu = 19,3 g/cm3.
F = 96500 C/mol ; 1e = 0,10 A ; π = 3,14.
Khối lượng mol nguyên tử Au = 197 gam/mol
a) Thời gian điện phân 9.000.000 đồng (1 chỉ Au = 37,5 gam Au nguyên chất). ĐÚNG
b) Trong quá trình mạ khuấyện tại được dùng là anode. SAI
c) Khối lượng Au cần mạ cho một chiếc khuyên tai là 1,52 g (làm tròn đến hàng phần trăm). ĐÚNG
d) Chi phí mua Au cho mỗi chiếc khuyên tai là 3.636.120 đồng (làm tròn đến hàng đơn vị). ĐÚNG
Câu 20: Cho các hợp chất hữu cơ CH3COOH, HCOOCH3, C2H5OH.
a) Có các cặp chất là đồng phân của nhau ở điều kiện thường. SAI
b) Ở điều kiện thường, các chất trên đều tác dụng với dung dịch NaOH. ĐÚNG
c) Nhiệt độ sôi tăng dần theo thứ tự: HCOOCH3, C2H5OH, CH3COOH. ĐÚNG
d) Nhiệt độ sôi của CH3COOH cao hơn HCOOCH3 do giữa các phân tử CH3COOH tạo được liên kết hydrogen. ĐÚNG
Câu 21: Ở nước ta, nước mắm truyền thống được sản xuất thủ công từ cá cơm theo các giai đoạn chính như sau:
Giai đoạn 1: rửa sạch cá cơm rồi trộn cá với muối ăn theo tỉ lệ nhất định.
Giai đoạn 2: ủ hỗn hợp (cá cơm và muối ăn) trong các thùng gỗ, chum, sành từ 6 đến 24 tháng
Giai đoạn 3: thu được nước cốt của mắm (gọi là mắm nhỉ) bỏ bã hớt váng đem gạt cặn.
Giai đoạn 4: lọc mắm nhỉ, pha chế và đóng chai. Trước đây, người ta thường dùng than củi sạch trong quá trình lọc mắm.
a) Để đánh giá chất lượng của nước mắm, người ta thường dựa vào độ đạm (số gam nitrogen trên 100 mL nước mắm). Khi dùng 200 kg cá cơm (chứa 70% nước, 20% protein và 10% lipid và các chất khác) để làm nước mắm thì thu được 190 lít nước mắm có độ đạm là 21,05. Biết rằng: 1 gam protein chứa trung bình 16% khối lượng nitrogen. ĐÚNG
b) Than củi sạch được sử dụng trong giai đoạn 4 trong quá trình lọc mắm có tác dụng hấp phụ tạp chất, giúp nước mắm trong hơn, sạch hơn; góp phần loại bỏ các mùi không mong muốn, cải thiện chất lượng nước mắm. ĐÚNG
c) Giai đoạn 2 protein trong cá cơm sẽ bị thủy phân thành các amino acid và các sản phẩm chứa nitrogen khác. ĐÚNG
d) Muối ăn trong giai đoạn 1 giúp bảo quản, ức chế sự phát triển của vi khuẩn gây hư hỏng, tạo điều kiện thuận lợi cho quá trình lên men. ĐÚNG
Câu 22: Một pin điện hóa Zn – H2 được thiết lập ở điều kiện thường như hình vẽ sau (vôn kế có điện trở rất lớn).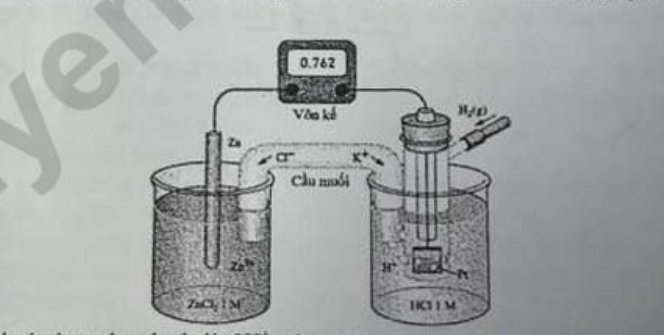
a) Quá trình oxi hoá xảy ra ở cathode là: 2H+ + 2e → H2. SAI
b) Thế điện cực chuẩn của cặp oxi hoá – khử Zn2+/Zn là -0,762V. ĐÚNG
c) Chất điện li trong cầu muối là KNO3. ĐÚNG
d) Phản ứng hoá học xảy ra trong pin là: Zn(s) + 2H+(aq) → Zn2+(aq) + H2(g). ĐÚNG
PHẦN III. Câu trắc nghiệm yêu cầu trà lời ngắn. Thí sinh trả lời từ Câu 23 đến Câu 28.
Câu 23: Epibatidine, một loại đầu kháng mau được phân lập từ da của loài ếch mũ tên độc Equadorian Epipedobates ba màu. Đây là hợp chất có tác dụng giảm đau gấp vài lần morphine, nhưng lại không gây nghiện. Cấu trúc hóa học của epibatidine mô tả như hình dưới: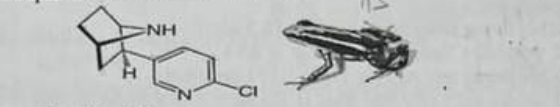
Số nguyên tử hydrogen trong epibatidine là ? 2
Câu 24: Trong số các chất: NaHCO3, Al, CaCl2, Ag có bao nhiêu chất tác dụng được với dung dịch HCl ở nhiệt độ thường? NaHCO3, Al, Ag.
Câu 25: Một nhà máy sản xuất urea sử dụng quy trình Haber-Bosch : N2(g) + 3H2(g) (\rightleftharpoons) 2NH3(g) để sản xuất ammonia. Giai đoạn sản xuất khí hydrogen bằng phản ứng của khí methane (CH4) và hơi nước (H2O) được thực hiện theo phương trình hóa học (1) như sau:
CH4(g) + H2O(g) —> CO(g) + 3H2(g) (1)
Phản ứng (1) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy khí methane theo phương trình hóa học (2):
CH4(g) + 2O2(g) —-> CO2(g) + 2H2O(g) (2)
Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của methane ở phản ứng (1) là 95%. Tính khối lượng khí methane (theo tấn, làm tròn đến hàng phần mười) cần thiết để sản xuất 3,40 tấn NH3(g) trong giai đoạn trên. Biết 80% lượng nhiệt tỏa ra từ phản ứng (2) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành (Δ, Ho298) của các chất ở điều kiện chuẩn được cho trong bảng sau:
Câu 26: Cho các trường hợp sau:
(1) Sợi dây Ag nhúng trong dung dịch HNO3.
(2) Cho thanh Fe tiếp xúc với thanh Cu rồi đồng thời nhúng vào dung dịch HCl.
(3) Thanh Zn nhúng trong dung dịch CuSO4.
(4) Thanh Zn nhúng trong dung dịch H2SO4 loãng.
(5) Nhúng thanh thép vào dung dịch HNO3 loãng.
Số trường hợp xuất hiện ăn mòn điện hoá là trường hợp 1, 2, 3 và 4.
Câu 27: Cho dãy các carbohydrate sau: glucose, saccharose, cellulose, tinh bột và fructose. Số chất trong dãy phản ứng được với Cu(OH)2 trong môi trường kiềm ở nhiệt độ thường tạo thành dung dịch có màu xanh lam là glucose, fructose và saccharose.
Câu 28: Thuỷ phân hoàn toàn 8,8 gam ester X có công thức phân tử C4H8O2 trong 300 ml dung dịch NaOH 1M thu được hỗn hợp hai chất hữu cơ Y và Z trong đó Y có tỉ khối hơi so với H2 là 23. Khối lượng chất rắn thu được khi cô cạn dung dịch sau phản ứng có giá trị là 6,6 gam.
Mục đích tổ chức thi tốt nghiệp THPT 2025 là gì?
Căn cứ theo Mục 1 Phương án Tổ chức kỳ thi và xét công nhận tốt nghiệp trung học phổ thông từ năm 2025 ban hành kèm theo Quyết định 4068/QĐ-BGDĐT ngày 30/10/2023 của Bộ Giáo dục và Đào tạo, mục đích tổ chức kỳ thi tốt nghiệp THPT năm 2025 nhằm:
– Đánh giá đúng kết quả học tập của người học theo mục tiêu và chuẩn cần đạt theo yêu cầu của Chương trình giáo dục phổ thông (GDPT) 2018.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông (THPT) và làm một trong các cơ sở để đánh giá chất lượng dạy, học của các cơ sở giáo dục phổ thông và công tác chỉ đạo của các cơ quan quản lý giáo dục.
– Cung cấp dữ liệu đủ độ tin cậy cho các cơ sở giáo dục đại học, giáo dục nghề nghiệp sử dụng trong tuyển sinh theo tinh thần tự chủ.
Thí sinh thi tốt nghiệp THPT 2025 có bắt buộc thi môn Hóa học không?
Căn cứ theo Mục 5 Phương án Tổ chức kỳ thi và xét công nhận tốt nghiệp trung học phổ thông từ năm 2025 ban hành kèm theo Quyết định 4068/QĐ-BGDĐT năm 2023, quy định như sau:
Thí sinh dự thi tốt nghiệp bắt buộc phải thi môn Ngữ văn, môn Toán và 02 môn tự chọn trong số các môn còn lại đã được học ở lớp 12, bao gồm: Ngoại ngữ, Lịch sử, Vật lí, Hóa học, Sinh học, Địa lí, Giáo dục kinh tế và pháp luật, Tin học, Công nghệ.
Đồng thời, căn cứ theo Điều 3 Quy chế thi tốt nghiệp THPT ban hành kèm theo Thông tư 24/2024/TT-BGDĐT, các môn thi được tổ chức như sau:
Môn thi
Kỳ thi gồm 03 buổi thi:
– 01 buổi thi môn Ngữ văn,
– 01 buổi thi môn Toán,
– 01 buổi thi của bài thi tự chọn gồm 02 môn trong số các môn: Vật lí, Hóa học, Sinh học, Lịch sử, Địa lí, Giáo dục kinh tế và pháp luật, Tin học, Công nghệ định hướng Công nghiệp (Công nghệ Công nghiệp), Công nghệ định hướng Nông nghiệp (Công nghệ Nông nghiệp), Ngoại ngữ (Tiếng Anh, Tiếng Nga, Tiếng Pháp, Tiếng Trung Quốc, Tiếng Đức, Tiếng Nhật và Tiếng Hàn).
Theo quy định này, các môn thi tốt nghiệp THPT năm 2025 bao gồm:
02 môn bắt buộc: Toán và Ngữ văn.
– 02 môn tự chọn trong số các môn: Vật lí, Hóa học, Sinh học, Lịch sử, Địa lí, Giáo dục kinh tế và pháp luật, Tin học, Công nghệ định hướng Công nghiệp, Công nghệ định hướng Nông nghiệp, Ngoại ngữ.
Như vậy, kỳ thi tốt nghiệp THPT năm 2025 không bắt buộc thí sinh phải thi môn Hóa học.
Việc thi môn Hóa học chỉ áp dụng nếu thí sinh chọn môn này là một trong hai môn tự chọn. Nếu thí sinh không chọn môn Hóa học, thì không bắt buộc phải dự thi môn này.




