Đề thi thử Đại học 2025 môn Hóa học – Đề 15 là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Với cấu trúc bám sát đề minh họa mới nhất của Bộ GD&ĐT, đề số 15 không chỉ giúp học sinh ôn luyện hiệu quả mà còn là công cụ đánh giá năng lực toàn diện trước kỳ thi tốt nghiệp THPT. Các câu hỏi được phân bố hợp lý từ nhận biết – thông hiểu đến vận dụng – vận dụng cao, trải đều trên nhiều chuyên đề như: Phản ứng trao đổi ion trong dung dịch, điện phân, kim loại và hợp chất, este – lipit, amin – amino axit – protein, bài toán đồ thị và nhận biết hóa chất.
Những kiến thức và kỹ năng học sinh cần tập trung khi làm đề này:
- Kỹ năng xác định nhanh bản chất phản ứng và lựa chọn phương pháp giải tối ưu.
- Vận dụng linh hoạt các định luật bảo toàn trong bài toán nhiều chất, nhiều bước.
- Phân tích dữ liệu thực nghiệm, đồ thị, và chuỗi biến hóa hóa học.
Hãy cùng Dethitracnghiem.vn tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 – ĐỀ 15













PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1: Khi bị cháy xăng dầu không nên dùng nước để dập tắt vì
A. Xăng dầu nhẹ hơn nước nổi trên mặt nước, làm tăng khả năng tiếp xúc với oxygen, làm đám cháy loang rộng hơn.
B. Xăng dầu tác dụng với nước
C. Nước xúc tác cho phản ứng cháy của xăng dầu
D. Đám cháy cung cấp nhiệt làm H₂O bị phân hủy giải phóng oxygen cung cấp thêm cho đám cháy to hơn.
Câu 2: Benzyl acetate là ester có mùi thơm của hoa nhài. Công thức của benzyl acetate là
A. C₂H₅COOC₆H₅.
B. CH₃COOC₆H₅.
C. C₆H₅COOCH₃.
D. CH₃COOCH₂C₆H₅.
Câu 3: Để tráng một lớp bạc lên ruột phích, người ta cho chất X phản ứng với lượng dư dung dịch AgNO₃ trong NH₃ đun nóng. Chất X là
A. tinh bột.
B. ethyl acetate.
C. saccharose.
D. glucose.
Câu 4: Số nhóm amino và số nhóm carboxyl có trong một phân tử glutamic acid tương ứng là
A. 1 và 2.
B. 1 và 1.
C. 2 và 1.
D. 2 và 2.
Câu 5: Polymer nào sau đây trong thành phần chỉ gồm hai nguyên tố C và H?
A. Poly(phenol formaldehyde).
B. Poly(methyl methacrylate).
C. Polybuta-1,3-diene.
D. Nylon-6,6.
Câu 6: Cho biết số thứ tự của Mg trong bảng tuần hoàn là 12. Vị trí của Mg trong bảng tuần hoàn là
A. chu kì 3, nhóm IIIA
B. chu kì 3, nhóm IIB.
C. chu kì 3, nhóm IIA
D. chu kì 2, nhóm IIA
Câu 7: Các kim loại Na, K đều hoạt động hóa học mạnh. Vì vậy, để bảo quản lâu dài, chúng thường được ngâm trong
A. dầu hỏa.
B. nước máy.
C. ethyl alcohol
D. giấm ăn.
Câu 8: Nguyên tử của một nguyên tố X có tổng số các loại hạt trong hạt nhân là 79. Trong đó số hạt mang điện là 35 hạt. Kí hiệu nguyên tử của X là
A. ⁷⁹₃₅X
B. ⁹⁰₃₅X
C. ⁴⁵₃₅X
D. ¹¹⁵₃₅X
Câu 9: Cho các cân bằng hoá học:
(1) N₂(g) + 3H₂(g) ⇌ 2NH₃(g)
(2) H₂(g) + I₂(g) ⇌ 2HI(g)
(3) 2SO₂(g) + O₂(g) ⇌ 2SO₃(g)
(4) 2NO₂(g) ⇌ N₂O₄(g)
Khi thay đổi áp suất những cân bằng hóa học bị chuyển dịch là:
A. (1), (2), (3).
B. (2), (3), (4).
C. (1), (3), (4).
D. (1), (2), (4).
Câu 10: Chất X được tạo thành trong cây xanh nhờ quá trình quang hợp. Thủy phân hoàn toàn X (xúc tác acid) thu được chất Y. Chất Y có nhiều trong quả nho chín nên còn được gọi là đường nho. Hai chất X và Y lần lượt là
A. tinh bột và glucose.
B. cellulose và saccharose.
C. cellulose và fructose.
D. tinh bột và saccharose.
Câu 11: Thủy phân không hoàn toàn tetrapeptide X mạch hở, thu được hỗn hợp sản phẩm trong đó có Gly-Ala, Phe-Val và Ala-Phe. Cấu tạo của X là
A. Gly-Ala-Val-Phe.
B. Val-Phe-Gly-Ala.
C. Ala-Val-Phe-Gly.
D. Gly-Ala-Phe-Val.
Câu 12: Khi pin làm việc ở điều kiện chuẩn, nhận định nào sau đây là đúng?![]() A. Ag được tạo ra ở cực dương, Ni được tạo ra ở cực âm.
A. Ag được tạo ra ở cực dương, Ni được tạo ra ở cực âm.
B. Ag được tạo ra ở cực dương, Ni²⁺ được tạo ra ở cực âm.
C. Ag⁺ được tạo ra ở cực âm và Ni được tạo ra ở cực dương.
D. Ag⁺ được tạo ra ở cực âm và Ni²⁺ được tạo ra ở cực dương.
Câu 13: Để tái chế nhôm, người ta có thể sử dụng phế liệu kim loại như vỏ của các lon, hộp chứa nước giải khát hay thực phẩm. Phế liệu này còn lẫn các tạp chất là các hợp chất hữu cơ và vô cơ (có trong nhãn, mác in hoặc sơn trên vỏ lon, hộp). Phế liệu được cắt, băm nhỏ rồi cho vào lò nung đến khi chảy lỏng. Phần lớn các tạp chất biến thành xỉ lỏng, nổi lên trên, được vớt ra khỏi lò. Phần còn lại trong lò là nhôm tái chế ở trạng thái nóng chảy. a. Quá trình tái chế nhôm thể hiện sự chuyển thể của nhôm lần lượt là sự nóng chảy, sự đông đặc.
a. Quá trình tái chế nhôm thể hiện sự chuyển thể của nhôm lần lượt là sự nóng chảy, sự đông đặc.
b. Có thể sử dụng nhôm tái chế theo quy trình trên để tạo dụng cụ y tế.
c. Giai đoạn cắt, băm nhỏ phế liệu nhôm trước khi nung chảy: giúp giảm bớt thể tích và tiết kiệm nhiên liệu đốt nung nóng chảy.
d. Tái chế nhôm ít gây ô nhiễm môi trường.
Số nhận định đúng là
A. 1
B. 2
C. 3
D. 4
Câu 14: Muối nào sau đây tồn tại trong dung dịch và bị phân huỷ khi đun nóng?
A. CaCO₃.
B. Ca(HCO₃)₂.
C. CaCl₂.
D. CaSO₄.
Câu 15: Cho phát biểu sau: “Phức chất đơn giản thường có một…(1)… liên kết với các phối tử bao quanh. Liên kết giữa nguyên tử trung tâm và phối tử trong phức chất là liên kết …(2)…”. Cụm từ cần điền vào (1) và (2) lần lượt là
A. cation kim loại, ion.
B. nguyên tử kim loại, cho – nhận.
C. nguyên tử trung tâm, cho – nhận.
D. phối tử, ion.
Câu 16: Phân rã tự nhiên \( ^{232}_{90}\text{Th} \) tạo ra đồng vị bền \( ^{208}_{82}\text{Pb} \) đồng thời giải phóng một số hạt α và β. Vận dụng định luật bảo toàn số khối và bảo toàn điện tích tính được số hạt α và β cho quá trình phân rã một hạt nhân \( ^{223}_{90}\text{Th} \) lần lượt là
A. 8; 6.
B. 6; 4.
C. 6; 8.
D. 8; 4.
Câu 17: Một hợp chất hữu cơ X có % khối lượng của C, H, Cl lần lượt là: 14,28% ; 1,19% ; 84,53%. Công thức phân tử của X và số công thức cấu tạo phù hợp là
A. CHCl₃ và 1.
B. C₂H₂Cl₄ và 3.
C. C₂H₄Cl₂ và 2.
D. C₂H₂Cl₄ và 2.
Câu 18: Cho một pin Galvani với điện cực Zn và Cu có sức điện động chuẩn là 1,34V. Sử dụng pin này để thắp sáng một bóng đèn nhỏ với cường độ dòng điện chạy qua là I = 0,02A. Nếu điện cực kẽm hao mòn 0,1 mol do pin phóng điện thì thời gian tối đa mà pin thắp sáng được bóng đèn là bao nhiêu giờ ?Cho biết các công thức:
Q = n.F = I.t , trong đó: Q là điện lượng (C), n là số mol electron đi qua dây dẫn, I là cường độ dòng điện (A),t là thời gian (giây), F là hằng số Faraday ( 96500Cmol⁻¹).
A. 128
B. 268
C. 234
D. 134
PHẦN II. Câu hỏi trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu thí sinh chọn đúng hoặc sai.
Câu 1: α-Linolenic acid (ALA) là một acid béo được tìm thấy các loại các loại hạt (chia, hạnh lanh, cây gai dầu), quả hạch (đặc biệt là quả óc chó) và các loại dầu thực vật phổ biến. Đây là một trong hai acid béo cần thiết cho sức khỏe mà cơ thể không tự tổng hợp được mà có được thông qua ăn uống. ALA có công thức cấu tạo như sau: a) ALA có 18 nguyên tử carbon.
a) ALA có 18 nguyên tử carbon.
b) Phản ứng của ALA với ethyl alcohol là phản ứng thuận nghịch.
c) Vận dụng Nội dung Chất béo chứa 3 gốc ALA có phân tử khối là 878.
d) Để hoá rắn 1 mol chất béo có cấu tạo gồm 3 gốc của ALA cần 8 mol H₂.
Câu 2: Năm 1965, trong quá trình tổng hợp thuốc chống loét dạ dày, nhà hóa học James M. Schlatter (Mỹ) đã vô tình phát hiện hợp chất X (một chất ngọt nhân tạo với tên thường gọi là “Aspartame”) có cấu tạo như hình dưới: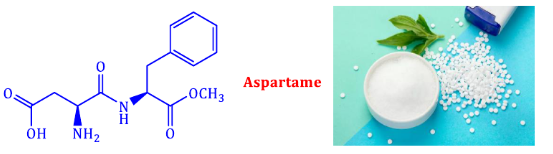
Aspartame ngọt hơn khoảng 200 lần so với đường ăn thông thường. Aspartame thường được sử dụng trong đồ uống và thực phẩm dành cho người ăn kiêng vì có ít calo hơn đường thông thường. Tổ chức Y tế thế giới (WHO) thông báo xếp chất làm ngọt nhân tạo aspartame vào danh sách các chất “có thể gây ung thư cho con người” nhưng lưu ý chất này vẫn an toàn nếu được tiêu thụ trong giới hạn khuyến nghị hằng ngày. Hướng dẫn của WHO đã không thay đổi kể từ năm 1981: tối đa 40 miligam aspartame/mỗi kg trọng lượng cơ thể/ngày. Các khuyến nghị của Mỹ “hào phóng” hơn một chút: Vào năm 1983, FDA (Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ) đưa ra mức 50 miligam/mỗi kg trọng lượng cơ thể/ngày. Hiệp hội Đồ uống Mỹ cho biết soda dành cho người ăn kiêng thường chứa trung bình 100 miligam aspartame mỗi lon.
a) Biết Nội dung Nước ngọt có gas như pepsi vị chanh 0 calo “sảng khoái tột đỉnh, bung hết chất mình” có thể sử dụng aspartame làm chất tạo ngọt.
b) Vận dụng Nội dung Phần trăm khối lượng của nguyên tố oxygen trong aspartame khoảng 30,21%.
c) Hiểu Nội dung Aspartame là ester methyl với dipeptide tạo bởi aspartic acid (HOOCCH(NH₂)CH₂COOH) và phenylalanine (C₆H₅CH₂CH(NH₂)COOH).
d) Vận dụng Nội dung Số lon soda mà một người nặng trung bình ở Mỹ là 80kg nên uống theo khuyến nghị về lượng aspartame giới hạn hằng ngày của WHO và FDA hơn kém nhau khoảng 13 lon.
Câu 3: Thực hiện thí nghiệm sau:
Bước 1: Cho dung dịch NaCl 5% vào ống thuỷ tinh hình chữ U như hình bên.
Bước 2: Nhúng một thanh đồng và một thanh kẽm đã làm sạch vào hai đầu của ống chữ U.
Bước 3: Nối hai thanh kim loại bằng dây dẫn.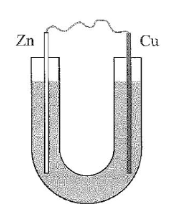 Sau bước 3,
Sau bước 3,
a) Biết Nội dung chỉ xảy ra ăn mòn hoá học và có sự phát sinh dòng điện.
b) Hiểu Nội dung kẽm bị oxi hoá và đóng vai trò là anode.
c) Hiểu Nội dung Cu²⁺ bị khử thành Cu bám vào thanh đồng, làm khối lượng thanh đồng tăng dần.
d) Biết Nội dung kẽm bị ăn mòn, đồng không bị ăn mòn.
Câu 4: Gói làm nóng thức ăn (FRH: Flameless Ration Heater) được phát minh nhằm hâm nóng các bữa ăn tiện lợi cho người lính trên chiến trường. Một số gói lâu tự sôi cũng sử dụng công nghệ này. FRH có thành phần chính gồm bột kim loại Mg trộn với một lượng nhỏ bột Fe và NaCl. Khi sử dụng, chỉ cần cho khoảng 30 mL nước vào hỗn hợp FRH, hỗn hợp này phản ứng mãnh liệt theo phương trình Mg(s) + 2H₂O(l) → Mg(OH)₂(s) + H₂ (g) và tỏa rất nhiều nhiệt, đủ để làm nóng thức ăn nhanh chóng.
a) Một gói FRH chứa khoảng 8 gam hỗn hợp (Mg 90%, Fe 4% và NaCl 4% về khối lượng) có thể tỏa ra tối đa 642,6 kJ. Biết rằng enthalpy tạo thành chuẩn (ΔfH⁰₂₉₈) của Mg(OH)₂(s) và H₂O (l) lần lượt là -928,4 kJ mol⁻¹và-285,8 kJ mol⁻¹.
b) Gói FRH trên có đủ làm nóng 300 g súp từ 30 °C lên 100 °C .Biết nhiệt dung riêng của súp khoảng 4,2 J g⁻¹ C⁻¹, giả sử gói súp chỉ nhận được 50% lượng nhiệt tối đa tỏa ra, phần nhiệt còn lại làm nóng các vật dụng khác và thất thoát vào môi trường.
c) Magnesium phản ứng chậm với nước ở nhiệt độ thường, nhưng magnesium trong gói FRH lại có thể phản ứng nhanh chóng với nước.
d) Người ta chỉ dùng khoảng 30 mL nước mà không dùng lượng nước nhiều hơn.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1: Khí oxygen được điều chế trong phòng thí nghiệm bằng cách nhiệt phân potassium chlorate. Để thí nghiệm thành công và rút ngắn thời gian tiến hành có thể dùng một số biện pháp sau:
(1) Dùng chất xúc tác manganes dioxide
(2) Nung ở nhiệt độ cao
(3) Dùng phương pháp dời nước để thu khí oxygen
(4) Đập nhỏ potassium chlorate.
Số biện pháp dùng để tăng tốc độ phản ứng là
Câu 2: Cho các chất sau: C₁₅H₃₁COONa; C₁₅H₃₁COOK; CH₃[CH₂]₁₀OSO₃Na; CH₃[CH₂]₁₁C₆H₄SO₃Na; C₁₇H₃₅COOK. Số chất là thành phần chính của chất giặt rửa tổng hợp?
Câu 3: Các phát biểu sau nói về ứng dụng của tinh bột hoặc cellulose:
(1) Cung cấp những chất dinh dưỡng cơ bản của người và động vật.
(2) Trong công nghiệp dùng sản xuất bánh kẹo, glucose, ethanol và hồ dán.
(3) Sản xuất sợi tự nhiên và sợi nhân tạo.
(4) Sản xuất ethanol và cellulose trinitrate (dùng chế tạo thuốc súng không khói).
Số phát biểu nói về ứng dụng của cellulose là …
Câu 4. Thực hiện các thí nghiệm sau
Thí nghiệm 1: Rót khoảng 2 mL dung dịch HCl vào ống nghiệm có một viên Zn nguyên chất.
Thí nghiệm 2: Rót khoảng 2 mL dung dịch HCl vào ống nghiệm có một viên Zn nguyên chất, sau đó thêm vài giọt dung dịch CuSO₄.
Thí nghiệm 3: Rót khoảng 2 mL dung dịch HCl vào ống nghiệm có một mẩu dây đồng.
Thí nghiệm 4: Rót khoảng 2 mL dung dịch HCl vào ống nghiệm có một viên Zn nguyên chất và một mẩu dây Cu tiếp xúc với nhau.
Số thí nghiệm xuất hiện ăn mòn điện hóa là bao nhiêu?
Câu 5.Cho dãy các hợp chất của kim loại nhóm IA: Na₂CO₃, NaHCO₃, KOH, K₂SO₄, K₂CO₃ và KHCO₃. Hợp chất X có cả hai tính chất sau:
– Tác dụng với dung dịch HCl tạo ra khí Y làm đục nước vôi trong.
– Đốt trên ngọn lửa đèn khí thấy ngọn lửa có màu tím.
Có bao nhiêu chất trong dãy trên thỏa mãn cả hai tính chất của hợp chất X?
Câu 6. Dung dịch FeSO₄ để lâu ngày bị oxi hóa một phần bởi oxi của không khí tạo thành Fe³⁺ (dung dịch X). Cho 30 mL dung dịch H₂SO₄ 0,5M vào 10 mL dung dịch X thu được dung dịch Y.
Thí nghiệm 1: Chuẩn độ 10,0 mL dung dịch Y bằng dung dịch KMnO₄ 0,05M cho đến khi xuất hiện màu hồng nhạt bền (phản ứng coi như vừa đủ) thì thấy hết 9,0 mL dung dịch KMnO₄.
Thí nghiệm 2: Ngâm một lá sắt dư vào 10,0 mL dung dịch Y, khuấy đều cho đến khi khử hoàn toàn Fe³⁺ thành Fe²⁺. Lấy lá sắt ra và rồi chuẩn độ bằng dung dịch KMnO₄ 0,05M. Khi màu hồng nhạt bền xuất hiện thì thấy hết 10,5 mL dung dịch KMnO₄. Lượng FeSO₄ bị oxi hóa trong không khí bao nhiêu %? (làm tròn đến phần nguyên).
Mục đích tổ chức kỳ thi Tốt nghiệp THPT năm 2025 là gì?
Căn cứ theo các văn bản chỉ đạo và hướng dẫn của Bộ Giáo dục và Đào tạo, kỳ thi Tốt nghiệp THPT năm 2025 được tổ chức nhằm đạt các mục tiêu chính sau:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo chương trình giáo dục phổ thông mới.
– Sử dụng kết quả kỳ thi để xét công nhận tốt nghiệp THPT và làm cơ sở tuyển sinh cho các trường đại học, cao đẳng.
– Góp phần phản ánh chất lượng giáo dục của từng địa phương và trên phạm vi cả nước, đồng thời là căn cứ điều chỉnh nội dung, phương pháp dạy học trong nhà trường.
Thí sinh thi tốt nghiệp THPT năm 2025 có bắt buộc phải thi môn Hóa học không?
Theo quy định của Bộ GD&ĐT, kỳ thi Tốt nghiệp THPT năm 2025 bao gồm 3 bài thi bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
Ngoài ra, thí sinh phải chọn một trong hai bài thi tổ hợp:
– Tổ hợp Khoa học Tự nhiên (KHTN): gồm các môn Vật lí, Hóa học, Sinh học.
– Tổ hợp Khoa học Xã hội (KHXH): gồm các môn Lịch sử, Địa lí, Giáo dục công dân (áp dụng cho học sinh chương trình GDPT).
Như vậy, môn Hóa học chỉ bắt buộc đối với thí sinh đăng ký thi tổ hợp KHTN, phục vụ cho mục đích xét tốt nghiệp hoặc tuyển sinh đại học, cao đẳng vào các ngành có yêu cầu môn Hóa.
Vì lý do đó, Đề thi thử tốt nghiệp THPT 2025 môn Hóa học – Đề 15 là tài liệu ôn luyện hữu ích dành cho học sinh chọn tổ hợp KHTN. Đề thi giúp học sinh rèn luyện kỹ năng làm bài, củng cố kiến thức và chuẩn bị tâm thế vững vàng cho kỳ thi chính thức.




