Đề thi thử Đại học 2025 môn Hóa học – Đề 4 là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Đề 4 là một phần trong chuỗi luyện đề bám sát theo cấu trúc đề thi tốt nghiệp THPT 2025 môn Hóa học của Bộ Giáo dục và Đào tạo. Đề thi được thiết kế với các câu trắc nghiệm trải đều từ mức độ nhận biết đến vận dụng cao, kèm theo đáp án chi tiết giúp học sinh tự học và tra cứu dễ dàng.
Các trọng tâm kiến thức xuất hiện trong đề bao gồm:
- Phần vô cơ: Phản ứng trao đổi ion, dãy hoạt động kim loại, phản ứng nhiệt phân – điện phân, dạng bài kim loại phản ứng với axit, muối và nước.
- Phần hữu cơ: Phân biệt este – ancol – axit – amin – peptit – glucozơ, viết sơ đồ phản ứng chuyển hóa hợp chất, nhận biết hợp chất hữu cơ qua phản ứng màu.
- Dạng bài tập phổ biến: Bài toán đồ thị – hiệu suất phản ứng – bài toán tổng hợp nhiều chất – nhận biết hóa chất qua hiện tượng – bài toán pH và thủy phân este – peptit.
- Kỹ năng quan trọng: Tư duy phân tích đề nhanh, kết nối dữ kiện logic, áp dụng sơ đồ tư duy và bảng hệ thống hóa kiến thức.
Đề số 4 không chỉ phù hợp để luyện tập nâng cao trình độ, mà còn giúp học sinh phát hiện lỗ hổng kiến thức và làm quen với các bẫy thường gặp trong đề thi thật.
Hãy cùng Dethitracnghiem.vn cùng tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 SỞ – ĐỀ 4






PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Trường hợp nào sau đây không xảy ra sự ăn mòn kim loại?
A. Tàu đánh cá làm bằng thép bị hoen gỉ sau thời gian đi biển về.
B. Tượng đồng bị chuyển màu xanh khi để lâu ngày trong không khí ẩm.
C. Vòng tay làm bằng bạc kim loại bị hoá đen khi sử dụng lâu ngày.
D. Nấu chảy vàng để đúc khuôn khi chế tác vàng trang sức.
Câu 2. Đặc điểm về tính chất vật lí nào sau đây là đúng với kim loại kiềm?
A. Khối lượng riêng lớn.
B. Nhiệt độ nóng chảy và nhiệt độ sôi cao.
C. Dẫn điện tốt hơn Cu.
D. Độ cứng thấp.
Câu 3. Qua nghiên cứu thực nghiệm cho thấy cao su thiên nhiên là polymer của monomer nào sau đây?
A. Buta-1,2-diene.
B. Buta-1,3-diene.
C. 2-methylbuta-1,3-diene.
D. Buta-1,4-diene.
Câu 4. Liên kết trong mạng tinh thể kim loại là loại liên kết nào sau đây?
A. Liên kết ion.
B. Liên kết cộng hoá trị.
C. Liên kết hydrogen.
D. Liên kết kim loại.
Câu 5. Cho các loại nước sau:
(a) Nước có chứa nhiều ion Ca²⁺.
(b) Nước có chứa nhiều ion Ca²⁺,Mg²⁺, HCO₃⁻.
(c) Nước có chứa ít ion Ca²⁺,Mg²⁺ nhưng chứa nhiều ion SO₄²⁻.
(d) Nước có chứa ít ion Ca²⁺ nhưng chứa nhiều ion Mg²⁺ và Cl⁻.
Loại nước nào trong các loại nước trên không phải là nước cứng?
A. (a) và (c).
B. (a) và (d).
C. Chỉ có (c).
D. (c) và (d).
Câu 6. Phản ứng thủy phân chất ester trong môi trường kiềm gọi là phản ứng
A. ester hóa.
B. xà phòng hóa.
C. trung hòa.
D. trùng ngưng.
Câu 7. Sự phát triển của công nghệ tạo ra nhiều phương pháp tổng hợp polymer nhằm phục vụ đời sống, bên cạnh việc khai thác các polymer sẵn có từ thiên nhiên. Phát biểu nào sau đây về các phương pháp điều chế polymer là đúng?
A. Cellulose là polymer trùng ngưng giữa các phân tử glucose.
B. Poly(vinyl alcohol) được tổng hợp từ alcohol tương ứng.
C. Polystyrene được tổng hợp từ styrene bằng phản ứng trùng hợp.
D. Tơ olon (hay polyacrylonitrile) được khai thác từ thiên nhiên.
Câu 8. NaHCO₃ được sử dụng là phụ gia thực phẩm với tên gọi baking soda, có kí hiệu là E500(ii) dùng làm chất điều chỉnh độ chua trong sốt cà Khi đó, NaHCO₃ sẽ tác dụng với H⁺ để làm giảm nồng chua, nước ép hoa quả,… độ H⁺. Vai trò của NaHCO₃ trong phản ứng là
A. acid.
B. chất oxi hoá.
C. chất khử.
D. base.
Câu 9. Phổ khối lượng (MS) là phương pháp hiện đại để xác định phân tử khối của các hợp chất hữu cơ. Kết quả phân tích phổ khối lượng cho thấy phân tử khối của hợp chất hữu cơ X là 60. Chất X có thể là
A. acetic acid.
B. methyl acetate.
C. acetone.
D. ethanol.
Câu 10. Cho một mẫu nhỏ calcium (Ca) vào cốc nước có thêm vài giọt dung dịch phenolphathalein. Khi kết thúc phản ứng,
A. dung dịch trong cốc trong suốt, màu hồng và có pH lớn hơn 7.
B. dung dịch trong cốc có màu xanh và trong suốt.
C. dung dịch trong cốc có màu hồng và vẩn đục.
D. dung dịch trong cốc có màu hồng và trong suốt.
Câu 11. Nicotine là một loại alkaloid tự nhiên được tìm thấy trong cây thuộc họ Cà, chủ yếu trong thuốc lá (nicotine chiếm 0,6 – 3,0% trọng lượng thuốc lá khô). Nicotine có nhiều tác hại đối với cơ thể, nhất là đối với phụ nữ mang thai và trẻ sơ sinh, do đó cần hạn chế sử dụng và phổ biến thuốc lá. Công thức cấu tạo phân tử nicotine như hình bên. Trong phân tử nicotine, nguyên tử N số (1) là amine bậc mấy?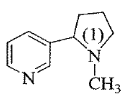 A. Bậc I.
A. Bậc I.
B. Bậc II.
C. Bậc III.
D. Bậc IV.
Câu 12. Chất nào sau đây thuộc loại disaccharide?
A. Glucose.
B. Saccharose.
C. Cellulose.
D. Fructose.
Câu 13. Cho hỗn hợp các alkane có mạch carbon thẳng sau: pentane (sôi ở 36°C), heptane (sôi ở 98°C), octane (sôi ở 126°C) và nonane (sôi ở 151°C). Có thể tách riêng các chất đó bằng cách nào sau đây?
A. Chiết.
B. Kết tinh.
C. Bay hơi.
D. Chưng cất.
Câu 14. Chất ứng với công thức nào sau đây không có tác dụng giặt rửa?
A. CH₃[CH₂]₁₆COOK.
B. CH₃[CH₂]₁₀CH₂C₆H₄SO₃Na.
C. (CH₃[CH₂]₁₄COO)₃C₃H₅.
D. CH₃[CH₂]₁₀CH₂OSO₃Na.
Câu 15. Khi đun nóng protein trong dung dịch acid hoặc kiềm hoặc dưới tác dụng của các enzyme, protein bị thủy phân thành ..(1)…, cuối cùng thành ..(2)..
A. (1) phân tử protein nhỏ hơn; (2) amino acid.
B. (1) chuỗi polypeptide; (2) hỗn hợp các α-amino acid.
C. (1) chuỗi polypeptide; (2) amino acid.
D. (1) amino acid; (2) chuỗi polypeptide.
Câu 16. Quan sát Hình 6.1 dưới đây: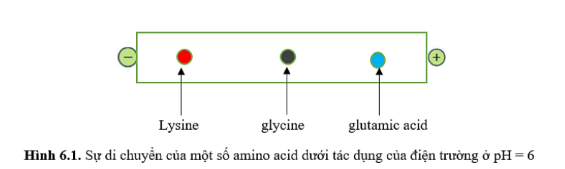 Trong điều kiện thí nghiệm ở pH = 6,0, cho các phát biểu sau:
Trong điều kiện thí nghiệm ở pH = 6,0, cho các phát biểu sau:
(a) Lysine dịch chuyển về phía cực âm nên lysine tồn tại chủ yếu ở dạng cation.
(b) Glycine hầu như không dịch chuyển nên glycine tồn tại chủ yếu ở dạng ion lưỡng cực.
(c) Glutamic acid dịch chuyển về phía cực âm nên glutamic acid tồn tại chủ yếu ở dạng anion.
(d) Thí nghiệm trên chứng minh tính điện li của các phân tử amino acid.
Số phát biểu đúng là
A. 2.
B. 3.
C. 1.
D. 4.
Câu 17. Thuỷ ngân (Hg) có thể chuyển thành dạng hơi khuếch tán trong không khí, khi đó sẽ làm tăng nguy cơ mắc các bệnh về hô hấp và một số bệnh khác. Khi nhiệt kế thuỷ ngân bị vỡ, có thể sử dụng hoá chất nào sau đây để loại bỏ thuỷ ngân?
A. Dung dịch HCl.
B. Dung dịch NaOH.
C. Bột lưu huỳnh.
D. Bột than gỗ (chứa carbon).
Câu 18. Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá – khử sau: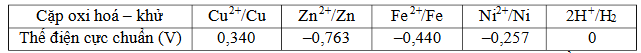 Số kim loại trong dãy các kim loại Zn, Ni, Fe, Cu phản ứng được với dung dịch HCl ở điều kiện chuẩn là
Số kim loại trong dãy các kim loại Zn, Ni, Fe, Cu phản ứng được với dung dịch HCl ở điều kiện chuẩn là
A. 3.
B. 4.
C. 1.
D. 2.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Thực hiện thí nghiệm cho dung dịch NH₃ vào ống nghiệm đựng bột Ni(OH)₂ xanh lá cây đến dư, thu được phức chất bát diện chỉ chứa phối tử NH₃ có màu xanh dương.
a) Phức chất [Ni(NH₃)₆]²⁺ được tạo thành.
b) Dấu hiệu nhận biết phức chất tạo thành là kết tủa màu xanh lá cây bị tan ra.
c) Phức chất thu được chứa bốn phối tử NH₃
d) Phức chất thu được có nguyên tử trung tâm là Ni²⁺.
Câu 2. Trong phòng thí nghiệm, ethyl acetate được điều chế từ acetic acid và ethanol, xúc tác H₂SO₄ đặc, theo mô hình thí nghiệm sau: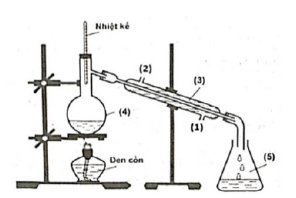 Biết nhiệt độ trong bình cầu (4) giữ ở mức 65 – 70°C, nhiệt độ trong ống sinh hàn (3) duy trì ở 25°C.
Biết nhiệt độ trong bình cầu (4) giữ ở mức 65 – 70°C, nhiệt độ trong ống sinh hàn (3) duy trì ở 25°C.
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, ethanol và ethyl acetate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:![]() a) Vai trò của ống sinh hàn (3) để ngưng tụ hơi nước vào ở (1) và nước ra ở (2).
a) Vai trò của ống sinh hàn (3) để ngưng tụ hơi nước vào ở (1) và nước ra ở (2).
b) Chất lỏng trong bình hứng (5) có ethyl acetate.
c) Nhiệt độ phản ứng ở bình cầu (4) càng cao thì phản ứng điều chế ethyl acetate xảy ra càng nhanh.
d) Dựa vào phổ hồng ngoại, không thể phân biệt được acetic acid, ethanol và ethyl acetate.
Câu 3. Al₂O₃ có nhiệt độ nóng chảy rất cao (2050°C) nên việc điện phân nóng chảy Al₂O₃ nguyên chất sẽ khó thực hiện. Hiện nay, theo công nghệ Hall-Héroult, người ta hoà tan Al₂O₃ trong cryolite (Na₃AlF₆) nóng chảy được hỗn hợp chất điện phân có nhiệt độ nóng chảy thấp hơn (khoảng gần 1000°C). Giải pháp này giúp tiết kiệm năng lượng, đồng thời tạo ra chất lỏng có tính dẫn điện tốt, nhẹ hơn Al và nổi lên phía trên lớp Al lỏng, bảo vệ Al không bị oxi hoá bởi không khí. Sơ đồ thùng điện phân được biểu diễn như hình dưới đây: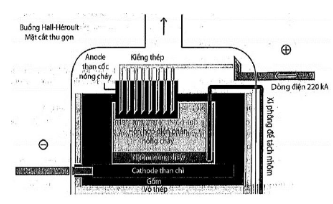
Quá trình điện phân được tiến hành với dòng điện có hiệu điện thế thấp (khoảng 5 V) và cường độ dòng điện 100 – 300 kA. Để sản xuất được 1 tấn Al cần tiêu tốn khoảng 2 tấn Al₂O₃, 50 kg cryolite, 400 kg than cốc
Cho biết: Năng lượng điện tiêu thụ theo lí thuyết, \( A_{\text{lt}} = \dfrac{U \cdot m_{\text{Al}} \cdot F}{9{,}3 \cdot 6 \cdot 10^6} \, (\text{kWh}) \)
là khối lượng Al được điều chế (gam); F là hằng số Faraday, F = 96485 C mol⁻¹, U (V) là hiệu điện thế đặt vào hai cực của bình điện phân.
a) Tại cathode xảy ra quá trình khử cation Al³⁺.
b) Cryolite không bị điện phân trong thùng điện phân.
c) Năng lượng điện tiêu thụ để sản xuất được 1 kg Al theo lí thuyết là 16 kWh.
d) Khí thoát ra ở anode chủ yếu là khí CO₂.
Câu 4. Khi con người sử dụng thức ăn chứa tinh bột, enzyme α-amylase có trong nước bọt thúc đẩy quá trình thuỷ phân tinh bột thành các phân tử nhỏ hơn gồm dextrin và maltose. Quá trình này tiếp tục ở ruột non, nơi phần lớn tinh bột bị thuỷ phân thành glucose. Glucose được hấp thụ vào máu và di chuyển đến các tế bào trong khắp cơ thể. Glucose có thể được sử dụng cho nhu cầu năng lượng hoặc có thể được chuyển đổi thành glycogen lưu trữ trong gan và cơ.
a) Khi ăn cơm, nếu nhai kĩ sẽ thấy vị ngọt vì tinh bột bị thuỷ phân thành glucose.
b) Tinh bột bị thủy phân bởi enzyme α-amylase hoặc môi trường acid.
c) Glucose chủ yếu đóng vai trò cung cấp năng lượng cho tế bào.
d) Glycogen lưu trữ trong gan và cơ, khi cần thiết có thể chuyển hoá thành glucose để cung cấp năng lượng cho cơ thể.
PHẦN III: Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Biết: E⁰(pin Ni-Ag) = 1,06 V; E⁰(Ni²⁺/Ni) = –0,26 V, thế điện cực chuẩn của cặp oxi hoá – khử Ag⁺/Ag là bao nhiêu volt (V)?
Câu 2. Docosahexaenoic acid (DHA) thuộc loại acid béo omega-n, là thành phần quan trọng của não người, vỏ não, da và võng mạc. Docosahexaenoic acid có công thức cấu tạo như sau: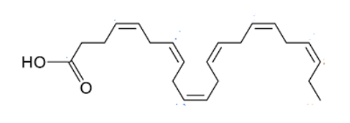 Giá trị của n là bao nhiêu?
Giá trị của n là bao nhiêu?
Câu 3. Cho các tính chất sau: (1) chất rắn kết tinh, màu trắng, (2) dễ tan trong nước, (3) có vị ngọt, (4) phản ứng với thuốc thử Tollens, (5) phản ứng với methanol có HCl xúc tác. Tính chất nào đúng với glucose? Liệt kê đáp án theo dãy số thứ tự tăng dần (ví dụ: 1234, 235,…).
Câu 4. Một số amine no, đơn chức, mạch hở, trong phân tử có phần trăm khối lượng nitrogen bằng 23,73%. Có bao nhiêu chất là đồng phân tác dụng được với dung dịch nitrous acid (HNO₂) ở nhiệt độ thích hợp sinh ra alcohol và khí nitrogen?
Câu 5. Một viên thực phẩm chức năng có khối lượng 250 mg trước nguyên tố sắt ở dạng muối Fe(II) cùng một số chất khác. Kết quả kiểm nghiệm thấy lượng Fe(II) trong viên này phản ứng vừa đủ với 8,5 mL dung dịch KMnO₄ 0,04M. Phần trăm khối lượng của nguyên tố sắt trong viên thực phẩm chức năng trên là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Câu 6. Ở điều kiện chuẩn, cần phải đốt cháy hoàn toàn bao nhiêu gam methane CH₄(g) (làm tròn đến hàng phần trăm) để cung cấp nhiệt cho phản ứng tạo 1 mol CaO bằng cách nung CaCO₃. Giả thiết hiệu suất các quá trình đều là 100%. Phương trình nhiệt của phản ứng nung vôi và đốt cháy methane như sau:
(1) CaCO₃(s) → CaO(s) + CO₂(g)
(2) CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g)
Biết nhiệt tạo thành (ΔfH⁰₂₉₈) của các chất ở điều kiện chuẩn được cho trong bảng sau: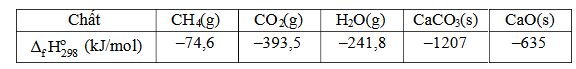
Mục đích tổ chức kỳ thi Tốt nghiệp THPT năm 2025 là gì?
Dựa trên các văn bản hướng dẫn và chỉ đạo từ Bộ Giáo dục và Đào tạo, kỳ thi Tốt nghiệp THPT năm 2025 được tổ chức nhằm đạt được những mục tiêu chính sau:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo chương trình giáo dục phổ thông mới.
– Sử dụng kết quả thi để xét công nhận tốt nghiệp THPT và làm căn cứ tuyển sinh cho các trường đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục tại các địa phương và trên toàn quốc, từ đó điều chỉnh nội dung, phương pháp dạy học trong các nhà trường phù hợp hơn với thực tiễn.
Thí sinh năm 2025 có bắt buộc phải thi môn Hóa học không?
Theo quy định hiện hành của Bộ GD&ĐT, thí sinh dự thi tốt nghiệp THPT năm 2025 phải tham gia 3 bài thi bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
Ngoài ra, thí sinh sẽ chọn một trong hai bài thi tổ hợp:
– Tổ hợp Khoa học Tự nhiên (KHTN): gồm các môn Vật lí, Hóa học, Sinh học.
– Tổ hợp Khoa học Xã hội (KHXH): gồm các môn Lịch sử, Địa lí, Giáo dục công dân (áp dụng với học sinh chương trình GDPT hiện hành).
Trong đó, môn Hóa học là một trong ba môn thành phần của bài thi tổ hợp KHTN. Tuy nhiên, thí sinh chỉ cần thi môn Hóa học nếu chọn tổ hợp KHTN – đặc biệt nếu có định hướng xét tuyển vào các ngành yêu cầu môn Hóa trong tổ hợp xét tuyển đại học hoặc cao đẳng.
Vì lý do đó, Đề thi thử tốt nghiệp THPT 2025 môn Hóa học – Đề 4 được xây dựng để hỗ trợ học sinh chọn tổ hợp KHTN ôn luyện hiệu quả, đánh giá năng lực hiện tại và nâng cao kỹ năng làm bài, chuẩn bị kỹ lưỡng cho kỳ thi chính thức.




