Đề thi thử Đại học 2025 môn Hóa học – Đề 9 là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Với mục tiêu giúp học sinh lớp 12 ôn tập hiệu quả và làm quen với cấu trúc đề thi chuẩn, đề số 9 được xây dựng sát với đề minh họa của Bộ GD&ĐT năm 2025. Nội dung đề bao quát đầy đủ các chuyên đề trọng tâm như: Sự điện li, Cân bằng hóa học, Tốc độ phản ứng, Este – Lipit, Peptit – Protein, Kim loại và hợp chất của kim loại, Đại cương hóa hữu cơ, cùng các dạng bài tập tính toán phức tạp giúp rèn luyện kỹ năng tư duy logic và xử lý dữ liệu nhanh chóng.
Những kiến thức cốt lõi cần nắm để giải đề này bao gồm:
- Phân biệt rõ các loại phản ứng hóa học và bản chất các chất.
- Vận dụng tốt các công thức tính nhanh khối lượng, nồng độ, thể tích khí.
- Nắm vững phương pháp giải bài tập đồ thị, bài tập tổng hợp vô cơ – hữu cơ.
Hãy cùng Dethitracnghiem.vn tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 – ĐỀ 9










PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn 1 phương án.
Câu 1: Nội dung: Cho phương trình hóa học của phản ứng sau:
(1) CuO + CO -(t⁰)→ Cu + CO₂
(2) 2CuSO₄ +2H₂O -(đpdd)→ 2Cu + O₂ +2H₂SO₄
(3) Fe + CuSO₄ → FeSO₄ + Cu
(4) Fe₂O₃ + 3C -(t⁰)→ 3CO + 2Fe
Số phản ứng có thể được dùng để điều chế kim loại bằng phương pháp nhiệt luyện là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 2: Kim loại nào sau đây tác dụng mạnh với nước ở nhiệt độ thường
A. Na.
B. Mg.
C. Fe.
D. Be.
Câu 3: Trong 7 loại tơ sau: tơ nylon-6,6, tơ tằm, tơ acetate, tơ capron, sợi bông, tơ enang (nylon-7), tơ visco. Số tơ thuộc loại tơ tổng hợp là
A. 3.
B. 2.
C. 4.
D. 5.
Câu 4:Thí nghiệm: glucose bị oxi hóa bởi thuốc thử Tollens. Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho khoảng 2 mL dung dịch AgNO₃ 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch dung dịch ammonia 5%, lắc đều cho đến khi kết tủa tan hết. Dung dịch thu được là thuốc thử Tollens.
Bước 3: Thêm tiếp khoảng 2 mL dung dịch glucose 2% lắc đều. Sau đó, ngâm ống nghiệm vào cốc thuỷ tinh chứa nước nóng trong vài phút.
Phát biểu nào sau đây sai?
A. Sản phẩm hữu cơ thu được sau bước 3 là ammonium gluconate.
B. Thí nghiệm trên chứng minh glucose có tính chất của polyalcohol
C. Sau bước 3, có lớp bạc (silver) kim loại bám trên thành ống nghiệm.
D. Trong phản ứng ở bước 3, glucose đóng vai trò là chất khử.
Câu 5: Nguyên tử nguyên tố P có 15 proton, 16 neutron, 15 electron được kí hiệu là
A. ¹⁶₁₅P .
B. ³¹₁₅P .
C. ³¹₁₆P .
D. ³⁰₁₆P .
Câu 6: Số lượng phối tử có trong mỗi phức chất [PtCl₄]²⁻, [Fe(CO)₅] lần lượt là
A. 4 và 5.
B. 5 và 6.
C. 2 và 5.
D. 1 và 2.
Câu 7: Tien hanh luu hoa cao su thien nhien theo ti le khoi luong giua polyisoprene va sulfur (S) tương ứng là 97: 3. Giả thiết sulfur (S) cộng vào nối đôi C=C trong polymer và cứ k mắt xích có một cầu nối-S-S -. Giá trị của k là bao nhiêu?
A. 10
B. 20
C. 30
D. 40
Câu 8: Yếu tố nào sau đây luôn luôn không làm dịch chuyển cân bằng của hệ phản ứng?
A. Nhiệt độ.
B. Áp suất.
C. Nồng độ.
D. Chất xúc tác.
Câu 9: Cho các phát biểu sau về phenol (C₆H₅OH)
(a) Phenol vừa tác dụng được với dung dịch NaOH vừa tác dụng được với Na.
(b) Phenol phản ứng được với dung dịch nước bromine tạo nên kết tủa trắng.
(c) Phenol có tính acid nhưng yếu hơn nấc thứ nhất tính acid của H₂CO₃.
(d) Phenol phản ứng được với dung dịch KHCO₃ tạo CO₂.
(e) Phenol là một alcohol thơm.
Số phát biểu đúng là
A. 2.
B. 3.
C. 4.
D. 5.
Câu 10: Methyl acrylate là một chất kích thích mạnh, có thể gây chóng mặt, đau đầu, hoa mắt và khó thở khi tiếp xúc với da hoặc hít phải. Ester này có công thức cấu tạo thu gọn là
A. CH₃COOC₂H₅.
B. CH₃COOCH₃.
C. C₂H₅COOCH₃.
D. CH₂=CHCOOCH₃.
Câu 11: CAmine nào sau đây ở trạng thái lỏng ở điều kiện thường?
A. Aniline.
B. Methylamine.
C. Ethylamine.
D. Dimethylamine.
Câu 12: Polymer thiên nhiên X được sinh ra trong quá trình quang hợp của cây xanh. Ở nhiệt độ thường, X tạo với dung dịch iodine hợp chất có màu xanh tím. Polymer X là
A. tinh bột.
B. cellulose.
C. saccharose.
D. glicogen.
Câu 13: Cho các phản ứng hóa học sau:
(a) CH₃CHO + Br₂ + H₂O → CH₃COOH + 2HBr.
(b) CH₃CHO + 2AgNO₃ + 3NH₃ + H₂O → CH₃COONH₄ + 2Ag↓ + 2NH₄NO₃.
(c) CH₃CHO + H₂ → CH₃CH₂OH.
(d) 2CH₃CHO + O₂ → 2CH₃COOH.
Số phản ứng trong đó acetaldehyde thể hiện tính khử là
A. 2.
B. 1.
C. 3.
D. 4.
Câu 14: Cho các phát biểu sau:
(a) Trong chế biến thực phẩm, người ta hydrogen hóa chất béo lỏng để được chất béo rắn.
(b) Do có chứa liên kết đôi C=C trong phân tử nên chất béo không no bị oxi hóa chậm bởi oxygen trong không khí.
(c) Phản ứng thủy phân chất béo trong môi trường acid là phản ứng thuận nghịch.
(d) Ở nhiệt độ thường, chất béo chứa nhiều gốc acid béo không no thường ở thể rắn.
Số phát biểu đúng là
A. 4.
B. 1.
C. 2.
D. 3.
Câu 15: α-amino acid là amino acid có nhóm amino gắn với carbon ở vị trí số
A. 2.
B. 4.
C. 1.
D. 3.
Câu 16: Tiến hành thí nghiệm theo các bước sau:
Bước 1: Nhỏ vài giọt aniline vào ống nghiệm chứa khoảng 10 ml nước cất, lắc đều hỗn hợp.
Bước 2: Nhỏ từ từ từng giọt acid HCl đặc vào ống nghiệm, vừa nhỏ vừa lắc đều đến khi thu được dung dịch đồng nhất.
Bước 3: Thêm từ từ từng giọt dung dịch NaOH có pha phenlphtalein vào dung dịch trên.
Cho các phát biểu sau:
a. Sau bước 1, quan sát được aniline không tan, tách thành lớp mỏng nổi lên mặt nước.
b. Sau bước 2 aniline tác dụng với HCl tạo thành muối tan trong nước.
c. Ở bước 3, khi nhỏ dung dịch NaOH có pha phenlphtalein vào thì xuất hiện màu hồng.
d. Sau bước 3, thu được dung dịch đồng nhất có màu hồng.
Số phát biểu đúng là:
A. 1.
B. 2.
C. 3.
D. 4.
Câu 17: Trong nước, thế điện cực chuẩn của kim loại Mⁿ⁺/M càng lớn thì dạng khử có tính khử (1). và dạng oxi hoá có tính oxi hoá (2). Cụm từ cần điền vào (1)và(2) lần lượt là
A. càng mạnh và càng yếu.
B. càng mạnh và càng mạnh.
C. càng yếu và càng yếu.
D. càng yếu và càng mạnh.
Câu 18: Acquy chì là một loại acquy đơn giản, gồm bản cực dương bằng PbO₂, bản cực âm bằng Pb, cả hai điện cực được đặt vào dung dịch H₂SO₄ loãng. Loại acquy này có thể sạc lại nhiều lần. Đây cũng là loại acquy được sử dụng phổ biến trên các dòng xe máy hiện nay với nhiều ưu điểm vượt trội. Nhược điểm của acquy chì là
A. dễ sản xuất, giá thành thấp.
B. gây ô nhiễm môi trường.
C. có khả năng trữ một lượng điện lớn trong bình ắc quy.
D. hoạt động ổn định.
PHẦN II. Câu hỏi trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu thí sinh chọn đúng hoặc sai.
Câu 1: Tơ, cao su, keo dán… là những vật liệu polymer có ứng dụng rộng rãi trong đời sống.
a) Keo dán là vật liệu có khả năng kết dính bề mặt của 2 vật liệu rắn với nhau mà không làm thay đổi bản chất vật liệu.
b) Vải làm từ tơ nylon-6 bền trong môi trường base hoặc môi trường acid.
c) Đoạn mạch tơ nylon-6 có khối lượng phân tử là 15000 đvC. Số lượng mắt xích trong đoạn mạch nylon-6 khoảng 133.
Chất dẻo PVC được điều chế theo sơ đồ:
CH₄ -(H=20%)→ C₂H₂ -(H=90%)→ C₂H₃Cl -(H=80%)→ PVC
Khí CH₄ chiếm 80% thể tích khí thiên nhiên, vậy từ 10.000 m³ (điều kiện chuẩn) khí thiên nhiên thì có thể điều chế được khoảng 1,45 tấn PVC.
Câu 2: Trong công nghiệp, nhôm được sản xuất từ quặng bauxite theo hai giai đoạn chính:
Giai đoạn 1: Tinh chế quặng bauxite.
Giai đoạn 2: Điện phân nóng chảy Al₂O₃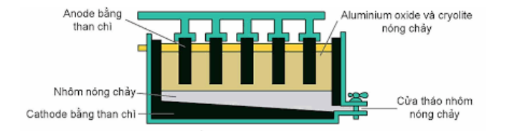
a) Thành phần chính của quặng bauxite là Al₂O₃.2H₂O.
b) Để tách được kim loại Al ra khỏi quặng người ta dùng phương pháp điện phân nóng chảy Al₂O₃.
c) Tại cathode xảy ra quá trình khử Al³⁺, tại anode xảy ra quá trình oxi hóa ion O²⁻
d) Để thu được 1,8 tấn Al tinh khiết thì cần 6,8 tấn quặng bauxite chứa 35% Al₂O₃ về khối lượng. Hiệu suất cả quá trình là 80%.
Câu 3: Nitric acid (HNO₃) là một trong ba acid chính của ngành công nghiệp hóa chất hiện đại.
a) Trong phân tử HNO₃ có 1 liên kết cho nhận.
b) HNO₃ là một acid mạnh và có tính oxi khử mạnh.
c) Trong hóa học hữu cơ, dung dịch nitric acid 68% được sử dụng để chế tạo thuốc nổ, ví dụ như trinitrotoluene(TNT).
d) Trong công nghiệp, người ta sản xuất nitric acid (HNO₃) từ ammonia theo sơ đồ chuyển hoá sau:
NH₃ -(+O₂, t⁰)→ NO -(+O₂)→ NO₂ -(+O₂, +H₂O)→ HNO₃
Để điều chế 200 000 tấn nitric acid có nồng độ 60% cần dùng 33660 tấn ammonia (Biết rằng hiệu suất của phân ứng sản xuất nitric acid theo sơ đồ trên là 96,2%).
Câu 4: Vào mùa mưa khí hậu ẩm ướt, đặc biệt ở các vùng mưa lũ dễ phát sinh một số bệnh như ghẻ nở. Người bị bệnh khi đó được khuyên nên bôi vào các vị trí ghẻ nở một loại thuốc thông dụng là DEP. Thuốc DEP có thành phần hoá học quan trọng là diethyl phtalate
a) Công thức cấu tạo thu gọn của diethyl phtalate là C₆H₄(COOC₂H₅)₂
b) Cho 1 mol diethyl phtalate tác dụng vừa đủ với dung dịch NaOH thì dùng hết 2 mol NaOH.
c) Thủy phân hoàn toàn 1 mol diethyl phtalate trong môi trường acid thu được 1 mol acid C₆H₄(COOH)₂ và 1 mol ethyl alcohol.
d) Phần trăm khối lượng nguyên tố carbon trong phân tử diethyl phtalate là 64,86%.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1: Điện phân 200 mL dung dịch CuSO₄ nồng độ x mol/L với điện cực trơ. Sau một thời gian thu được dung dịch Y vẫn còn màu xanh, có khối lượng giảm 8 g so với dung dịch ban đầu. Cho 16,8 g bột sắt vào Y, sau khi các phản ứng xảy ra hoàn toàn, thu được 12,4 g kim loại. Giá trị của x là bao nhiêu?
Câu 2: Để tráng một số lượng gương soi có diện tích bề mặt 0,35 m² với độ dày 0,1 µm người ta đun nóng dung dịch chứa 30,6 gam glucose với một lượng dung dịch silver nitrate trong ammonia. Biết khối lượng riêng của silver là 10,49 g/cm³, hiệu suất phản ứng tráng gương là 80% (tính theo glucose). Số lượng gương soi tối đa sản xuất được là (kết quả lấy phần nguyên gần nhất; cho nguyên tử khối H = 1; C = 12; Ag = 108).
Câu 3: Ở 20°C, độ tan của NaCl trong nước là 35,9 g trong 100 g nước. Ở nhiệt độ này, dung dịch NaCl bão hòa có nồng độ a%.Giá trị của a là bao nhiêu? (Làm tròn kết quả đến phần mười).
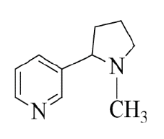
Câu 4: Nicotine là amine rất độc, có nhiều trong khói thuốc lá, cókhả năng gây tăng huyết áp và nhịp tim, gây sơ vữa động mạnh vànhvà suy giảm trí nhớ. Công thức cấu tạo của nicotine cho ở hình bên. Xác định số nguyên tử carbon trong một phân tử nicotine.
 Câu 5: Xăng sinh học E5 (chứa 5% ethanol về thể tích, còn lại là xăng, giả thiết chỉ là octane). Khi được đốt cháy hoàn toàn, 1 mol ethanol tỏa ra lượng nhiệt là 1365,0 kJ và 1 mol octane tỏa ra lượng nhiệt là 5928,7 kJ. Trung bình, một chiếc xe máy di chuyển được 1km thì cần một nhiệt lượng chuyển thành công cơ học có độ lớn là 211,8 kJ. Nếu xe máy đó đã sử dụng 4,6 lít xăng E5 ở trên thì quãng đường di chuyển được là bao nhiêu km, biết hiệu suất sử dụng nhiên liệu của động cơ là 25%; khối lượng riêng của etanol là 0,8 g/mL, của octan là 0,7 g/mL (đáp án làm tròn đến số nguyên).
Câu 5: Xăng sinh học E5 (chứa 5% ethanol về thể tích, còn lại là xăng, giả thiết chỉ là octane). Khi được đốt cháy hoàn toàn, 1 mol ethanol tỏa ra lượng nhiệt là 1365,0 kJ và 1 mol octane tỏa ra lượng nhiệt là 5928,7 kJ. Trung bình, một chiếc xe máy di chuyển được 1km thì cần một nhiệt lượng chuyển thành công cơ học có độ lớn là 211,8 kJ. Nếu xe máy đó đã sử dụng 4,6 lít xăng E5 ở trên thì quãng đường di chuyển được là bao nhiêu km, biết hiệu suất sử dụng nhiên liệu của động cơ là 25%; khối lượng riêng của etanol là 0,8 g/mL, của octan là 0,7 g/mL (đáp án làm tròn đến số nguyên).
Câu 6: Cho các phức chất: [Co(NH₃)₆]Cl₃, [Cr(H₂O)₆]Cl₃, [Ni(CO)₄], Na[BF₄], FH₂⁺, K₄[Fe(CN)₆], Fe(CO)₅. Có bao nhiêu phức ion?
Mục đích tổ chức kỳ thi Tốt nghiệp THPT năm 2025 là gì?
Căn cứ theo các văn bản chỉ đạo và hướng dẫn của Bộ Giáo dục và Đào tạo, kỳ thi Tốt nghiệp THPT năm 2025 được tổ chức nhằm các mục đích chính sau:
– Đánh giá kết quả học tập của học sinh sau 12 năm theo chương trình giáo dục phổ thông mới.
– Sử dụng kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh vào các trường đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục tại các địa phương cũng như trên toàn quốc, từ đó làm cơ sở điều chỉnh nội dung và phương pháp giảng dạy trong nhà trường.
Thí sinh thi Tốt nghiệp THPT năm 2025 có bắt buộc phải thi môn Hóa học không?
Theo quy định hiện hành của Bộ GD&ĐT, thí sinh dự thi Tốt nghiệp THPT năm 2025 bắt buộc phải tham gia 3 bài thi: Toán, Ngữ văn và Ngoại ngữ.
Ngoài ra, thí sinh sẽ chọn một trong hai bài thi tổ hợp:
– Tổ hợp Khoa học Tự nhiên (KHTN): gồm các môn Vật lí, Hóa học, Sinh học.
– Tổ hợp Khoa học Xã hội (KHXH): gồm các môn Lịch sử, Địa lí, Giáo dục công dân (áp dụng cho học sinh học chương trình GDPT hiện hành).
Trong tổ hợp KHTN, môn Hóa học là một trong ba môn thi thành phần. Tuy nhiên, thí sinh không bắt buộc phải thi môn Hóa học, trừ khi chọn tổ hợp KHTN để xét tốt nghiệp hoặc dùng kết quả thi xét tuyển vào các ngành học có yêu cầu môn Hóa.
Chính vì vậy, Đề thi thử tốt nghiệp THPT 2025 môn Hóa học – Đề 9 là tài liệu ôn tập hữu ích dành cho các thí sinh chọn tổ hợp KHTN. Đề giúp học sinh củng cố kiến thức, kiểm tra năng lực hiện tại và rèn luyện kỹ năng làm bài để tự tin bước vào kỳ thi chính thức.




