Đề thi thử Đại học 2025 môn Hóa học – Sở GD Hải Dương là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT thuộc chương trình Đề thi vào Đại học.
Đề được xây dựng sát với cấu trúc đề minh họa 2025 của Bộ GD&ĐT, bao quát đầy đủ các chuyên đề trọng tâm như: este – lipit, amino axit – protein, polime, kim loại, phản ứng vô cơ – hữu cơ và các dạng bài tính nhanh.
Tài liệu này là công cụ hữu hiệu để học sinh rèn kỹ năng, làm quen áp lực thời gian và kiểm tra mức độ sẵn sàng cho kỳ thi.
Hãy cùng Dethitracnghiem.vn khám phá và thử sức ngay với đề thi này!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 SỞ GD HẢI DƯƠNG
Cho nguyên tử khối của các nguyên tố: H=1; C=12; N=14; O=16; Na=23; Cl=35 ,5; Br =80; Ag=108
PHẦN I. Trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.





Câu 1: Trong phân tử chất nào sau đây có 1 nhóm amino (-NH2) và 2 nhóm carboxyl (-COOH)?
A. Alanine.
B. Glutamic acid.
C. Lysine.
D. Formic acid.
Câu 2: Số nguyên tử carbon trong phân tử saccharose là:
A. 10.
B. 12.
C. 5.
D. 12.
Câu 3: Cho dãy các chất sau: saccharose, glucose, fructose, cellulose, tinh bột. Số chất tham gia phản ứng thủy phân trong môi trường acid là
A. 1.
B. 4.
C. 5.
D. 4.
Câu 4: Tên gọi của este CH3COOCH3 là
A. Methyl acetate.
B. Ethyl acetate.
C. Ethyl formate.
D. Methyl formate.
Câu 5: Tên gọi của polymer có công thức -(CH2 -CHCl)-n là
A. polyethylene.
B. polystyrene.
C. poly(vinyl chloride).
D. poly(methyl methacrylate).
Câu 6: Glucose là một trong hai loại monosaccharide phổ biến trong đời sống. Glucose có dạng mạch hở và hai dạng mạch vòng chuyển hóa qua lại lẫn nhau:
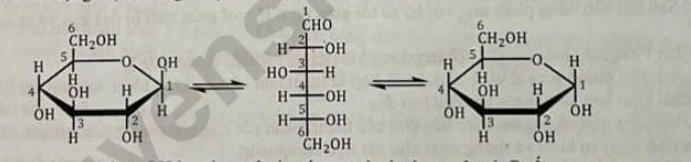 Ở dạng mạch vòng, nhóm -OH hemiacetal của Glucose ở vị trí nguyên tử C số:
Ở dạng mạch vòng, nhóm -OH hemiacetal của Glucose ở vị trí nguyên tử C số:
A. 5.
B. 1.
C. 6.
D. 2.
Câu 7: Chất nào sau đây thuộc loại amine bậc 3?
A. (CH3)3N.
B. CH3-NH2.
C. CH3-NH-CH3.
D. C2H5-NH2.
Câu 8: Trong phản ứng: NH3 + H2O <=> NH4+ + OH-, những chất (ion) nào đóng vai trò là acid theo thuyết Brønsted – Lowry?
A. H2O và OH-.
B. H2O và OH-.
C. NH3 và OH-.
D. NH3 và NH4+.
Câu 9: Công thức của tristearin là
A. (C17H33COO)3C3H5.
B. C15H31COOH.
C. (C17H35COO)3C3H5.
D. C15H31COOC3H5.
Câu 10: Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trong đời sống: kích thích quả mau chín, điều chế nhựa làm sản phẩm gia dụng,… Phản ứng hóa học của ethylene với dung dịch Br2 như sau:
CH2 = CH2 + Br2 -> CH2Br – CH2Br
Cơ chế của phản ứng trên xảy ra như sau:
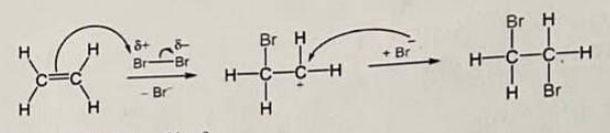 Nhận định nào sau đây không đúng?
Nhận định nào sau đây không đúng?
A. Giai đoạn 1, liên kết đôi phân tửng với tác nhân Br tạo thành phân tử mang điện dương.
B. Phản ứng trên thuộc loại phản ứng cộng.
C. Hiện tượng của phản ứng là dung dịch bromine bị mất màu.
D. Giai đoạn 2, phân tử mang điện dương kết hợp với anion Br tạo thành sản phẩm.
Câu 11: Chất nào sau đây được sử dụng làm chất giặt rửa tổng hợp
A. CH3COOH.
B. C15H31COOH.
C. C12H25OSO3Na.
D. C15H31COONa.
Câu 12: Phát biểu nào sau đây sai?
A. Khi nhỏ acid HNO3 đặc vào lòng trắng trứng thấy có kết tủa màu vàng.
B. Tất cả các protein đều tan được trong nước tạo thành dung dịch keo.
C. Liên kết của nhóm CO với NH giữa hai đơn vị α-amino acid được gọi là liên kết peptide.
D. Khi cho Cu(OH)2/OH- vào dung dịch lòng trắng trứng xuất hiện màu tím đặc trưng.
Câu 13: Poly(vinyl chloride), có phân tử khối là 35 000. Số mắt xích của polymer này là
A. 406.
B. 600.
C. 560.
D. 460.
Câu 14: Khí SO2 là một trong các chất chủ yếu gây ô nhiễm môi trường nhưng khi được sử dụng đúng mục đích sẽ có nhiều ứng dụng: dùng để sản xuất sulfuric acid, tẩy trắng bột giấy, chống nấm mốc cho lương thực, thực phẩm,… Khi dẫn khí SO2 vào dung dịch KMnO4 màu tím nhận thấy dung dịch bị mất màu vì xảy ra phản ứng hóa học sau:
SO2 + KMnO4 + H2O -> K2SO4 + H2SO4 + MnSO4
Phát biểu nào sau đây đúng?
A. SO2 được dùng để tẩy trắng bột giấy, khử màu trong sản xuất đường,…
B. SO2 là một trong các tác nhân làm ô nhiễm khí quyển, gây mưa acid và viêm đường hô hấp ở người.
C. Trong phản ứng đã cho, SO2 là chất khử.
D. Sau khi cân bằng phản ứng với hệ số tối giản thì tỉ lệ mol giữa chất bị oxi hoá và chất bị khử là 2:1.
Câu 15: Phát biểu nào sau đây không đúng khi nói về vật liệu composite?
A. Vật liệu composite là vật liệu được tổng hợp từ hai nhiều vật liệu khác nhau, tạo nên vật liệu mới có tính chất kém hơn so với các vật liệu ban đầu.
B. Vật liệu nền có vai trò đảm bảo cho các thành phần cốt của composite liên kết với nhau nhằm tạo ra một nguyên khối và thống nhất cho vật liệu composite.
C. Thành phần vật liệu composite gồm vật liệu nền (chủ yếu là polymer) và vật liệu cốt (sợi hoặc hạt).
D. Vật liệu cốt có vai trò đảm bảo cho composite có được các đặc tính cơ học cần thiết.
Câu 16: Điểm chớp cháy là nhiệt độ thấp nhất ở áp suất khí quyển mà một chất lỏng hoặc vật liệu dễ bay hơi tạo thành lượng hơi đủ bốc cháy trong không khí khi tiếp xúc nguồn lửa.Điểm chớp cháy được sử dụng để phân biệt chất lỏng dễ cháy với chất lỏng có thể gây cháy:Chất lỏng có điểm chớp cháy <37,8 độ C gọi là chất lỏng dễ cháy. Chất lỏng có điểm chớp cháy >37,8 độ C gọi là chất lỏng có thể gây cháy.Cho bảng số liệu sau: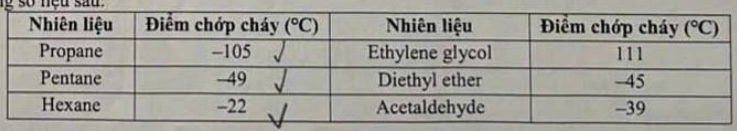
 Số chất lỏng dễ cháy trong bảng trên là.
Số chất lỏng dễ cháy trong bảng trên là.
A. 9.
B. 7.
C. 6.
D. 8.
Câu 17: Nitrobenzene được ứng dụng trong nông nghiệp để tổng hợp chất kích thích tăng trưởng thực vật, kích thích cây ra hoa. Phản ứng nitro hóa benzene trong phòng thí nghiệm được thực hiện như sau:
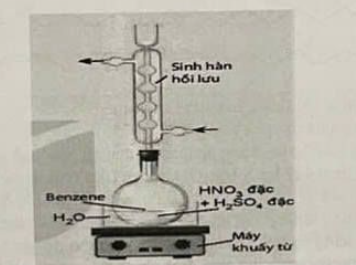 Bước 1: Cho cồn từ vừa đủ dung dịch tích 250 mL, thêm khoảng 30 mL H2SO4 đặc, làm lạnh trong chậu nước đá rồi thêm từ từ vào khoảng 30 mL HNO3 đặc, sau đó thêm tiếp khoảng 10 mL benzene và lắp sinh hàn hồi lưu. Đun cách thủy hỗn hợp phản ứng trên bếp từ đến 80 °C trong khoảng 60 phút.
Bước 1: Cho cồn từ vừa đủ dung dịch tích 250 mL, thêm khoảng 30 mL H2SO4 đặc, làm lạnh trong chậu nước đá rồi thêm từ từ vào khoảng 30 mL HNO3 đặc, sau đó thêm tiếp khoảng 10 mL benzene và lắp sinh hàn hồi lưu. Đun cách thủy hỗn hợp phản ứng trên bếp từ đến 80 °C trong khoảng 60 phút.
Bước 2: Để nguội rồi cho hỗn hợp vào phễu chiết, quan sát thấy chất lỏng tách thành hai lớp.
Bước 3: Chiết lấy lớp chất lỏng phía trên, thêm khoảng 100 mL nước lạnh vào phễu chiết để rửa acid.
Nhận định nào sau đây đúng?
A. Nên thay benzene bằng toluene thì phản ứng xảy ra khó khăn hơn benzene.
B. Phản ứng xảy ra trong giai đoạn là phản ứng cộng nhóm nitro vào vòng benzene.
C. Sau bước 2, thu được chất lỏng màu vàng, nằm ở phần trên của phễu chiết.
D. Sau bước 2, chất lỏng trong phễu chiết tách thành 2 lớp, lớp trên là sản phẩm phản ứng, lớp dưới là dung dịch hỗn hợp 2 acid.
Câu 18: Xà phòng hóa hoàn toàn 3,7 gam HCOOC2H5 bằng một lượng vừa đủ dung dịch NaOH đun nóng. Cô cạn dung dịch sau phản ứng, thu được m gam muối khan. Giá trị của m là
A. 5,2.
B. 3,2.
C. 3,4.
D. 4,8.
PHẦN II. Trắc nghiệm tự chấm điểm. Thí sinh chỉ trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1: Cho carbohydrate X có cấu tạo như sau:
(Hình vẽ cấu tạo carbohydrate X – Saccharose)
Thủy phân hoàn toàn X, thu được chất Y. Chất Y có trong máu người người trưởng thành, khỏe mạnh vào lúc đói với nồng độ khoảng 4,4 – 7,2 mmol/L (hay 80 – 130 mg/dL).
Cho các phát biểu sau:
a) X có công thức phân tử (C6H10O5)n, mỗi mắt xích của X chứa 5 nhóm -OH.
b) Chất Y có phản ứng lên men, tạo thành ethanol hoặc lactic acid.
c) Chất X có khả năng phản ứng với ethanol khi có mặt HCl khan làm xúc tác.
d) Ethanol có thể được sản xuất từ carbohydrate X. Loại ethanol này được dùng để sản xuất xăng E5 (chứa 5% ethanol về thể tích). Lượng ethanol thu được từ 1 tấn mùn cưa (chứa 50% chất X, phần còn lại là chất trơ) có thể pha chế được 4262 lít xăng E5. Biết hiệu suất quá trình sản xuất ethanol (từ X) là 60% và ethanol có khối lượng riêng là 0,8 gam.mL-1 (kết quả làm tròn đến hàng đơn vị).
Câu 2: Triglyceride X có công thức cấu tạo như hình sau:
(Hình vẽ cấu tạo triglyceride X)
a) Acid béo có gốc kí hiệu (3) thuộc loại acid béo omega-6.
b) Phần trăm khối lượng của oxygen trong X là 8,43%.
c) Các gốc của acid béo trong phân tử X đều có cấu hình cis-.
d) Hydrogen hóa hoàn toàn 427 kg X bằng hydrogen (dư) ở nhiệt độ cao và áp suất cao, Ni xúc tác (hiệu suất 90%) thu được 388 kg chất béo rắn. (kết quả làm tròn đến hàng đơn vị).
e) X có khả năng phản ứng với dung dịch Br2 theo tỉ lệ mol 1 : 1.
f) X không tan trong nước lạnh nhưng tan nhiều trong hexane.
Câu 3: Tyrosine là một trong những loại amino acid cần thiết và có thể bổ sung cho cơ thể thông qua các thực phẩm ăn uống hàng ngày. Tyrosine làm tăng mức độ chất dẫn truyền tế bào thần kinh như dopamine, adrenaline và norepinephrine giúp điều chỉnh tâm trạng, cải thiện trí nhớ, giúp tỉnh táo đầu óc và tăng khả năng tập trung. Cơ thể có thể tổng hợp tyrosine từ các loại thực phẩm như thịt, cá, trứng, sản phẩm từ sữa, đậu, các loại hạt, yến mạch và lúa mỳ. Tyrosine có cấu tạo như sau:
(Hình vẽ cấu tạo Tyrosine)
a) Tyrosine có công thức phân tử là C9H11NO3.
b) Tyrosine tác dụng với dung dịch KOH tối đa theo tỉ lệ mol là 1 : 1.
c) Tyrosine có thể được dùng tới 150 mg trên mỗi kg trọng lượng cơ thể, liên tục hàng ngày trong vòng 3 tháng mà không gây ảnh hưởng đến sức khỏe. Nếu bạn nặng 60kg, bạn có thể bổ sung tới 10 gam tyrosine/ngày.
Câu 4: Cho 1 mol tyrosine phản ứng với lượng dư dung dịch Br2/CCl4 thu được kết tủa có khối lượng là 339 gam.
Cho khoảng 2 ml ethanol và 2 ml acetic acid tuyệt đối vào ống nghiệm, lắc đều hỗn hợp.
Thêm khoảng 1 ml dung dịch H2SO4 đặc, lắc nhẹ để các chất trộn đều với nhau.
Kẹp ống nghiệm vào kẹp gỗ rồi đặt ống nghiệm vào cốc nước nóng (khoảng 60 °C – 70 °C) trong khoảng 5 phút, thỉnh thoảng lắc đều hỗn hợp. Sau đó lấy ống nghiệm ra khỏi cốc nước nóng, để nguội hỗn hợp rồi rót sang ống nghiệm khác chứa 5 ml dung dịch muối ăn bão hòa rồi thì thấy chất lỏng trong ống nghiệm tách thành hai lớp, lớp trên có mùi thơm đặc trưng.
Phản ứng xảy ra trong thí nghiệm theo phương trình hoá học sau:
CH3COOH + C2H5OH <=> CH3COOC2H5 + H2O (1); Kc = 4
Ghi phổ hồng ngoại của hai chất tham gia phản ứng trong 2 hình không tương ứng dưới đây:
(Hình vẽ phổ IR của 2 chất)
Mục đích tổ chức kỳ thi Đại học năm 2025 là gì?
Căn cứ theo quy chế hiện hành của Bộ Giáo dục và Đào tạo và các văn bản hướng dẫn tổ chức kỳ thi Đại học năm 2025, mục đích của kỳ thi là:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo yêu cầu của chương trình giáo dục phổ thông.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục của địa phương và cả nước, làm cơ sở điều chỉnh nội dung, phương pháp dạy học trong nhà trường.
Thí sinh thi Đại học năm 2025 có bắt buộc thi môn Hóa học không?
Theo quy định hiện hành của Bộ Giáo dục và Đào tạo và hướng dẫn tổ chức kỳ thi tốt nghiệp Đại học năm 2025, thí sinh dự thi phải thực hiện như sau:
– Thi 3 môn bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
– Ngoài ra, thí sinh phải chọn một trong hai bài thi tổ hợp: Khoa học Tự nhiên (gồm các môn Vật lí, Hóa học, Sinh học) hoặc Khoa học Xã hội (gồm các môn Lịch sử, Địa lí, Giáo dục công dân – dành cho học sinh học chương trình giáo dục phổ thông).
Trong số các môn thi, Hóa học là một trong ba môn thuộc bài thi tổ hợp Khoa học Tự nhiên, thí sinh chỉ phải thi môn Hóa học nếu chọn tổ hợp này, không phụ thuộc vào mục đích xét tuyển đại học.
Như vậy, kỳ thi Đại học năm 2025 không bắt buộc thí sinh phải thi môn Hóa học, việc thi môn này phụ thuộc vào lựa chọn bài thi tổ hợp của thí sinh.




