Đề thi thử Đại học 2025 môn Hóa học – Sở GD Hưng Yên là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT thuộc chương trình Đề thi vào Đại học.
Đề bám sát cấu trúc đề minh họa 2025 của Bộ GD&ĐT, bao quát các chuyên đề trọng tâm như: este – lipit, amino axit – protein, polime, đại cương kim loại, phản ứng hóa học và bài toán bảo toàn. Đây là tài liệu luyện tập hiệu quả, giúp học sinh củng cố kiến thức, nâng cao kỹ năng giải nhanh và làm quen với dạng đề chuẩn.
Hãy cùng Dethitracnghiem.vn khám phá và luyện tập đề thi này ngay bây giờ!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 SỞ GD HƯNG YÊN



Tuyệt vời! Dưới đây là toàn bộ nội dung đề thi được chép lại từ hình ảnh, định dạng chuẩn và đánh dấu đáp án trắc nghiệm đúng theo yêu cầu.
SỞ GIÁO DỤC VÀ ĐÀO TẠO HƯNG YÊN
ĐỀ THI CHÍNH THỨC
(Đề thi gồm 04 trang)
KỲ THI TỐT NGHIỆP THPT NĂM 2025
Môn thi: HOÁ HỌC
Thời gian: 50 phút (không kể thời gian giao đề)
Họ tên thí sinh: ………………………………………………………..
Số báo danh: …………………………………………………………..
Mã đề thi: 0303
Cho biết nguyên tử khối: Li = 7, Na = 23, K = 39, Mg = 24, Ca = 40, Ba = 137, Al = 27, Fe = 56, Zn = 65, Cu = 64, Ag = 108, H = 1, C = 12, N = 14, O = 16, P = 31, S = 32, Cl = 35,5, Br = 80, I = 127.
Phần I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Một chất X có công thức phân tử là C₃H₈O. Chất X làm mất màu nước bromine, tác dụng với Na. Sản phẩm oxi hóa X bởi CuO không phải là aldehyde. Vậy X là
A. 2-methylpropan-1-ol.
B. but-3-en-2-ol.
C. butan-2-ol.
D. but-3-en-1-ol.
Câu 2. Propyl acetate là ester có mùi đặc trưng của quả lê. Công thức cấu tạo của propyl acetate là
A. CH₃COOCH₂CH₂CH₃.
B. CH₃CH₂COOCH₂CH₃.
C. CH₃COOCH₂CH₃.
D. CH₃CH₂COOCH₂CH₂CH₃.
Câu 3. Mì chính là muối monosodium glutamate. Cho biết phân tử khối của mì chính là bao nhiêu?
A. 191.
B. 190.
C. 169.
D. 147.
Câu 4. Erythrosine (E127 hay Red No.3) là chất màu tổng hợp dễ tan trong nước, thường được sử dụng làm chất tạo màu đỏ hồng cho các loại thực phẩm như bánh kẹo, xúc xích, kem, nước giải khát. Tuy được cấp phép sử dụng nhiều năm nay nhưng các nghiên cứu gần đây cũng chỉ ra rằng chất này có tác động không tốt cho sức khỏe người sử dụng nên cần hạn chế, nhất là trẻ nhỏ. Biết Red No.3 có công thức cấu tạo như hình dưới đây (phân tử chứa 4 nguyên tử iodine):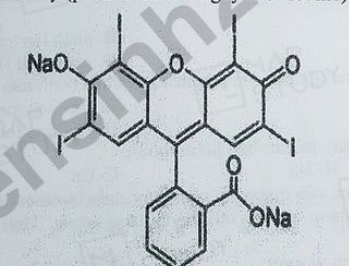 Phần trăm về khối lượng của iodine trong erythrosine là
Phần trăm về khối lượng của iodine trong erythrosine là
A. 9,99%.
B. 15,23%.
C. 57,73%.
D. 27,27%.
Câu 5. Phần trăm khối lượng của nguyên tố oxygen trong 1 phân tử glucose là
A. 44,41%.
B. 51,43%.
C. 49,38%.
D. 53,33%.
Câu 6. Polymer nào sau đây được sử dụng làm chất dẻo?
A. Polyisoprene.
B. Polyacrylonitrile.
C. Polypeptide.
D. Polyethylene.
Câu 7. Để hàn các vết đứt gãy trên đường ray xe lửa, người ta sử dụng hỗn hợp gồm Al và Fe₂O₃ theo tỉ lệ mol tương ứng 2 : 1. Khi tiến hành hàn đường ray bằng hỗn hợp trên xảy ra phản ứng hóa học:
2Al(r) + Fe₂O₃(r) → Al₂O₃(r) + 2Fe(r)
Biết nhiệt tạo thành chuẩn của Fe₂O₃(r) và Al₂O₃(r) lần lượt là -826 kJ/mol và -1666 kJ/mol, hiệu suất phản ứng đạt 95%. Nhiệt lượng tỏa ra (kJ) khi dùng 100 gam hỗn hợp trên là
A. 420.
B. 798.
C. 199.
D. 399.
Câu 8. Xét phản ứng hoá học giữa hai cặp oxi hoá – khử của kim loại:
R²⁺ + 2M → R + 2M²⁺ và R²⁺/R lẫn lượt là X (V) và Y (V). Nhận biết nào sau đây đúng?
A. X > Y.
B. X < Y.
C. 2X = Y.
D. X = Y.
Câu 9. Chất nào sau đây là ethylamine?
A. CH₃ – NH – CH₂ – CH₃.
B. CH₃-CH₂-NH₂.
C. C₂H₅ – NH₂.
D. (CH₃)₂NH.
Câu 10. Công thức cấu tạo thu gọn của formaldehyde là
A. CH₃CHO.
B. HCOOH.
C. CH₂=CHCHO.
D. HCHO.
Câu 11. Trong trồng trọt, không nên sử dụng phân đạm ammonium nitrate (NH₄NO₃) cùng với vôi sống (CaO) vì
A. làm thất thoát nitrogen do giải phóng khí NH₃.
B. tạo ra hợp chất không tan trong đất.
C. làm giảm khả năng hấp thu dinh dưỡng của cây trồng.
D. làm thất thoát nitrogen dưới dạng khí N₂.
Câu 12. Cấu hình electron nguyên tử lớp ngoài cùng của nguyên tử kim loại kiềm là
A. ns².
B. ns¹np¹.
C. ns¹.
D. ns²np¹.
Câu 13. Cho các phát biểu sau:
a) Sử dụng xà phòng để giặt quần áo trong nước cứng sẽ làm vải nhanh mục.
b) Nếu nhỏ dung dịch I₂ vào lát cắt củ khoai mì thì xuất hiện màu đỏ.
c) Khi nấu canh cua, hiện tượng riêu cua nổi lên trên là do sự đông tụ protein.
d) Một số ester có mùi thơm được dùng làm chất tạo hương trong sản xuất công nghiệp.
e) Tái làm từ nylon-6,6 bền trong nước xà phòng có tính kiềm.
Số phát biểu đúng là
A. 3.
B. 5.
C. 4.
D. 2.
Câu 14. Vu mùa lúa vừa qua, năng suất lúa của gia đình bạn giảm sút do đất bị chua. Để cải tạo đất chua, gia đình bạn nên sử dụng
A. vôi.
B. phân lân superphosphate.
C. phân đạm urea.
D. phân kali (KCl).
Câu 15. Điện phân CaCl₂ nóng chảy, ở cathode xảy ra quá trình nào?
A. Khử ion Ca²⁺.
B. Oxi hoá ion Ca²⁺.
C. Khử ion Cl⁻.
D. Oxi hoá ion Cl⁻.
Câu 16. Kim loại nào sau đây là kim loại kiềm thổ?
A. Ca.
B. Na.
C. Cu.
D. Ag.
Câu 17. Glucose là sản phẩm của quá trình phân huỷ carbohydrate, là loại đường đơn giản mà các tế bào trong cơ thể có thể dễ dàng chuyển đổi thành năng lượng. Tính chất vật lý nào sau đây không phải của glucose?
A. Dễ tan trong nước và có vị ngọt.
B. Ít ngọt hơn fructose.
C. Chất kết tinh không màu.
D. Chất rắn màu vàng.
Câu 18. Kim loại X được sử dụng trong sản xuất nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
A. Hg.
B. W.
C. Pb.
D. Cr.
Phần II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
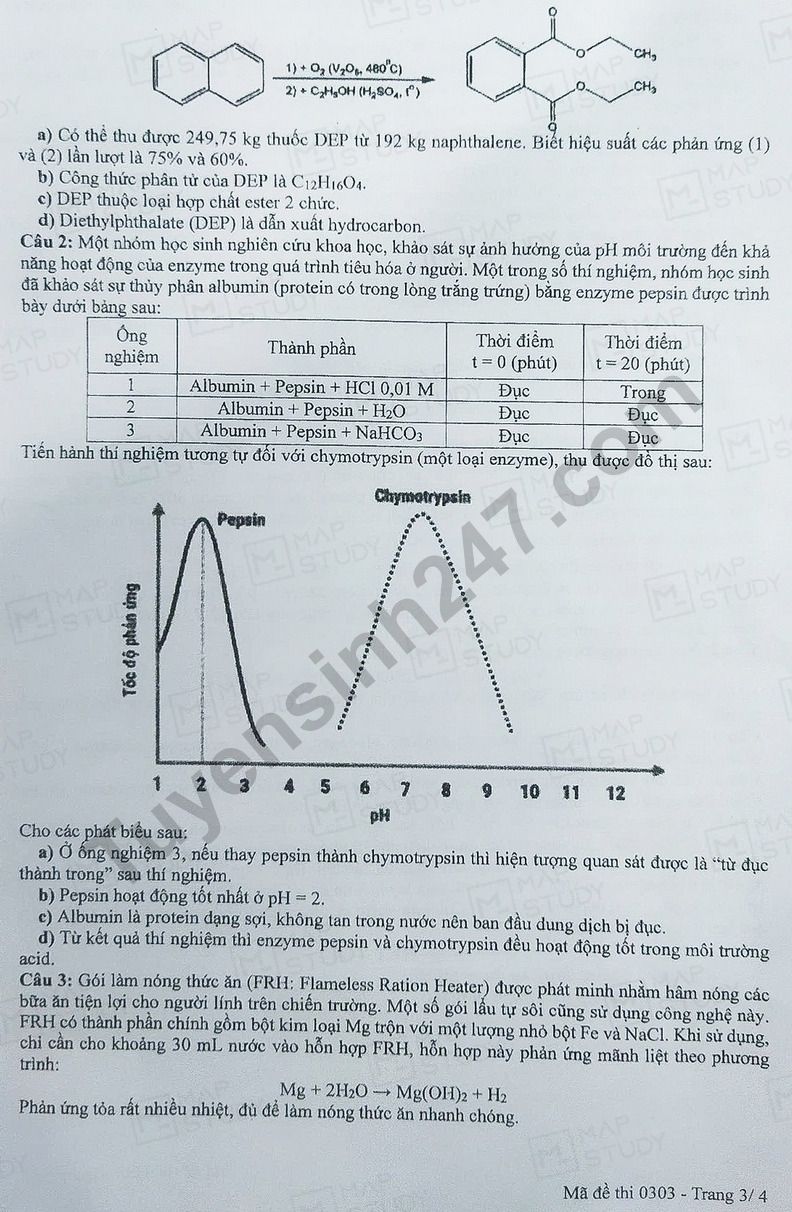
Câu 1. Diethyl phthalate (DEP) là chất lỏng không màu, có vị đắng và mùi khó chịu được dùng để sản xuất thuốc diệt côn trùng bảo vệ cho vật nuôi. Từ naphthalene điều chế DEP theo 2 giai đoạn như sau: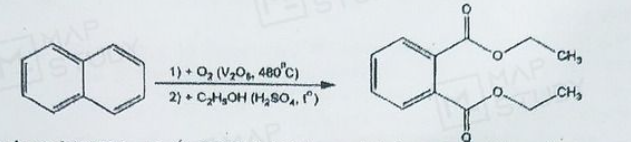
a) Có thể thu được 249,75 kg thuốc DEP từ 192 kg naphthalene. Biết hiệu suất cả quá trình phản ứng (1) và (2) lần lượt là 75% và 60%.
b) Công thức phân tử của DEP là C₁₂H₁₄O₄.
c) DEP thuộc loại hợp chất ester 2 chức.
d) Diethyl phthalate (DEP) là dẫn xuất hydrocarbon.
Câu 2. Một nhóm học sinh nghiên cứu khoa học khảo sát sự ảnh hưởng của pH môi trường đến khả năng hoạt động của enzyme trong quá trình tiêu hóa ở người. Một trong số thí nghiệm, nhóm học sinh đã khảo sát sự thủy phân albumin (protein có trong lòng trắng trứng) bằng enzyme pepsin được trình bày dưới bảng sau:
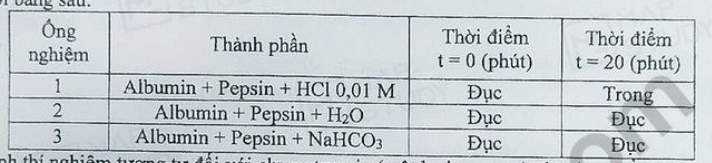
Tiến hành thí nghiệm tương tự đối với chymotrypsin (một loại enzyme), thu được đồ thị sau:
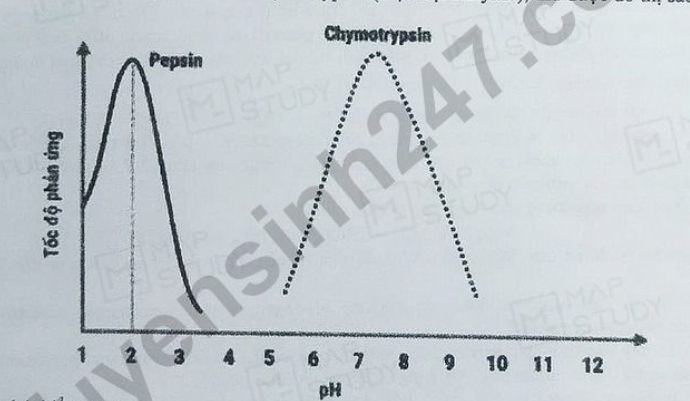
Cho các phát biểu sau:
a) Ở ống nghiệm 3, nếu thay pepsin thành chymotrypsin thì hiện tượng quan sát được là “từ đục thành trong” sau thí nghiệm.
b) Pepsin hoạt động tốt nhất ở pH = 2.
c) Albumin là protein dạng sợi, không tan trong nước nên ban đầu dung dịch bị đục.
d) Từ kết quả thí nghiệm thì enzyme pepsin và chymotrypsin đều hoạt động tốt trong môi trường acid.
Câu 3. Gói làm nóng thức ăn (FRH: Flameless Ration Heater) được phát minh nhằm làm nóng các bữa ăn tiện lợi cho người lính trên chiến trường. Một số gói lẩu tự sôi cũng sử dụng công nghệ này. FRH có thành phần chính gồm bột kim loại Mg trộn với một lượng nhỏ bột Fe và NaCl. Khi sử dụng, chỉ cần cho khoảng 30 mL nước vào hỗn hợp FRH, hỗn hợp này phản ứng mạnh liệt theo phương trình:
Mg + 2H₂O → Mg(OH)₂ + H₂
Phản ứng tỏa rất nhiều nhiệt, đủ để làm nóng thức ăn nhanh chóng.
Biết enthalpy tạo thành chuẩn của Fe₂O₃(s) và Al₂O₃(s) lần lượt là -826 kJ/mol và -1666 kJ/mol, hiệu suất phản ứng đạt 95%. Nhiệt lượng tỏa ra (kJ) khi dùng 100 gam hỗn hợp trên là -928,4 kJ/mol⁻¹ và -285,8 kJ mol⁻¹.
a) Một gói FRH trên có khối lượng 180 gam súp từ 30 °C lên 100 °C. Biết rằng nhiệt dung của súp là 4,2 J g⁻¹ °C⁻¹, giả sử gói súp chỉ nhận được 50% lượng nhiệt tỏa ra, phần nhiệt còn lại làm nóng các vật dụng khác và thất thoát vào môi trường.
b) Magnesium là kim loại có tính khử mạnh.
c) Một gói FRH chứa khoảng 8 gam hỗn hợp (Mg 90%, Fe 4% và NaCl 4% về khối lượng) có thể tỏa ra tối đa 642,6 kJ.
d) Khi cho nước vào hỗn hợp FRH có xảy ra quá trình ăn mòn điện hoá học.
Câu 4. Tại nhà máy giấy Bãi Bằng có xưởng sản xuất xút – chlorine với công suất lớn nhất trong cả nước bằng phương pháp điện phân dung dịch NaCl với anode làm bằng than chì và cathode làm bằng sắt, giữa hai điện cực có màng ngăn xốp để ngăn không cho Cl₂ tiếp xúc với OH⁻. Xút được dùng cho việc nấu bột giấy, chlorine dùng cho việc tẩy trắng bột giấy. Nước muối đi vào thùng điện phân có hàm lượng 316 g/L. Dung dịch thu được sau điện phân có chứa sodium hydroxide với hàm lượng 100 g/L. Giả sử muối ăn là tinh khiết, thể tích dung dịch điện phân không thay đổi.
a) Hiệu suất chuyển hoá muối trong thùng điện phân 46,28%. (Kết quả làm tròn đến hàng phần trăm).
b) Hàm lượng muối ăn còn lại sau điện phân là 146,25 g/L.
c) Nếu không có màng ngăn giữa hai điện cực thì sản phẩm thu được nước Javen.
d) Tại anode thu được H₂, tại cathode thu được Cl₂.
Phần III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Trên thế giới, kẽm (zinc) được sản xuất chủ yếu từ quặng zinc blende có thành phần chính là ZnS. Một nhà máy luyện kim kẽm sản xuất Zn từ 60 tấn quặng zinc blend (chứa 80% ZnS về khối lượng, còn lại là tạp chất không chứa kẽm) với hiệu suất cả quá trình đạt 90% theo các giai đoạn:
Đốt quặng zinc blende: 2ZnS(s) + 3O₂(g) → 2ZnO(s) + 2SO₂(g) (1)
Khử zinc oxide ở nhiệt độ cao bằng than cốc: ZnO(s) + C(s)→Zn(g) + CO(g) (2)
Toàn bộ lượng kẽm tạo ra được đúc thành thanh kẽm đặc hình hộp chữ nhật: Chiều dài 120 cm, chiều rộng 20 cm và chiều cao 15 cm. Biết khối lượng riêng của kẽm là 7,14 g/cm³. Giá trị xấp xỉ của khối lượng kẽm thu được theo tính toán là bao nhiêu kg?
Câu 2. Xét phản ứng trong quá trình tạo ra NO₂ nhiệt:
2NO(g) + O₂(g)→2NO₂(g)ΔH298 = 180,6 kJ
Nhiệt tạo thành chuẩn của NO(g) là a kJ/mol? Giá trị của a là? (Kết quả làm tròn đến hàng phần mười).
Câu 3. Cho các chất: glucose, amylose, fructose, glycogen, maltose, saccharose, cellulose. Có bao nhiêu chất là polysaccharide?
Câu 4. Cho dãy các chất sau: Tripalmitin, aminoacetic acid, Ala-Gly-Glu, ethyl propionate. Có bao nhiêu chất trong dãy có phản ứng với dung dịch NaOH (đun nóng)?
Câu 5. Cho các polymer sau: PVC, PPF, cao su buna-N, tơ nylon-6, tơ nylon-6,6, cao su buna-S. Có bao nhiêu polymer có thể được điều chế từ phản ứng trùng ngưng?
Câu 6. Phân tích một mẫu nước cứng thấy có chứa các ion: Ca²⁺, Mg²⁺, Cl⁻, HCO₃⁻; trong đó nồng độ Cl⁻ là 0,006M và của HCO₃⁻ là 0,01M. Cần lấy bao nhiêu ml dung dịch Na₂CO₃ 0,2M để chuyển 10 lít nước cứng trên thành nước mềm? Coi nước mềm là nước không chứa các ion Ca²⁺, Mg²⁺. (Kết quả làm tròn đến hàng đơn vị).
Mục đích tổ chức kỳ thi Đại học năm 2025 là gì?
Căn cứ theo quy chế hiện hành của Bộ Giáo dục và Đào tạo và các văn bản hướng dẫn tổ chức kỳ thi Đại học năm 2025, mục đích của kỳ thi là:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo yêu cầu của chương trình giáo dục phổ thông.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục của địa phương và cả nước, làm cơ sở điều chỉnh nội dung, phương pháp dạy học trong nhà trường.
Thí sinh thi Đại học năm 2025 có bắt buộc thi môn Hóa học không?
Theo quy định hiện hành của Bộ Giáo dục và Đào tạo và hướng dẫn tổ chức kỳ thi tốt nghiệp Đại học năm 2025, thí sinh dự thi phải thực hiện như sau:
– Thi 3 môn bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
– Ngoài ra, thí sinh phải chọn một trong hai bài thi tổ hợp: Khoa học Tự nhiên (gồm các môn Vật lí, Hóa học, Sinh học) hoặc Khoa học Xã hội (gồm các môn Lịch sử, Địa lí, Giáo dục công dân – dành cho học sinh học chương trình giáo dục phổ thông).
Trong số các môn thi, Hóa học là một trong ba môn thuộc bài thi tổ hợp Khoa học Tự nhiên, thí sinh chỉ phải thi môn Hóa học nếu chọn tổ hợp này, không phụ thuộc vào mục đích xét tuyển đại học.
Như vậy, kỳ thi Đại học năm 2025 không bắt buộc thí sinh phải thi môn Hóa học, việc thi môn này phụ thuộc vào lựa chọn bài thi tổ hợp của thí sinh.




