Đề thi thử Đại học 2025 môn Hóa học – Sở GDĐT Đắk Lắk là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT, thuộc chương trình Đề thi vào Đại học.
Đề thi được thiết kế bám sát theo cấu trúc đề minh họa 2025 của Bộ GD&ĐT, bao gồm các chuyên đề trọng tâm như: este – lipit, amino axit – protein, polime, kim loại và bài toán nhận biết – bảo toàn. Đề có mức độ phân hóa tốt, phù hợp để học sinh ôn luyện, nâng cao kỹ năng giải nhanh và kiểm tra mức độ sẵn sàng cho kỳ thi.
Hãy cùng Dethitracnghiem.vn luyện tập và chinh phục đề thi này ngay hôm nay!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 SỞ GDĐT ĐẮK LẮK




Cho biết nguyên tử khối: H=1; C=12; O=16; S=32; Cl=35 ,5; Fe=56; Cu=64; Ag=108;
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Hợp chất nào dưới đây không tạo được liên kết hydrogen liên phân tử?
A. H₂S.
B. CH₃OH.
C. NH₃.
D. H₂O.
Câu 2. Thí nghiệm được tiến hành như hình vẽ bên.
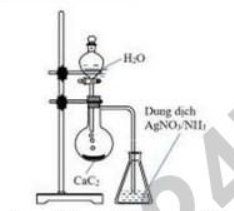
Hiện tượng xảy ra trong bình đựng dung dịch AgNO₃ trong NH₃ là
A. Có kết tủa vàng nhạt.
B. Dung dịch chuyển sang màu da cam.
C. Có kết tủa màu nâu đỏ.
D. Dung dịch chuyển sang màu xanh lam.
Câu 3. Cho 2 cặp oxi hóa – khử và thế điện cực chuẩn tương ứng: E⁰Fe²⁺/Fe (V) của Fe²⁺/Fe; Cu²⁺/Cu lần lượt là -0,440; +0,340. Sức điện động chuẩn của pin điện hóa tạo bởi các cặp oxi hóa – khử Fe²⁺/Fe và Cu²⁺/Cu là
A. -0,1 (V).
B. 0,78 (V).
C. 1,56 (V).
D. -0,87 (V).
Câu 4. Điện phân dung dịch copper (II) sulfate, nhóm học sinh đã tiến hành như sau: Nhúng hai điện cực vào cốc đựng khoảng 60 mL dung dịch CuSO₄ 0,5M rồi nối hai điện cực với nguồn điện để tiến hành điện phân (chú ý không để hai điện cực đã nối nguồn điện chạm vào nhau). Thời gian điện phân là 5 phút với cường độ dòng điện 10A. Quan sát hiện tượng thí nghiệm xảy ra, một học sinh đưa ra các phát biểu dưới đây, hãy cho biết phát biểu nào sai?
A. Màu xanh lam của dung dịch CuSO₄ nhạt dần.
B. Kim loại màu đỏ được sinh ra bám vào cathode.
C. Thấy có khí thoát ra ở 2 điện cực.
D. Có khí không màu (O₂) thoát ra ở anode.
Câu 5. Cho các phát biểu sau về amino acid:
(a) Amino acid có tính lưỡng tính, vừa có thể phản ứng với acid mạnh vừa có thể phản ứng với base mạnh.
(b) Ở pH thấp, amino acid tồn tại chủ yếu dưới dạng anion.
(c) Amino acid có thể di chuyển trong điện trường tùy thuộc vào pH của môi trường.
(d) Ở pH = 3, glycine nhận proton, trở thành cation và có khả năng di chuyển về phía cực âm.
Các phát biểu đúng là
A. (a), (b).
B. (a), (c), (d).
C. (a), (c).
D. (a), (b), (c).
Câu 6. Phân đạm là tên gọi chung của các loại phân bón vô cơ cung cấp nitrogen cho cây trồng, thúc đẩy quá trình tăng trưởng của cây, làm tăng năng suất cây trồng. Chất nào sau đây dùng làm phân đạm?
A. NaCl.
B. Ca(H₂PO₄)₂.
C. (NH₂)₂CO.
D. K₂CO₃.
Câu 7. Cho biết:

Trong các kim loại Cu, Ag, Fe và Ni. Số kim loại khử được ion H⁺ trong dung dịch ở điều kiện chuẩn là
A. 2.
B. 3.
C. 4.
D. 1.
Câu 8. Trong phân tử chất nào sau đây có 1 nhóm amino (-NH₂) và 2 nhóm carboxyl (-COOH)?
A. Lysine.
B. Formic acid.
C. Alanine.
D. Glutamic acid.
Câu 9. Phản ứng thủy phân tristearin trong môi trường kiềm còn được gọi là phản ứng
A. xà phòng hóa.
B. trùng hợp.
C. trùng ngưng.
D. este hóa.
Câu 10. Amino nào dưới đây là chất lỏng ở điều kiện thường?
A. methylamine.
B. ethylamine.
C. dimethylamine.
D. aniline.
Câu 11. Chất béo là triester của acid béo với
A. methyl alcohol.
B. ethyl alcohol.
C. ethylene glycol.
D. glycerol.
Câu 12. Chất nào dưới đây là thành phần chính của quặng hematite?
A. Iron(II) sulfide.
B. Iron(II) oxide.
C. Iron(III) oxide.
D. Iron.
Câu 13. Nước trái cây lên men có chứa rượu (alcohol) là một loại đồ uống khá quen thuộc với con người. Thực phẩm này thường được làm từ gạo nếp hoặc một số loại trái cây chín chứa nhiều đường, được ủ lên men và chưng cất thành rượu. Các cơ sở sản xuất rượu bán trên thị trường thường phải ghi rõ độ rượu. Trên nhãn một chai rượu Vang có ghi “ethanol 12%”. Cách ghi đó có ý nghĩa nào sau đây?
A. 100 ml rượu Vang trong chai này có 12 ml ethanol nguyên chất.
B. Trong chai rượu Vang này có 12 gam ethanol nguyên chất.
C. Rượu Vang trong chai có thành phần gồm 100 gam nước và 12 gam ethanol nguyên chất.
D. 100 ml rượu Vang trong chai này có 12 gam ethanol nguyên chất.
Câu 14. Phát biểu nào sau đây là không đúng khi nói về carbohydrate?
A. Cellulose không tan trong nước, nhưng tan tốt trong dung dịch Schweizer.
B. Tinh bột và cellulose là đồng phân cấu tạo của nhau.
C. Công thức phân tử glucose là C₆H₁₂O₆.
D. Sợi bông là cellulose gần như tinh khiết.
Câu 15. Carbohydrate nào sau đây thuộc loại polysaccharide?
A. Fructose.
B. Saccharose.
C. Tinh bột.
D. Glucose.
Câu 16. Tên gọi của polymer có công thức -(CH₂ – CHCl)-ₙ là
A. poly(vinyl chloride).
B. polyethylene.
C. polystyrene.
D. poly(methyl methacrylate).
Câu 17. Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
A. Cr.
B. Hg.
C. Pb.
D. W.
Câu 18. Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của các kim loại nhóm IA có dạng chung là
A. ns².
B. ns²np⁵.
C. ns²np³.
D. ns¹.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 6. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Trong công nghiệp, xút (sodium hydroxide) được sản xuất bằng phương pháp điện phân dung dịch sodium chloride có màng ngăn xốp. Bằng phương pháp này, người ta cũng thu được khí chlorine. Chất khí này được làm lỏng (loại hơi nước) rồi hóa lỏng để làm nguyên liệu quan trọng cho nhiều ngành công nghiệp chế biến và sản xuất hóa chất. Từ quá trình điện phân nêu trên, một lượng chlorine và hydrogen sinh ra được tận dụng để sản xuất hydrochloric acid đặc thương phẩm (nồng độ 32%, D = 1,153 g/mL ở 30 °C). Một nhà máy với quy mô sản xuất 200 tấn xút mỗi ngày thì đồng thời sản xuất được V m³ hydrochloric acid thương phẩm trên. Biết rằng, tại nhà máy này, 60% khối lượng chlorine sinh ra được dùng tổng hợp hydrochloric acid và hiệu suất của toàn bộ quá trình từ chlorine đến acid thương phẩm đạt 80% về khối lượng.
a) Có thể dùng sulfuric acid đặc làm khô khí chlorine thoát ra
b) Phương trình điện phân dung dịch NaCl là 2NaCl + 2H₂O → 2NaOH + H₂ + Cl₂.
c) Giá trị của V là 237 m³ (kết quả làm tròn đến hàng đơn vị).
d) Trong quá trình điện phân thì Cl₂ sẽ thoát ra tại cực cathode.
Câu 2. Một bạn học sinh đã tiến hành thí nghiệm như sau:
Bước 1: Cho 10 mL dung dịch H₂SO₄ 70% vào cốc thủy tinh, thêm một lượng nhỏ cellulose (bông) vào và dùng đũa thủy tinh khuấy đều. Sau đó, đặt cốc thủy tinh vào cốc nước nóng và khuấy trong khoảng 3 phút để cellulose tan hết tạo dung dịch đồng nhất.
Bước 2: Trung hoà dung dịch bằng cách thêm từ từ NaHCO₃ đến khi dùng sủi bọt khí, sau đó thêm tiếp 5 mL dung dịch NaOH 10%.
Bước 3: Cho 5 mL dung dịch thu được ở trên vào ống nghiệm chứa Cu(OH)₂ (được điều chế bằng cách cho 0,5 mL dung dịch CuSO₄ 5% vào 2 mL dung dịch NaOH 10%, lắc nhẹ). Đun nóng đều ống nghiệm khoảng 2 phút, sau đó để ống nghiệm trên giá khoảng 3 phút.
a) Sau bước 1, sản phẩm thu được có glucose.
b) Thí nghiệm trên chứng minh trong cellulose có 3 nhóm OH tự do và cellulose có tính chất của polyalcohol.
c) Thí nghiệm trên chứng minh trong cellulose có thể bị thủy phân trong môi trường acid hoặc môi trường base tạo glucose.
d) Sau bước 3, sản phẩm thu được có kết tủa màu đỏ gạch.
Câu 3. Trên bao bì một số sản phẩm được làm từ polimer X có kí hiệu như sau:

a) Kí hiệu 3 mũi tên tạo vòng khép kín có nghĩa sản phẩm làm từ PVC có thể tái chế sử dụng và hạn chế sự dùng tránh ô nhiễm môi trường.
b) Poly(vinyl chloride) được điều chế bằng phản ứng trùng ngưng vinyl chloride.
c) Trong công nghiệp, PVC được sản xuất từ ethylene với hiệu suất giả định cho từng bước theo sơ đồ sau: C₂H₄ → C₂H₅Cl → C₂H₄Cl₂ → CH₂=CHCl → PVC
độ H=85% H=68% H=79%
Để sản xuất 1,0 tấn PVC theo sơ đồ và hiệu suất trên thì cần dùng 1,2 tấn ethylene.
d) Polimer X là Poly(vinyl chloride) (PVC)
Câu 4. Trong phòng thí nghiệm, ethyl acetate được điều chế từ acetic acid và ethanol, xúc tác H₂SO₄ đặc, theo mô hình thí nghiệm sau:
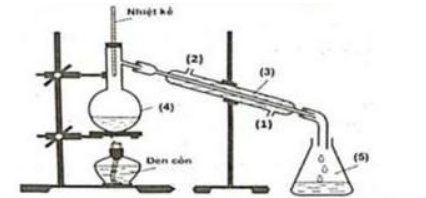
Biết nhiệt độ trong bình cầu (4) giữ ở mức 65 – 70°C, nhiệt độ trong ống sinh hàn (3) duy trì ở 25°C.
Cho biết nhiệt độ sôi của các chất như sau:

a) Khi thực hiện đun nóng 6,0 gam acetic acid với 6,0 gam ethanol có H₂SO₄ đặc làm xúc tác. Khối lượng ester tạo thành với hiệu suất phản ứng 60% là 6,6 gam.
b) Nếu nhiệt độ phản ứng ở bình cầu (4) càng cao thì phản ứng điều chế ethyl acetate xảy ra càng nhanh.
c) Chất lỏng trong bình hứng (5) có ethyl acetate.
d) Vai trò của ống sinh hàn (3) để ngưng tụ hơi, nước vào ở (1) và nước ra ở (2).
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Để xác định hàm lượng của Fe₂O₃ có trong một loại quặng, người ta tiến hành như sau: Cân 0,50 gam mẫu quặng, chế hóa theo quy trình hợp lí, thu được dung dịch X có chứa FeSO₄ trong môi trường H₂SO₄ (biết rằng toàn bộ lượng Fe₂O₃ trong quặng đều được chuyển thành FeSO₄). Dung dịch X tác dụng vừa đủ với 22,5 mL dung dịch KMnO₄ 0,025M. Thành phần phần trăm khối lượng của Fe₂O₃ có trong loại quặng nói trên là bao nhiêu? (Kết quả làm tròn đến hàng phần mười).
Câu 2. Trong các dung dịch (1) (CH₃)₂NH, (2) C₆H₅NH₂, (3) H₂NCH₂COOH, (4) H₂NCH₂CH(NH₂)COOH, (5) HOOCCH₂CH(NH₂)COOH. Số dung dịch làm quỳ tím chuyển sang màu xanh là bao nhiêu?
Câu 3. Một loại chất béo có chứa 65% triolein về khối lượng. Để sản xuất 4600 hộp kem dưỡng da (có chứa chất dưỡng ẩm glycerol) cần dùng tối thiểu x kg loại chất béo trên cho phản ứng với dung dịch NaOH, đun nóng. Biết rằng trong mỗi hộp kem dưỡng da có chứa 5 gam glycerol. Giá trị của x là bao nhiêu?
Câu 4. Khi nhiệt độ tăng lên 10%, tốc độ của một phản ứng hóa học tăng lên 3 lần. Hỏi khi nâng nhiệt độ lên từ 25°C đến 45°C thì tốc độ của phản ứng đó tăng lên bao nhiêu lần?
Câu 5. Cho các thí nghiệm sau về carbohydrate:
(a) Glucose phản ứng thuốc thử Tollens.
(b) Glucose phản ứng với nước bromine.
(c) Glucose phản ứng với copper(II) hydroxide trong môi trường kiềm, đun nóng.
(d) Saccharose phản ứng với copper(II) hydroxide trong môi trường kiềm ở điều kiện thường.
(e) Cellulose phản ứng với HNO₃ đặc có H₂SO₄ đặc, đun nóng.
Có bao nhiêu thí nghiệm xảy ra hoặc thuộc loại phản ứng oxi hóa – khử?
Câu 6. Để tráng một số lượng gương soi có diện tích bề mặt 0,5 m² với độ dày 0,1 μm người ta đun nóng dung dịch chứa 45 gam glucose với một lượng dung dịch silver nitrate trong ammonia. Biết khối lượng riêng của silver (bạc) là 10,49 g/cm³, hiệu suất phản ứng tráng bạc là 80% (tính theo glucose). Số lượng gương soi tối đa sản xuất được là? (Kết quả làm tròn đến hàng đơn vị).
Mục đích tổ chức kỳ thi Đại học năm 2025 là gì?
Căn cứ theo quy chế hiện hành của Bộ Giáo dục và Đào tạo và các văn bản hướng dẫn tổ chức kỳ thi Đại học năm 2025, mục đích của kỳ thi là:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo yêu cầu của chương trình giáo dục phổ thông.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục của địa phương và cả nước, làm cơ sở điều chỉnh nội dung, phương pháp dạy học trong nhà trường.
Thí sinh thi Đại học năm 2025 có bắt buộc thi môn Hóa học không?
Theo quy định hiện hành của Bộ Giáo dục và Đào tạo và hướng dẫn tổ chức kỳ thi tốt nghiệp Đại học năm 2025, thí sinh dự thi phải thực hiện như sau:
– Thi 3 môn bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
– Ngoài ra, thí sinh phải chọn một trong hai bài thi tổ hợp: Khoa học Tự nhiên (gồm các môn Vật lí, Hóa học, Sinh học) hoặc Khoa học Xã hội (gồm các môn Lịch sử, Địa lí, Giáo dục công dân – dành cho học sinh học chương trình giáo dục phổ thông).
Trong số các môn thi, Hóa học là một trong ba môn thuộc bài thi tổ hợp Khoa học Tự nhiên, thí sinh chỉ phải thi môn Hóa học nếu chọn tổ hợp này, không phụ thuộc vào mục đích xét tuyển đại học.
Như vậy, kỳ thi Đại học năm 2025 không bắt buộc thí sinh phải thi môn Hóa học, việc thi môn này phụ thuộc vào lựa chọn bài thi tổ hợp của thí sinh.




