Đề thi thử Đại học 2025 môn Hóa học – Sở GDĐT Lạng Sơn (Lần 1) là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT, nằm trong chương trình Đề thi vào Đại học.
Đề thi bám sát định hướng đề minh họa 2025 của Bộ GD&ĐT, bao gồm các chuyên đề quan trọng như: Este – Lipit, Amin – Amino axit, Cacbohiđrat, Kim loại, Phi kim và Hóa học đại cương. Với nội dung logic và mức độ phân hóa hợp lý, đề giúp học sinh rèn kỹ năng làm bài nhanh, chính xác và hiệu quả.
Hãy cùng Dethitracnghiem.vn khám phá đề thi này và bắt đầu luyện tập ngay hôm nay!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 SỞ GDĐT LẠNG SƠN (LẦN 1)
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1: Thuỷ phân saccharose, thu được hai monosaccharide X và Y. Chất X có nhiều trong quả nho chín nên còn được gọi là đường nho. Phát biểu đúng là
A. X không có phản ứng tráng bạc.
B. X có tính chất của alcohol đa chức.
C. Y không tan trong nước.
D. Y có phân tử khối bằng 342 amu.
Câu 2: Hình dưới đây là ký hiệu của 6 polymer nhiệt dẻo phổ biến có thể tái chế:

Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng….để giúp nhận biết vật liệu polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 6 được điều chế bằng phản ứng trùng hợp monomer là
A. CH₂=CH-C₆H₅.
B. CH₂=CH-Cl.
C. CH₂=CH-CH₃.
D. CH₂=CH₂.
Câu 3: Kim loại nào sau đây có nhiệt độ nóng chảy cao nhất?
A. Pb.
B. Na.
C. W.
D. Hg.
Câu 4: Tên thay thế của alanine là
A. 2-aminopropionic acid.
B. α-aminopropionic acid.
C. α-aminopropanoic acid.
D. 2-aminopropanoic acid.
Câu 5: Carbohydrate nào sau đây là chất rắn, hình sợi, không tan trong nước?
A. Tinh bột.
B. Glucose.
C. Cellulose.
D. Saccharose.
Câu 6: Insulin là hormone có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide X mạch hở. Khi thủy phân không hoàn toàn X, thu được hỗn hợp chứa các peptide: Phe-Phe-Tyr, Pro-Lys-Thr, Tyr-Thr-Pro, Phe-Tyr-Thr. Nếu đánh số thứ tự amino acid đầu N là số 1, thì amino acid ở vị trí số 6 trong X có kí hiệu là
A. Lys.
B. Tyr.
C. Pro.
D. Thr.
Câu 7: Phát biểu nào sau đây đúng?
A. Tơ nylon-6,6 được điều chế bằng phản ứng trùng ngưng các monomer tương ứng.
B. Trùng ngưng buta-1,3-diene với acrylonitrile có xúc tác Na được cao su buna-N.
C. Tơ visco là tơ bán tổng hợp.
D. Tơ nitron không có nhóm amide.
Câu 8: Triolein là chất béo không no, ở trạng thái lỏng. Công thức hóa học của triolein là
A. (C₁₇H₃₅COO)₃C₃H₅.
B. (C₁₅H₃₁COO)₃C₃H₅.
C. (C₁₇H₃₁COO)₃C₃H₅.
D. (C₁₇H₃₃COO)₃C₃H₅.
Câu 9: Khi đun nóng chất X có công thức phân tử C₄H₈O₂ với dung dịch NaOH thu được C₂H₅COONa. Công thức cấu tạo của X là
A. CH₃COOC₃H₇.
B. CH₃COOCH₃.
C. C₂H₅COOCH₃.
D. CH₃COOC₂H₅.
Câu 10: Ở trạng thái cơ bản, nguyên tử của nguyên tố nào sau đây có 1 electron ở lớp ngoài cùng?
A. Ca (Z = 20).
B. Na (Z = 11).
C. Al (Z = 13).
D. Fe (Z = 26).
Câu 11: Tại nhiều làng nghề thủ công mĩ nghệ, sulfur dioxide được dùng làm chất chống mốc cho các sản phẩm mây tre đan. Trong một ngày, một làng nghề đốt cháy 24 kg sulfur để tạo thành sulfur dioxide. Giả thiết có 20% lượng khí SO₂ trên bay vào khí quyền và chuyển hoá hết thành H₂SO₄ trong nước mưa theo sơ đồ: S → SO₂ → H₂SO₄. Nếu nồng độ H₂SO₄ trong nước mưa là 1,25.10⁻⁵ M thì thể tích (m³) nước mưa bị nhiễm acid có giá trị là
A. 10000.
B. 12000.
C. 24000.
D. 60000.
Câu 12: Catechin là một chất kháng oxi hoá mạnh, ức chế hoạt động của các gốc tự do nên có khả năng phòng chống bệnh ung thư, nhồi máu cơ tim. Trong lá chè tươi, catechin chiếm khoảng 25% đến 35% tổng trọng lượng khô. Ngoài ra, catechin còn có trong táo, lê, nho,…
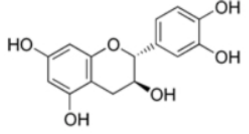
Công thức cấu tạo của catechin cho như hình dưới:
Phát biểu nào sau đây không đúng?
A. Catechin phản ứng được với dung dịch NaOH.
B. Phân tử catechin có 4 nhóm -OH phenol.
C. Công thức phân tử của catechin là C₁₅H₁₆O₆.
D. Catechin có phân tử khối là 290.
Câu 13: Ethylene là một hydrocarbon không no, có thể tham gia phản ứng với nhiều chất. Phản ứng hóa học của ethylene với dung dịch Br₂ được cho bởi phương trình: CH₂ = CH₂ + Br₂ → CH₂Br – CH₂Br. Cơ chế của phản ứng trên xảy ra như sau:
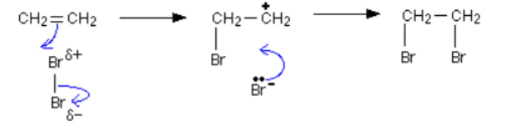
Cho các phát biểu sau:
(a) Phản ứng trên thuộc loại phản ứng thế.
(b) Giai đoạn 1, liên kết đôi phản ứng với tác nhân Brδ⁺ tạo thành phần tử mang điện dương.
(c) Giai đoạn 2, phần tử mang điện dương kết hợp với anion Br⁻ tạo thành sản phẩm.
(d) Hiện tượng của phản ứng là dung dịch bromine bị mất màu.
Số phát biểu đúng là
A. 4.
B. 1.
C. 3.
D. 2.
Câu 14: Có một số nhận xét về carbohydrate như sau:
(a) Saccharose, tinh bột và cellulose đều có thể bị thủy phân.
(b) Glucose, fructose, saccharose đều tác dụng được với Cu(OH)₂ và có khả năng tham gia phản ứng tráng bạc.
(c) Tinh bột và cellulose là đồng phân cấu tạo của nhau.
(d) Phân tử cellulose được cấu tạo bởi nhiều đơn vị β-glucose.
Trong các nhận xét trên, số nhận xét đúng là
A. 3.
B. 4.
C. 2.
D. 1.
Câu 15: Chất nào sau đây chứa liên kết cộng hoá trị trong phân tử?
A. KF.
B. HCl.
C. MgO.
D. NaCl.
Câu 16: Ammonia được tạo ra bằng cách cho nitrogen phản ứng với hydrogen với sự có mặt của chất xúc tác là iron. Phương trình phản ứng tạo ammonia diễn ra như sau: N₂(g) + 3H₂(g) ⇌ 2NH₃(g)
Biết năng lượng liên kết (E) ở 25°C; 1 bar của một số loại liên kết được cho trong bảng sau:

Biến thiên enthalpy chuẩn của phản ứng (kJ) tính theo năng lượng liên kết ở điều kiện trên có giá trị là
A. 993.
B. -959.
C. 1476.
D. -80.
Câu 17: Cho 5,6 gam CO và 5,4 gam H₂O vào một bình kín dung tích không đổi 10 L. Nung nóng bình một thời gian ở 830°C để hệ đạt đến trạng thái cân bằng. Phản ứng xảy ra như sau: CO(g) + H₂O(g) ⇌ CO₂(g) + H₂(g)
Biết hằng số cân bằng của phản ứng trong điều kiện trên là K_c = 1. Nồng độ của H₂O (M) ở trạng thái cân bằng là
A. 0,18.
B. 0,12.
C. 0,012.
D. 0,018.
Câu 18: Một pin điện hóa tạo bởi hai cặp oxi hóa – khử ở điều kiện chuẩn: Fe²⁺/Fe và Sn²⁺/Sn với thế điện cực chuẩn tương ứng là -0,44 V và -0,137 V. Cho các phát biểu về pin điện hóa trên như sau:
(a) Anode của pin là Fe.
(b) Cathode của pin là Fe²⁺.
(c) Quá trình xảy ra ở anode khi pin hoạt động là: Fe²⁺ + 2e⁻ → Fe.
(d) Quá trình xảy ra ở cathode khi pin hoạt động là: Sn²⁺ + 2e⁻ → Sn.
(đ) Sức điện động chuẩn của pin là 0,303 V.
Số phát biểu đúng là
A. 3.
B. 2.
C. 1.
D. 4.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
Câu 19: Tiến hành thí nghiệm sau: Cho vào ống nghiệm 1 mL dung dịch aniline. Thêm tiếp từ từ 0,5 – 1 mL nước bromine, vừa thêm vừa lắc đều.
a) Do ảnh hưởng của nhóm -NH₂ trong phân tử aniline làm giảm mật độ electron trong vòng benzene, đặc biệt ở các vị trí ortho và para nên phản ứng thế nguyên tử hydrogen trong vòng benzene của aniline dễ dàng hơn so với benzene.
b) Trong ống nghiệm xuất hiện kết tủa màu trắng có tên 2,4,6-tribromoaniline có phân tử khối bằng 330 amu.
c) Trong thí nghiệm trên, hiện tượng thu được tương tự nếu thay dung dịch aniline bằng dung dịch methylamine.
d) Thí nghiệm có thể dùng để phân biệt hai chất lỏng toluene và aniline.
Câu 20: Isoamyl acetate được dùng để tạo mùi chuối trong thực phẩm. Chất này cũng được dùng làm dung môi vecni và sơn mài cũng như dùng làm chất dẫn dụ các đàn ong mật đến một địa điểm nhỏ. Trong phòng thí nghiệm, isoamyl acetate được điều chế từ acetic acid và isoamyl alcohol với xúc tác H₂SO₄ đặc, ở nhiệt độ khoảng 145°C theo mô hình thí nghiệm sau :
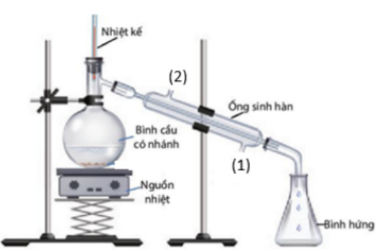
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, isoamyl alcohol và isoamyl acetate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau :

Biết nhiệt độ sôi của các chất acetic acid, isoamyl alcohol và isoamyl acetate lần lượt là 117,9°C; 131,1°C và 142°C.
a) Không thể dùng phương pháp chưng cất phân đoạn để tách các chất lỏng trong hỗn hợp sau phản ứng.
b) Dựa vào phổ hồng ngoại, có thể phân biệt được acetic acid, isoamyl alcohol và isoamyl acetate.
c) Chất lỏng trong bình hứng chỉ có isoamyl acetate.
d) Vai trò của ống sinh hàn để ngưng tụ chất lỏng, nước vào ở (1) và nước ra ở (2).
Câu 21: Điện phân (với điện cực trơ) dung dịch copper(II) sulfate, nhóm học sinh đã tiến hành như sau : Nhúng hai điện cực vào cốc đựng khoảng 60 mL dung dịch CuSO₄ 0,5M rồi nối hai điện cực với nguồn điện để tiến hành điện phân (Chú ý không để hai điện cực đã nối nguồn điện chạm vào nhau). Thời gian điện phân là 5 phút với cường độ dòng điện 10A. Quan sát hiện tượng thí nghiệm xảy ra, một học sinh phát biểu như sau :
a) Có khí không màu (O₂) thoát ra ở anode.
b) Màu xanh lam của dung dịch CuSO₄ nhạt dần.
c) Khi quá trình điện phân bắt đầu xảy ra, có khí thoát ra ở cả hai điện cực.
d) Kim loại màu đỏ được sinh ra bám vào cathode.
Câu 22: Nhúng thanh Cu tinh khiết có khối lượng là m₁ (gam) vào dung dịch iron(III) chloride, sau một thời gian, lấy thanh Cu ra cân lại thấy khối lượng là m₂ (gam). Cho các phát biểu sau :
a) Trên bề mặt thanh Cu có một lớp kim loại Fe bám vào.
b) Giá trị của m₂ lớn hơn m₁.
c) Phương trình phản ứng xảy ra là: 3Cu(s) + 2Fe²⁺(aq) → 2Fe(s) + 3Cu²⁺(aq).
d) Dung dịch thu được sau thí nghiệm chứa ion Fe²⁺.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
Câu 23: Muốn mạ đồng một tấm sắt có tổng diện tích bề mặt là x cm² với bề dày lớp mạ là 0,18 mm, người ta dùng tấm sắt đó làm cathode của một bình điện phân chứa dung dịch CuSO₄ và anode là một thanh đồng nguyên chất, rồi cho dòng điện có cường độ I = 10 A chạy qua trong thời gian 2 giờ 40 phút 50 giây. Cho biết đồng có khối lượng riêng D = 8,9 g/cm³; Điện lượng Q (coulomb) được xác định theo công thức: Q = n.F = I.t. Trong đó: n là số mol electron đi qua dây dẫn, I là cường độ dòng điện (ampe), t là thời gian (giây), hằng số Faraday F = 96500 C/mol. Giả thiết Cu được sinh ra bám đồng đều trên bề mặt tấm sắt với bề dày lớp Cu như nhau ở mọi vị trí. Tính giá trị của x (kết quả cuối cùng làm tròn đến hàng đơn vị).
Câu 24: Trong công nghiệp, kim loại nhôm được sản xuất từ quặng bauxite Al₂O₃.2H₂O bằng phương pháp điện phân nóng chảy với điện cực than chì và có mặt cryolite. Giả sử ở cathode thu được kim loại nhôm, ở anode chỉ thu được hỗn hợp khí CO và CO₂ theo tỉ lệ thể tích 1 : 1. Nếu thu được 99,16 m³ (ở đkc) hỗn hợp khí ở anode thì khối lượng (kg) quặng bauxite đã sử dụng là bao nhiêu? biết hiệu suất cả quá trình điện phân là 80% ?
Câu 25: Cho sơ đồ phản ứng sau (M, X, Y, T, W là các hợp chất hữu cơ khác nhau, T chỉ chứa một loại nhóm chức) :
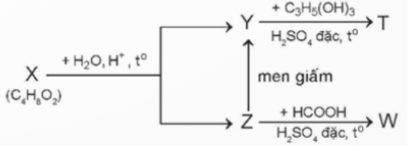
Phân tử khối của T là bao nhiêu ?
Câu 26: Cho các cặp oxi hoá – khử và giá trị thế điện cực chuẩn tương ứng :

Cho các phát biểu sau: Ở điều kiện chuẩn :
(1) Ion Cu²⁺ có tính oxi hoá mạnh hơn ion Fe³⁺.
(2) Dãy sắp xếp theo chiều tăng dần tính khử: Ag, Cu, Fe²⁺.
(3) Ion Fe²⁺ khử được ion Ag⁺ thành Ag kim loại.
(4) Ion Fe³⁺ và ion Ag⁺ đều oxi hoá được Cu thành ion Cu²⁺.
Viết số thứ tự của các phát biểu đúng theo thứ tự tăng dần từ trái sang phải (ví dụ: 12 hoặc 123 hoặc 23.).
Câu 27: Cellulose trinitrate là chất dễ cháy và nổ mạnh, được điều chế từ cellulose và nitric acid. Muốn điều chế 29,7 kg cellulose trinitrate (hiệu suất 90%) thì thể tích (lít) dung dịch nitric acid 96% (d = 1,52 g/mL) cần dùng là bao nhiêu? (kết quả cuối cùng làm tròn đến hàng phần mười)
Câu 28: Cocaine được tách từ lá cây “côca” lần đầu tiên năm 1860. Cocaine là một chất gây nghiện, được xếp vào loại ma túy mạnh. Khi phân tích định lượng cocaine, có %C = 67,33%; %H = 6,93%; %O = 21,12%; còn lại là nitrogen. Khối lượng phân tử của cocaine nhỏ hơn 400 amu. Số nguyên tử oxygen trong một phân tử cocaine là bao nhiêu ?
Mục đích tổ chức kỳ thi Đại học năm 2025 là gì?
Căn cứ theo quy chế hiện hành của Bộ Giáo dục và Đào tạo và các văn bản hướng dẫn tổ chức kỳ thi Đại học năm 2025, mục đích của kỳ thi là:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo yêu cầu của chương trình giáo dục phổ thông.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục của địa phương và cả nước, làm cơ sở điều chỉnh nội dung, phương pháp dạy học trong nhà trường.
Thí sinh thi Đại học năm 2025 có bắt buộc thi môn Hóa học không?
Theo quy định hiện hành của Bộ Giáo dục và Đào tạo và hướng dẫn tổ chức kỳ thi tốt nghiệp Đại học năm 2025, thí sinh dự thi phải thực hiện như sau:
– Thi 3 môn bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
– Ngoài ra, thí sinh phải chọn một trong hai bài thi tổ hợp: Khoa học Tự nhiên (gồm các môn Vật lí, Hóa học, Sinh học) hoặc Khoa học Xã hội (gồm các môn Lịch sử, Địa lí, Giáo dục công dân – dành cho học sinh học chương trình giáo dục phổ thông).
Trong số các môn thi, Hóa học là một trong ba môn thuộc bài thi tổ hợp Khoa học Tự nhiên, thí sinh chỉ phải thi môn Hóa học nếu chọn tổ hợp này, không phụ thuộc vào mục đích xét tuyển đại học.
Như vậy, kỳ thi Đại học năm 2025 không bắt buộc thí sinh phải thi môn Hóa học, việc thi môn này phụ thuộc vào lựa chọn bài thi tổ hợp của thí sinh.




