Đề thi thử Đại học 2025 môn Hóa học – Sở GD&ĐT Thái Nguyên là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT, nằm trong chương trình Đề thi vào Đại học.
Đề thi được biên soạn bám sát cấu trúc đề minh họa 2025 của Bộ GD&ĐT, tập trung kiểm tra các chuyên đề trọng tâm như: Este – Lipit, Amin – Amino axit, Cacbohiđrat, Kim loại, Phi kim và Hóa học đại cương. Với độ khó được phân chia hợp lý, đề thi giúp học sinh đánh giá năng lực, nâng cao kỹ năng giải nhanh và chuẩn bị vững vàng cho kỳ thi tốt nghiệp THPT.
Hãy cùng Dethitracnghiem.vn luyện tập với đề thi này để tự tin bước vào kỳ thi THPT Quốc gia 2025!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 SỞ GD&ĐT THÁI NGUYÊN
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Sodium carbonate là hóa chất quan trọng trong công nghiệp thủy tinh, bột giặt, phẩm nhuộm, giấy, sợi. Công thức của sodium carbonate là
A. Na₂CO₃.
B. NaHCO₃.
C. MgCO₃.
D. CaCO₃.
Câu 2. Chất nào sau đây thuộc loại monosaccharide?
A. Saccharose.
B. Cellulose.
C. Tinh bột.
D. Fructose.
Câu 3. Kim loại nào sau đây điều chế được bằng phương pháp thủy luyện?
A. Cu.
B. Mg.
C. Ca.
D. K.
Câu 4. Cho các phát biểu sau:
(a) Để khử chua đất bằng vôi sống (thành phần chính là CaO) và bón đạm ammonium cho lúa, cần bón vôi khử chua trước rồi vài ngày sau mới bón đạm ammonium.
(b) Ca₃(PO₄)₂ là thành phần chính của phần lân vi cung cấp nguyên tố dinh dưỡng phosphorus cho cây trồng.
(c) Tro thực vật cũng là một loại phân kali vì có chứa K₂CO₃.
(d) Người ta dùng loại phân bón chứa nguyên tố K để tăng cường sức chống bệnh, chống rét và chịu hạn cho cây.
Số phát biểu đúng là
A. 2.
B. 3.
C. 1.
D. 4.
Câu 5. Ion nào sau đây có tính oxi hoá mạnh nhất ở điều kiện chuẩn?
A. Cu²⁺.
B. Fe²⁺.
C. Ag⁺.
D. Al³⁺.
Câu 6. Cho các pin điện hóa và sức điện động chuẩn tương ứng:
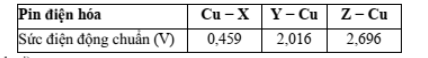 Dãy các kim loại xếp theo chiều tăng dần tính khử từ trái sang phải là
Dãy các kim loại xếp theo chiều tăng dần tính khử từ trái sang phải là
A. X, Cu, Z, Y.
B. Y, Z, Cu, X.
C. Z, Y, Cu, X.
D. X, Cu, Y, Z.
Câu 7. Ester X được tạo bởi ethyl alcohol và acetic acid. Công thức của X là
A. HCOOC₂H₅.
B. HCOOCH₃.
C. CH₃COOCH₃.
D. CH₃COOC₂H₅.
Câu 8. Phương trình hoá học của phản ứng khi cho ethylene tác dụng với dung dịch Br₂ là
CH₂=CH₂ + Br₂ → CH₂Br-CH₂Br
Cơ chế của phản ứng trên xảy ra như sau:
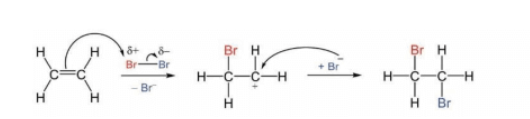 Nhận định nào sau đây không đúng?
Nhận định nào sau đây không đúng?
A. Trong giai đoạn đầu của phản ứng có sự hình thành liên kết σ.
B. Trong phân tử ethylene có 2 liên kết pi.
C. Phản ứng trên thuộc loại phản ứng cộng.
D. Trong giai đoạn đầu của phản ứng có sự phân cắt liên kết pi.
Câu 9. Công thức phân tử của ethylamine là
A. C₂H₅N.
B. C₂H₆N.
C. C₂H₇N.
D. C₂H₁₁N.
Câu 10. Phát biểu nào sau đây là đúng khi nói về tính điện li của amino acid?
A. Trong dung dịch, dạng tồn tại chủ yếu của amino acid chỉ phụ thuộc vào pH của dung dịch.
B. Ở pH thấp, amino acid tồn tại chủ yếu ở dạng anion (tích điện âm), di chuyển về điện cực dương trong điện trường.
C. Ở pH cao, amino acid tồn tại chủ yếu ở dạng cation (tích điện dương), di chuyển về điện cực âm trong điện trường.
D. Tính điện li của amino acid là khả năng di chuyển khác nhau trong điện trường tùy thuộc vào pH của môi trường.
Câu 11. Hiện nay, khí CO₂ là một trong những chất chữa cháy có thể dập tắt được nhiều loại đám cháy. Khí CO₂ trong bình chữa cháy được nén ở thể lỏng và nhiệt độ thấp (~70°C), khi phun ra sẽ làm loãng nồng độ oxygen và thu nhiệt xung quanh làm giảm nhiệt độ trong vùng cháy.
Cho các phát biểu sau:
 (a) Khí CO₂ được sử dụng chủ yếu trong bình chữa cháy để dập tắt các đám cháy chất lỏng, các đám cháy kim loại (Al, Mg), các đám cháy thiết bị điện, các đám cháy trong phòng thí nghiệm, các khoang tàu, hầm tàu,…
(a) Khí CO₂ được sử dụng chủ yếu trong bình chữa cháy để dập tắt các đám cháy chất lỏng, các đám cháy kim loại (Al, Mg), các đám cháy thiết bị điện, các đám cháy trong phòng thí nghiệm, các khoang tàu, hầm tàu,…
(b) Dùng bình khí CO₂ chữa cháy các đám cháy than hồng có thể tạo ra khí độc hại và nguy hiểm.
(c) Do khí chữa cháy, khí CO₂ không để lại dấu vết, không gây hư hỏng thiết bị nên bình chữa cháy bằng khí CO₂ được sử dụng nhiều trong phòng thí nghiệm hóa học và được học.
(d) Khi nồng độ khí CO₂ đủ để dập tắt đám cháy trong phòng kín thì có thể gây nguy hiểm cho sức khỏe và tính mạng nếu con người còn ở trong phòng bị cháy.
Số phát biểu đúng là
A. 3.
B. 1.
C. 4.
D. 2.
Câu 12. Phổ khối lượng (MS) là phương pháp hiện đại để xác định phân tử khối của các hợp chất hữu cơ. Kết quả phân tích phổ khối lượng cho chất X cho quả như hình dưới đây:
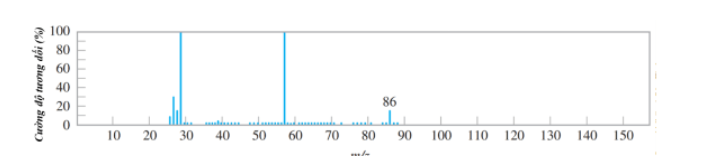 Chất X có thể là
Chất X có thể là
A. CH₃COOH
B. C₃H₇COOH
C. CH₃COOC₂H₅
D. HCOOHC₃H₇
Câu 13. Tên gọi của polymer có công thức (-CH₂-CH₂)n là
A. poly(vinyl chloride).
B. polyethylene.
C. poly(methylmethacrylate).
D. polystyrene.
Câu 14. Tên gọi của ester CH₃COOC₂H₅ là
A. ethyl formate.
B. methyl acetate.
C. methyl formate.
D. ethyl acetate.
Câu 15. Ở trạng thái cơ bản, cấu hình electron của ion Na⁺ là 1s²2s²2p⁶. Số hạt mang điện trong nguyên tử Na là
A. 18.
B. 11.
C. 9.
D. 22.
Câu 16. Số nhóm carboxyl (-COOH) trong phân tử alanine là
A. 3.
B. 1.
C. 2.
D. 4.
Câu 17. Nguyên tố calcium đóng vai trò tối thiết yếu cho việc phát triển xương, góp phần duy trì hoạt động của cơ bắp, truyền dẫn thần kinh, tăng cường khả năng miễn dịch. Trong cơ thể người, phần lớn calcium tập trung ở
A. xương.
B. răng.
C. cơ.
D. móng.
Câu 18. Kim loại nào sau đây có khối lượng riêng nhỏ nhất?
A. Fe.
B. Li.
C. Pb.
D. W.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Saccharose được sử dụng như một chất làm ngọt phổ biến trong sản xuất thực phẩm, có trong nhiều loại thực vật, có nhiều nhất trong cây mía, củ cải đường và hoa thốt nốt.
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho khoảng 2 mL dung dịch NaOH 10% vào ống nghiệm. Sau đó, thêm khoảng 0,5 mL dung dịch CuSO₄ 5% vào, lắc nhẹ.
Bước 2: Cho khoảng 3 mL dung dịch saccharose 5% vào ống nghiệm, lắc đều, thu được dung dịch X.
Bước 3: Đun nóng dung dịch X.
a) Công thức cấu tạo của saccharose là
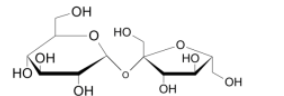 b) Bước 1 xuất hiện kết tủa màu xanh, bước 2 thu được dung dịch X có màu vàng.
b) Bước 1 xuất hiện kết tủa màu xanh, bước 2 thu được dung dịch X có màu vàng.
c) Do trong phân tử saccharose không còn nhóm –OH hemiacetal và nhóm –OH hemiketal nên ở bước 3 không thấy xuất hiện kết tủa màu đỏ gạch.
d) Nếu bước 1 thay dung dịch CuSO₄ bằng dung dịch FeSO₄ thì hiện tượng ở bước 2 vẫn tương tự.
Câu 2. Tiến hành thí nghiệm (như hình vẽ): Rót dung dịch NaCl bão hòa vào cốc 1, cốc 2, cốc 3; cho dầu nhờn vào cốc 4. Cho vào cốc 1 và cốc 4 một đinh sắt sạch, cho vào cốc 2 đinh sắt sạch được quấn bởi dây kẽm, cho vào cốc 3 đinh sắt sạch được quấn bởi dây đồng. Để 4 cốc trong không khí khoảng 5 ngày.
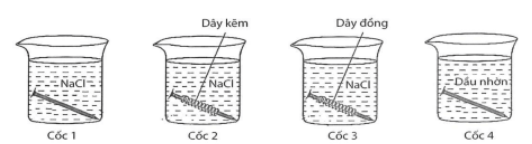 Cốc 1: NaCl solution, Iron nail.
Cốc 1: NaCl solution, Iron nail.
Cốc 2: NaCl solution, Iron nail wrapped with Zinc wire.
Cốc 3: NaCl solution, Iron nail wrapped with Copper wire.
Cốc 4: Oil, Iron nail.]
a) Ở cốc 4, đinh sắt không bị gỉ. Do đó các đồ vật bằng sắt có thể bảo vệ bằng cách tra dầu mỡ.
b) Để bảo vệ tàu biển làm bằng thép, người ta gắn các tấm kẽm lên vỏ tàu (phần chìm dưới nước).
c) Ở cốc 1, đinh sắt bị gỉ và dung dịch có màu vàng của FeCl₃. Ở cốc 2, đinh sắt không bị gỉ, dây Zn bị ăn mòn.
d) Ở cốc 3, đinh sắt bị gỉ nhanh nhất và dây đồng không bị ăn mòn.
Câu 3. β-carotene có rất nhiều trong rau quả xanh và vàng đặc biệt là ở quả gấc, cà rốt… β-carotene được cơ thể chuyển hóa thành vitamin A rất cần thiết cho cơ thể. Công thức cấu tạo của β-carotene là
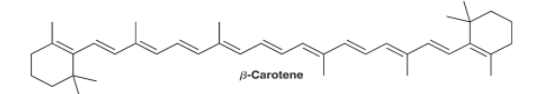 Thực hiện thí nghiệm tách β-carotene từ nước ép cà rốt như sau:
Thực hiện thí nghiệm tách β-carotene từ nước ép cà rốt như sau:
– Chuẩn bị: nước ép cà rốt, hexane; cốc thủy tinh 100 mL, bình tam giác 100 mL, phễu chiết 60 mL, giá thí nghiệm.
– Tiến hành:
Bước 1: Cho khoảng 20 mL nước ép cà rốt vào phễu chiết. Thêm khoảng 20 mL hexane, lắc đều khoảng 2 phút.
Bước 2: Để yên phễu chiết trên giá thí nghiệm khoảng 5 phút để chất lỏng tách thành hai lớp.
Bước 3: Mở khóa phễu chiết cho phần nước ở dưới chảy xuống, còn lại phần dung dịch β-carotene hòa tan trong hexane.
a) Trước khi chiết lớp hexane trong phễu không có màu, sau khi chiết lớp hexane trong phễu có màu vàng cam.
b) Thí nghiệm tách β-carotene từ nước cà rốt dựa theo nguyên tắc chiết lỏng – lỏng.
c) Phân tử carotene có công thức phân tử là C₄₀H₅₆ và có 11 liên kết pi.
d) β-carotene được tách ra khỏi nước dựa trên tính chất tan ít trong nước, tan nhiều trong dung môi hữu cơ.
Câu 4. Cho các bán phản ứng sau:
Zn²⁺ + 2e ⇌ Zn; E°Zn²⁺/Zn = -0,762V; Fe²⁺ + 2e ⇌ Fe; E°Fe²⁺/Fe = -0,440V
Cu²⁺ + 2e ⇌ Cu; E°Cu²⁺/Cu = +0,340V; Fe³⁺ + 1e ⇌ Fe²⁺; E°Fe³⁺/Fe²⁺ = +0,771V
O₂ + 2H⁺ + 2e ⇌ H₂O₂; E°O₂/H₂O₂ = +0,695V; H₂O₂ + 2H⁺ + 2e ⇌ 2H₂O; E°H₂O₂/H₂O = +1,770V
a) Trong cặp oxi hoá – khử, tính oxi hoá của dạng oxi hoá luôn mạnh hơn tính oxi hoá của dạng khử.
b) Trong cặp oxi hoá – khử, các nguyên tử trong dạng oxi hoá có số oxi hoá khác với các nguyên tử trong dạng khử.
c) Sức điện động chuẩn của pin điện hoá Fe – Cu là 0,780 V.
d) Điện phân (với điện cực trơ) dung dịch chứa ZnCl₂, FeCl₃ và CuCl₂, ion Fe³⁺ sẽ điện phân trước tại cathode.
PHẦN III. Câu hỏi yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Cho các chất sau: (1) chất rắn kết tinh, dễ tan trong nước, (2) phản ứng thủy phân, (3) phản ứng với copper(II) hydroxide, (4) phản ứng với nước bromine, (5) phản ứng với thuốc thử Tollens. Tính chất nào đúng với glucose? Liệt kê đáp án theo dãy số thứ tự tăng dần (ví dụ: 1234, 235,…).
Câu 2. Xăng E5 là một loại xăng sinh học, được tạo thành khi trộn 5 thể tích C₂H₅OH (D = 0,8 g/mL) với 95 thể tích xăng truyền thống. Giả sử xăng truyền thống chỉ chứa hai alkane C₅H₁₂ và C₇H₁₆ (tỉ lệ mol tương ứng 3 : 4, D ≈ 0,7 g/mL). Biết nhiệt lượng tỏa ra khi đốt cháy 1 mol các chất trong xăng E5 như sau: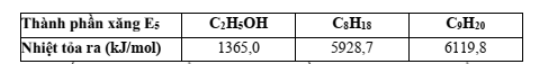
Trung bình, một chiếc xe máy di chuyển được 1 km thì cần một lượng chuyên thành công cơ học có độ lớn là 211,8 kJ. Nếu chiếc xe máy di chuyển từ Thái Nguyên đến Bắc Giang với quãng đường là 60 km thì hết bao nhiêu lít xăng E5 (làm tròn đến hàng phần mười)?
Biết hiệu suất sử dụng nhiên liệu của động cơ xe máy là 25%.
Câu 3. Cho các chất: alanine (1), aminoacetic acid (2), methylamine (3), aniline (4), glutamic acid (5). Chất nào trong số các chất trên tan tốt trong nước? Liệt kê đáp án theo số thứ tự tăng dần (ví dụ: 1234, 235,…).
Câu 4. Cho khí CO (dư) đi qua ống sứ đựng 1,82 gam hỗn hợp X gồm Al₂O₃ và CuO tới khi phản ứng xảy ra hoàn toàn. Dẫn khí đi ra vào nước vôi trong dư, tạo thành 1 gam kết tủa. Thành phần phần trăm khối lượng Al₂O₃ trong X là a%, tính giá trị của a (làm tròn đến hàng phần mười).
Câu 5. Điện phân nóng chảy hỗn hợp gồm Al₂O₃ (10%) và cryolite (90%) với anode và cathode đều là than chì. Sau thời gian điện phân thu được 5,4 tấn Al tại cathode và hỗn hợp khí tại anode gồm CO₂ (80% theo thể tích) và CO (20% theo thể tích). Giả thiết không có sản phẩm nào được sinh ra trong quá trình điện phân. Tính khối lượng carbon (theo tấn) đã bị oxi hóa tại anode (làm tròn kết quả đến hàng đơn vị).
Câu 6. Thủy phân hoàn toàn một triglyceride X trong dung dịch NaOH thu được glycerol và hỗn hợp sodium stearate và sodium oleate (tỉ lệ số mol tương ứng là 2 : 1). Phân tử khối của X là bao nhiêu?
Mục đích tổ chức kỳ thi Đại học năm 2025 là gì?
Căn cứ theo quy chế hiện hành của Bộ Giáo dục và Đào tạo và các văn bản hướng dẫn tổ chức kỳ thi Đại học năm 2025, mục đích của kỳ thi là:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo yêu cầu của chương trình giáo dục phổ thông.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục của địa phương và cả nước, làm cơ sở điều chỉnh nội dung, phương pháp dạy học trong nhà trường.
Thí sinh thi Đại học năm 2025 có bắt buộc thi môn Hóa học không?
Theo quy định hiện hành của Bộ Giáo dục và Đào tạo và hướng dẫn tổ chức kỳ thi tốt nghiệp Đại học năm 2025, thí sinh dự thi phải thực hiện như sau:
– Thi 3 môn bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
– Ngoài ra, thí sinh phải chọn một trong hai bài thi tổ hợp: Khoa học Tự nhiên (gồm các môn Vật lí, Hóa học, Sinh học) hoặc Khoa học Xã hội (gồm các môn Lịch sử, Địa lí, Giáo dục công dân – dành cho học sinh học chương trình giáo dục phổ thông).
Trong số các môn thi, Hóa học là một trong ba môn thuộc bài thi tổ hợp Khoa học Tự nhiên, thí sinh chỉ phải thi môn Hóa học nếu chọn tổ hợp này, không phụ thuộc vào mục đích xét tuyển đại học.
Như vậy, kỳ thi Đại học năm 2025 không bắt buộc thí sinh phải thi môn Hóa học, việc thi môn này phụ thuộc vào lựa chọn bài thi tổ hợp của thí sinh.




