Đề thi thử Đại học 2025 môn Hóa học – THPT Hà Trung – L1 – Thanh Hóa là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT. Đây là tài liệu giá trị dành cho học sinh lớp 12 đang ôn luyện giai đoạn nước rút trước kỳ thi quan trọng nhất trong năm.
Đề thi này được tổ chức bởi Trường THPT Hà Trung – Thanh Hóa trong đợt khảo sát lần 1 năm 2025, nhằm giúp học sinh lớp 12 đánh giá năng lực hiện tại và chuẩn bị kiến thức vững vàng trước kỳ thi Tốt nghiệp THPT Quốc gia. Với cấu trúc bám sát đề minh họa mới nhất của Bộ GD&ĐT, đề thi bao gồm các nội dung trọng tâm của chương trình lớp 12 như: este – lipit, amin – amino axit, kim loại, điện phân, hóa học vô cơ – hữu cơ, bài toán đồ thị và các câu hỏi phân loại cao.
Đặc biệt, đề thi còn chú trọng vào các phương pháp giải nhanh như: bảo toàn khối lượng, bảo toàn electron, phương pháp trung bình, phương pháp đường chéo, giúp học sinh tối ưu hóa thời gian làm bài và nâng cao kỹ năng giải quyết bài tập trắc nghiệm chính xác, hiệu quả.
Hãy cùng Dethitracnghiem.vn cùng tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 THPT HÀ TRUNG THANH HÓA LẦN 1
Cho biết nguyên tử khối:
H=1; Be = 9; C=12; N=14; O=16; Na=23; Mg=24; Al=27; S =32; Cl=35 ,5; K=39; Ca=40; Fe=56.
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Tiêu lệnh chữa cháy do cục cảnh sát phòng cháy, chữa cháy ban hành bao gồm các bước:
(a) Dùng bình chữa cháy cát và nước để dập tắt.
(b) Điện thoại số 114 đội chữa cháy chuyên nghiệp.
(c) Khi xảy ra cháy báo động gấp.
(d) Cúp cầu dao điện nơi xảy ra cháy.
Thứ tự đúng của các bước trên là
A. (c), (d), (a), (b).
B. (d), (b), (a), (c).
C. (d), (c), (a), (b).
D. (c), (d), (b), (a).
Câu 2. Chromium được sử dụng để cắt thuỷ tinh có thể được giải thích dựa vào tính chất vật lí nào?
A. Tính dẫn điện.
B. Tính dẫn nhiệt.
C. Tính cứng.
D. Tính dẻo.
Câu 3. Phổ khối lượng (MS) là phương pháp hiện đại để xác định phân tử khối của các hợp chất hữu cơ. Kết quả phân tích phổ khối lượng cho thấy phân tử khối của hợp chất hữu cơ X là 60. Chất X có thể là
A. ethyl alcohol.
B. acetic acid.
C. methyl acetate.
D. methylamine.
Câu 4. Trong phân tử chất nào sau đây có 1 nhóm amino (-NH₂) và 2 nhóm carboxyl (-COOH)?
A. Acid fomic.
B. Alanine.
C. Glutamic acid.
D. Lysine.
Câu 5. Cho các phát biểu sau:
(1)Glucose và fructose không tham gia phản ứng thủy phân.
(2)Có thể phân biệt glucose và fructose bằng nước bromine.
(3)Carbohydrate là những hợp chất hữu cơ tạp chức, thường có công thức chung là Cn(H₂O)m.
(4)Chất béo không phải là carbohydrate.
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 6. Dung dịch của chất nào sau đây có môi trường base?
A.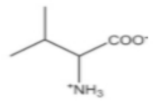
B.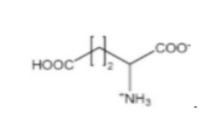
C.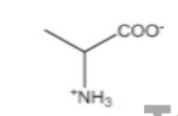
D.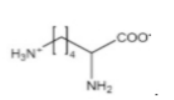
Câu 7. Hiện tượng phú dưỡng là một biểu hiện của môi trường ao, hồ bị ô nhiễm do dư thừa các chất dinh dưỡng. Sự dư thừa dinh dưỡng chủ yếu do hàm lượng các ion nào sau đây vượt quá mức cho phép?
A. Calcium, magnesium.
B. Sodium, potassium.
C. Chloride, sulfate.
D. Nitrate, phosphate.
Câu 8. Chất nào sau đây thuộc loại disaccharide?
A. Cellulose.
B. Glucose.
C. Fructose.
D. Saccharose.
Câu 9. Phát biểu nào sau đây đúng?
Trong tinh thể kim loại
A. các electron hoá trị và các ion dương kim loại đều chuyển động tự do trong toàn bộ mạng tinh thể.
B. các electron hoá trị ở các nút mạng và các ion dương kim loại chuyển động tự do.
C. các ion dương kim loại nằm ở các nút mạng tinh thể và các electron hoá trị chuyển động tự do xung quanh.
D. các electron hoá trị nằm ở giữa các nguyên tử kim loại cạnh nhau.
Câu 10. Kim loại nào sau đây có tính khử mạnh nhất?
A. Al.
B. K.
C. Mg.
D. Fe.
Câu 11. Polymer nào sau đây trong thành phần không chứa nguyên tố nitrogen?
A. Poly(ethylene terephthalate).
B. Poly(hexamethylene adipamide).
C. Polyacrylonitrile.
D. polycaproamide.
Câu 12. Ester X được tạo bởi methyl alcohol và acetic acid. Công thức của X là
A. CH₃COOCH₃.
B. CH₃COOC₂H₅.
C. HCOOC₂H₅.
D. HCOOCH₃.
Câu 13. Cho các cặp oxi hoá – khử của các halogen và thế điện cực chuẩn tương ứng:
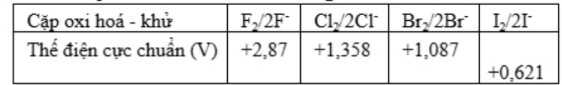 Dãy sắp xếp các ion halide theo thứ tự giảm dần tính khử là
Dãy sắp xếp các ion halide theo thứ tự giảm dần tính khử là
A. Br⁻, I⁻, F⁻, Cl⁻.
B. I⁻, Br⁻, Cl⁻, F⁻.
C. F⁻, Cl⁻, Br⁻, I⁻.
D. Cl⁻, F⁻, Br⁻, I⁻.
Câu 14. Một pin Galvani được cấu tạo bởi hai cặp oxi hoá – khử sau:
(1) Ag⁺ + 1e⁻ → Ag E°Ag⁺/Ag = 0,799 V
(2) Ni²⁺ + 2e⁻ → Ni E°Ni²⁺/Ni = -0,257 V
Khi pin làm việc ở điều kiện chuẩn, nhận định nào sau đây là đúng?
A. Ag được tạo ra ở cực âm và Ni²⁺ được tạo ra ở cực dương.
B. Ag⁺ được tạo ra ở cực âm và Ni được tạo ra ở cực dương.
C. Ag được tạo ra ở cực dương, Ni²⁺ được tạo ra ở cực âm.
D. Ag được tạo ra ở cực dương, Ni được tạo ra ở cực âm.
Câu 15. Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trọng đời sống: kích thích quả mau chín, điều chế nhựa làm sản phẩm gia dụng…. Phản ứng hóa học của ethylene với dung dịch Br₂ như sau:
CH₂ = CH₂ + Br₂ → CH₂Br-CH₂Br
Cơ chế của phản ứng trên xảy ra như sau:
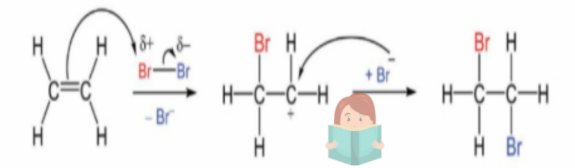 Nhận định nào sau đây không đúng?
Nhận định nào sau đây không đúng?
A. Giai đoạn 1, liên kết đôi phản ứng với tác nhân Br⁺ tạo thành phần tử mang điện dương.
B. Giai đoạn 2, phần tử mang điện dương kết hợp với anion Br⁻ tạo thành sản phẩm.
C. Phản ứng trên thuộc loại phản ứng cộng.
D. Hiện tượng của phản ứng là dung dịch bromine bị mất màu.
Câu 16. Trong hiện tượng ăn mòn kim loại xảy ra quá trình nào sau đây?
A. Quá trình khử kim loại.
B. Sự mài mòn kim loại.
C. Quá trình oxi hoá kim loại.
D. Quá trình điện phân.
Câu 17. Cho ester có công thức cấu tạo: CH₂=C(CH₃)COOCH₃. Tên gọi của ester là
A. methyl metacrylic.
B. methyl acrylic.
C. methyl methacrylate.
D. methyl acrylate.
Câu 18. Trong các chất dưới đây, chất nào là amine bậc hai?
A. CH₃NHCH₃.
B. (CH₃)₂CHNH₂.
C. C₆H₅NH₂.
D. H₂N[CH₂]₆NH₂.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Trong công nghiệp, copper(II) sulfate được sản xuất bằng cách ngâm đồng thô trong dung dịch H₂SO₄ loãng và sục oxygen không khí ở nhiệt độ thường.
Xét phản ứng xảy ra trong phương pháp sản xuất trên ở điều kiện chuẩn:
2Cu + O₂ + 2H₂SO₄ → 2CuSO₄ + 2H₂O
Cho các giá trị thế điện cực chuẩn của các cặp oxi hoá – khử: 2H⁺/H₂; Cu²⁺/Cu và O₂, H⁺/H₂O lần lượt là 0 V; +0,340 V và +1,229 V.
a) Cu là chất khử, O₂ là chất oxi hoá.
b) H₂SO₄ là môi trường.
c) O₂ có tính oxi hoá mạnh hơn ion H⁺.
d) H₂SO₄ là chất oxi hoá.
Câu 2. Trong dung dịch, dạng tồn tại của mỗi amino acid tùy thuộc vào giá trị pH của dung dịch đó. Giá trị pH mà khi đó amino acid tồn tại chủ yếu ở dạng ion lưỡng cực (nồng độ ion lưỡng cực là cực đại) được gọi là điểm đăng điện (pI). Khi pH > pI thì amino acid tồn tại chủ yếu ở dạng anion, pH < pI thì amino acid tồn tại chủ yếu ở dạng cation. Khi đặt dung dịch amino acid trong một điện trường thì dạng lưỡng cực không di chuyển về phía điện cực nào cả (nằm giữa hai điện cực), dạng anion sẽ di chuyển về phía cực dương còn dạng cation sẽ di chuyển về phía cực âm. Cho hai amino acid sau:
 Một nhóm học sinh nghiên cứu về tính điện di của glutamic acid (pI = 3,2) và lysine (pI = 9,7) rồi đưa ra kết luận:
Một nhóm học sinh nghiên cứu về tính điện di của glutamic acid (pI = 3,2) và lysine (pI = 9,7) rồi đưa ra kết luận:
a) Khi pH = 1 thì glutamic acid và lysine đều di chuyển về cực âm (cathode).
b) Khi pH = 13 thì glutamic acid tồn tại chủ yếu dạng anion HOOC-CH₂-CH₂-CH(NH₂)-COO⁻ và di chuyển về phía cực dương.
c) Khi pH = 6 thì glutamic acid di chuyển về phía cực âm còn lysine di chuyển về phía cực dương.
d) Có thể tách được glutamic acid và lysine ra khỏi hỗn hợp trong dung dịch ở pH = 6 bằng phương pháp điện di.
Câu 3. Một nhóm học sinh đã thực hiện phản ứng điều chế ethyl acetate từ nguyên liệu ban đầu là acetic acid và ethanol trong phòng thí nghiệm. Khi phản ứng kết thúc, nhóm đã thu được hỗn hợp sản phẩm gồm ethyl acetate và acetic acid, ethanol còn dư theo phương trình hoá học:
H⁺ CH₃COOH + C₂H₅OH ⇌ CH₃COOC₂H₅ + H₂O
Vì ethyl acetate không phân cực, còn acetic acid và ethanol đều phân cực nên nhóm đã dùng dung môi hữu cơ không phân cực diethyl ether (C₂H₅OC₂H₅) để chiết ethyl acetate ra khỏi hỗn hợp sau phản ứng.
a) Diethyl ether là dung môi chiết lí tưởng trong thí nghiệm trên vì ethyl acetate tan tốt trong dung môi này, còn acetic acid và ethanol lại tan tốt trong nước.
b) Bằng phương pháp chưng cất đơn giản, ta có thể tách ethyl acetate ra khỏi dung môi diethyl ether sau khi chiết.
c) Do diethyl ether có nhiệt độ sôi thấp hơn nhiều so với ethyl acetate (34,6 °C so với 77,1 °C) nên có thể thu được ethyl acetate sau khi chiết bằng cách dùng đèn cồn đun nhẹ cho dung môi diethyl ether bay hơi.
d) Để an toàn, ta có thể dùng nước nóng liên tục tưới lên bình cầu trong phương pháp chưng cất đơn giản để tách ethyl acetate ra khỏi dung môi diethyl ether sau khi chiết.
Câu 4. Polymer X có tính dai, bền, mềm mại, óng mượt, ít thấm nước, giặt mau khô. Polymer X dùng để dệt vải may mặc, vải lót săm lốp xe, dệt bít tất, bện làm dây cáp, dây dù, đan lưới, … Cấu tạo một đoạn mạch polymer X như sau:
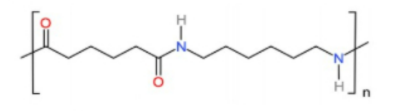 a) Các loại vải làm từ nylon-6,6 có thể giặt trong nước có độ kiềm cao.
a) Các loại vải làm từ nylon-6,6 có thể giặt trong nước có độ kiềm cao.
b) X được điều chế từ hexamethylenediamine và adipic acid bằng phản ứng trùng hợp.
c) X có tên là tơ nylon-6,6.
d) Các nhóm amide trong nylon-6,6 có khả năng tạo liên kết hydrogen giữa các chuỗi polymer, giúp tăng cường các tính chất cơ học cho nylon-6,6.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Trong quá trình sản xuất nhôm bằng phương pháp điện phân nóng chảy aluminium oxide, điện cực dương bằng than chì bị ăn mòn liên tục do phản ứng giữa carbon và oxygen tạo thành hỗn hợp khí O₂, CO và CO₂. Giả sử các khí trong hỗn hợp trên có tỉ lệ mol bằng nhau, các phản ứng xảy ra hoàn toàn, mỗi kg nhôm sinh ra tương ứng với bao nhiêu kg than chì bị đốt cháy ở cực dương? (Kết quả được làm tròn đến hàng phần trăm).
Câu 2. Khi xà phòng hóa hoàn toàn triglyceride X bằng dung dịch NaOH, đun nóng, thu được sản phẩm gồm glycerol và chất hữu cơ Y. Cho Y tác dụng với dung dịch HCl dư thu được palmitic acid. Xác định phân tử khối của X?
Câu 3. Glucose tồn tại đồng thời dạng mạch hở và mạch vòng (α và β). Glucose có tính chất của aldehyde và của polyalcohol. Cho các chất sau: Cu(OH)₂, nước bromine, dung dịch I₂ trong KI, thuốc thử Tollens và CH₃OH/HCl khan? Ở điều kiện thích hợp, số chất tác dụng được với glucose là bao nhiêu?
Câu 4. Số đồng phân amine bậc hai có công thức phân tử C₅H₁₃N là bao nhiêu?
Câu 5. Xăng E5 là một loại xăng sinh học, được tạo thành khi trộn 5 thể tích C₂H₅OH (D = 0,8 g/ml) với 95 thể tích xăng truyền thống, giúp thay thế một phần nhiên liệu hóa thạch đang ngày càng cạn kiệt cũng như giảm thiểu ô nhiễm môi trường. Khi đốt cháy hoàn toàn 1 lít xăng E5 thì hạn chế được a phần trăm thể tích khí CO₂ thải vào không khí so với đốt cháy hoàn toàn 1 lít xăng truyền thống ở cùng điều kiện nhiệt độ và áp suất. Giả sử xăng truyền thống chỉ chứa hai ankan C₈H₁₈ và C₉H₂₀ (tỉ lệ mol tương ứng 4 : 3, D = 0,7 g/ml). Giá trị của a là bao nhiêu? (Kết quả được làm tròn đến kết quả hàng phần trăm).
Câu 6. Một công ty chuyên sản xuất thép với công nghệ là lò luyện thép Martin (phản ứng luyện thép trong lò là: FeₓOᵧ + C → Fe + CO₂). Nguyên liệu công ty trên sử dụng để luyện thép gồm sắt phế liệu (chứa 50% Fe₃O₄; 49% Fe; 1% C theo khối lượng) và gang (với 4% khối lượng C). Với giá thành nguyên liệu và chi phí (nhân công, điện, hao mòn thiết bị) cho theo bảng sau:

Một mẻ luyện thép vừa đủ cần 5 tấn gang và m tấn sắt (iron) phế liệu. Kết quả số tiền công ty lãi là a triệu đồng. Giá trị của a là bao nhiêu? (Kết quả được làm tròn đến hàng phần mười).
Mục đích tổ chức kỳ thi Đại học năm 2025 là gì?
Căn cứ theo quy chế hiện hành của Bộ Giáo dục và Đào tạo và các văn bản hướng dẫn tổ chức kỳ thi Đại học năm 2025, mục đích của kỳ thi là:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo yêu cầu của chương trình giáo dục phổ thông.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục của địa phương và cả nước, làm cơ sở điều chỉnh nội dung, phương pháp dạy học trong nhà trường.
Thí sinh thi Đại học năm 2025 có bắt buộc thi môn Hóa học không?
Theo quy định hiện hành của Bộ Giáo dục và Đào tạo và hướng dẫn tổ chức kỳ thi tốt nghiệp Đại học năm 2025, thí sinh dự thi phải thực hiện như sau:
– Thi 3 môn bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
– Ngoài ra, thí sinh phải chọn một trong hai bài thi tổ hợp: Khoa học Tự nhiên (gồm các môn Vật lí, Hóa học, Sinh học) hoặc Khoa học Xã hội (gồm các môn Lịch sử, Địa lí, Giáo dục công dân – dành cho học sinh học chương trình giáo dục phổ thông).
Trong số các môn thi, Hóa học là một trong ba môn thuộc bài thi tổ hợp Khoa học Tự nhiên, thí sinh chỉ phải thi môn Hóa học nếu chọn tổ hợp này, không phụ thuộc vào mục đích xét tuyển đại học.
Như vậy, kỳ thi Đại học năm 2025 không bắt buộc thí sinh phải thi môn Hóa học, việc thi môn này phụ thuộc vào lựa chọn bài thi tổ hợp của thí sinh.




