Đề thi thử Đại học 2025 môn Hóa học – THPT Trần Quốc Tuấn là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Đề thi bám sát cấu trúc minh họa năm 2025 của Bộ GD&ĐT, bao phủ các chuyên đề trọng tâm như: este – lipit, amino axit – protein, polime, kim loại, phản ứng vô cơ – hữu cơ và các dạng bài tính nhanh, nhận biết. Với mức độ từ cơ bản đến nâng cao, đề giúp học sinh rèn kỹ năng xử lý câu hỏi trắc nghiệm hiệu quả và tự đánh giá năng lực bản thân.
Hãy cùng Dethitracnghiem.vn khám phá và luyện đề ngay hôm nay để tăng tốc ôn luyện cho kỳ thi sắp tới!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 THPT TRẦN QUỐC TUẤN





Cho biết nguyên tử khối: H = 1; C = 12; O = 16; Al = 27; S = 32; K = 39; Ca = 40; Mn = 55; Fe = 56; Cu = 64; Ba = 137.
Các kết quả làm tròn ở phép tính cuối cùng
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Carbohydrate nào dưới đây không có nhóm –OH hemiaxetal (hoặc hemiketal) trong phân tử?
A. Maltose.
B. Saccharose.
C. Glucose.
D. Fructose.
Câu 2. Cho hai quá trình sau:
[Cu(OH)₂]⁴⁻(aq) + 2NH₃(aq) ⇌ Cu(NH₃)₂₂(aq) + 2H₂O(l) ΔrH°₂₉₈ = –46kJ (I)
[Cu(OH)₂]⁴⁻(aq) + en(aq) ⇌ Cu(en)₂]⁴⁻(aq) + 2H₂O(l) ΔrH°₂₉₈ = –54 kJ (II)
Trong đó, en là ethylenediamine. Phản ứng này đã dùng tất cả các cặp electron hóa trị riêng để tạo liên kết chelate với cation Cu²⁺. Cho các phát biểu sau:
(1) quá trình (II) thuận lợi hơn quá trình (I) về mặt năng lượng.
(2) Phản ứng diễn ra ở quá trình (I) có sự biến đổi màu sắc.
(3) Xung quanh nguyên tử trung tâm trong phức chất [Cu(en)(OH)₂]⁴⁻ có 6 liên kết σ.
(4) Phản ứng diễn ra ở quá trình (I) và (II) đều có sự tạo thành phức không tan.
Số phát biểu đúng là:
A. 2.
B. 3.
C. 1.
D. 4.
Câu 3. Chất nào sau đây là dipeptide?
A. Gly-Val-Ala.
B. Glu-Glu-Ala.
C. Ala-Gly.
D. Valine.
Câu 4. Muối nào sau đây chỉ tồn tại trong dung dịch và bị phân hủy khi đun nóng?
A. CaCl₂.
B. Ca(NO₃)₂.
C. NaHCO₃.
D. CaSO₄.
Câu 5. Polymer không dùng làm chất dẻo là?
A. Polyethylene.
B. Poly(vinyl chloride).
C. Poly(urea-formaldehyde).
D. Poly(phenol formaldehyde).
Câu 6. Những thanh copper tinh khiết có khối lượng m₁ gam vào dung dịch iron(III) chloride, sau một thời gian, lấy thanh copper ra cân lại thấy khối lượng là m₂ gam. Phát biểu nào sau đây đúng?
A. Trên bề mặt thanh copper có 1 lớp kim loại iron bám vào.
B. Giá trị m₂ lớn hơn m₁.
C. Thí nghiệm trên có xảy ra ăn mòn điện hóa học.
D. Phương trình phản ứng xảy ra là: 3Cu(s) + 2Fe³⁺(aq) → 2Fe(s) + 3Cu²⁺(aq).
Câu 7. Ion barium cho ngọn lửa có màu gì khi thử màu ngọn lửa?
A. Màu lục.
B. Màu vàng.
C. Màu tím.
D. Màu đỏ son.
Câu 8. Trong phân tử chất nào sau đây không chứa nguyên tố nitrogen?
A. Methylammonium chloride.
B. Hemoglobin.
C. Saccharose.
D. Valine.
Câu 9. Điện phân dung dịch copper(II) sulfate bằng cặp điện cực copper với cường độ dòng điện không đổi. Đồ thị biểu diễn sự thay đổi khối lượng anode và cathode theo thời gian lần lượt là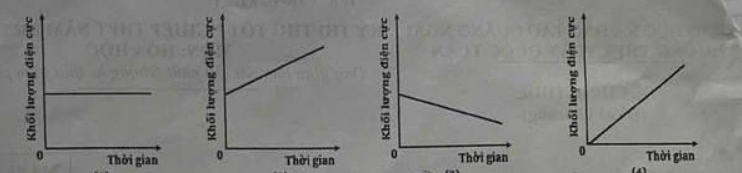
A. (2) và (3).
B. (2).
C. (3) và (2).
D. (3) và (4).
Câu 10. Cho cấu trúc phân tử của một carbohydrate như sau:
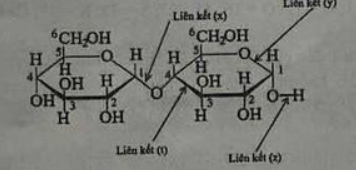 Liên kết glycoside là liên kết nào?
Liên kết glycoside là liên kết nào?
A. Liên kết (t).
B. Liên kết (y).
C. Liên kết (z).
D. Liên kết (x).
Câu 11. Oxaliplatin là thành phần chính của thuốc chống ung thư eloxatin, có công thức cấu tạo như hình bên. Số phối trí xung quanh nguyên tử trung tâm trong phân tử oxaliplatin là
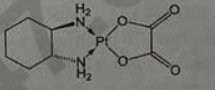 A. 3.
A. 3.
B. 2.
C. 4.
D. 1.
Câu 12. Hiện tượng “nước chảy đá mòn” và hiện tượng “xâm thực” của nước mưa vào các phiến đá vôi là do trong nước có hòa tan khí nào sau đây?
A. N₂.
B. CO₂.
C. CH₄.
D. O₂.
Câu 13. Kim loại nào sau đây không tan trong nước ở điều kiện thường?
A. Ba.
B. Be.
C. K.
D. Sr.
Câu 14. Trong công nghiệp, hydrogen hóa chất béo không no thành chất béo no để sản xuất các loại bơ nhân tạo. Chất béo X có công thức phân tử là C₅₅H₁₀₀O₆. Hydrogen hóa hoàn toàn chất béo X (xúc tác Nickel, t°) thu được chất béo Y. Công thức phân tử của Y là
A. C₅₅H₁₀₄O₆.
B. C₅₅H₁₀₆O₆.
C. C₅₅H₁₀₈O₆.
D. C₅₅H₁₁₀O₆.
Câu 15. Khi đun nóng ester của acetic acid trong dung dịch NaOH xảy ra phản ứng hóa học sau:
CH₃COOR + NaOH → CH₃COONa + ROH ()
Cơ chế của phản ứng xảy ra như sau: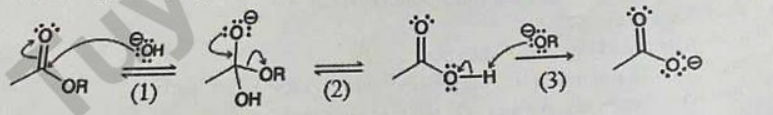
Nhận định nào sau đây không đúng?
A. Giai đoạn (1), acid nhường proton.
B. Giai đoạn (1) có sự phá vỡ liên kết π hình thành liên kết σ.
C. Phản ứng () là phản ứng thủy phân ester trong môi trường kiềm.
D. Giai đoạn (2) có sự thay thế nhóm OH bằng nhóm OR.
Câu 16. Nước nhiễm phèn thường có vàng nâu máu. Đó là do sự xuất hiện của:
A. [Fe(OH)₂(H₂O)₄]⁺.
B. [Al(OH)(H₂O)₅]²⁺.
C. [Fe(OH)₃].
D. [Al(OH)₃].
Câu 17. Trong cơ thể người, ion Mg²⁺ (Z=12) tham gia cấu trúc tế bào, tổng hợp protein và chất sinh năng lượng ATP (Adenosine Triphosphate). Tổng số hạt proton và electron của ion Mg²⁺ là
A. 12.
B. 24.
C. Mg²⁺.
D. 26.
Câu 18. Trong quá trình Solvay, ở giai đoạn tạo thành NaHCO₃ tốn cần bằng sau:
NaCl + NH₃ + CO₂ + H₂O → NaHCO₃ + NH₄Cl
Khi làm lạnh dung dịch trên, muối bị tách ra khỏi dung dịch là
A. NH₃.
B. NH₄HCO₃.
C. NH₄Cl.
D. NaHCO₃.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Dưới đây là sơ đồ để tách hỗn hợp amine benzen (RNH₂) và phenol (ArOH). Giả sử các chất trên không tan trong nước nhưng tan trong diethyl ether. Hỗn hợp này được tách thành các phần A, B.
[Diagram showing separation steps using diethyl ether, HCl, NaOH, resulting in A and B layers]
a) Hỗn hợp này được tách thành các phần A, B.
b) Quy trình tách trên dựa trên cơ sở của phương pháp kết tinh.
c) Dùng môi diethyl ether được thêm vào các bước cùng với dung nước nhằm mục đích hòa tan HCl và NaOH.
d) Có thể áp dụng quy trình tách này cho hỗn hợp gồm chất béo tristearin và phenol.
Câu 2. Để khảo sát sự ảnh hưởng của pH môi trường đến khả năng hoạt động của enzyme trong quá trình tiêu hóa ở người, nhóm học sinh đã khảo sát sự thủy phân albumin (protein có trong lòng trắng trứng) bằng enzyme pepsin được trình bày dưới bảng sau:
[Table showing experiment number, mixture, and clarity (Đục/Trong) at times t=0 and t=20 minutes]
Tiến hành thí nghiệm tương tự đối với chymotrypsin (một loại enzyme), thu được đồ thị sau:
[Graph showing relative rate of activity (Tốc độ phản ứng tương đối) vs pH for Pepsin and Chymotrypsin]
a) Albumin là protein dạng sợi, không tan trong nước nên ban đầu dung dịch bị đục.
b) Ở ống nghiệm 3, nếu thay pepsin thành chymotrypsin thì hiện tượng quan sát được là “từ đục thành trong” sau thí nghiệm.
c) Pepsin hoạt động tốt nhất ở pH = 2.
d) Từ kết quả thí nghiệm thì enzyme pepsin và chymotrypsin đều hoạt động tốt trong môi trường acid.
Câu 3. pI là giá trị pH mà tại đó amino acid có nồng độ ion lưỡng cực cực đại. Cho giá trị pI của các chất sau:
[Table showing Amino acid, Công thức cấu tạo (Structure), pI for Glycine, Aspartic acid, Lysine]
Dung dịch X gồm: glycine, aspartic acid và lysine. Đặt X vào nguồn điện một chiều, thấy hỗn hợp tách thành ba vết (trong đó có một vết chất không di chuyển) như hình sau:
[Diagram showing electrophoresis gel with wells labelled (1) (hỗn hợp X), (2), (3) and electrodes anode (-) and cathode (+)]
a) Dung dịch X có pH = 3.
b) Trong môi trường acid mạnh, glycine tồn tại chủ yếu ở dạng H₂N-CH₂-COO⁻.
c) Vị trí (3) tương ứng với chất lysine.
d) Nếu dung dịch X có pH = 8 thì glycine và aspartic acid di chuyển về cực (+) của điện trường.
Câu 4. Người ta thiết lập pin điện (I) và pin (II) ở điều kiện chuẩn theo sơ đồ như hình bên dưới.
[Diagrams of two electrochemical cells, Pin (I) and Pin (II)]
Nếu thiết lập pin (III) gồm kim loại Z(s) nhúng trong dung dịch Z²⁺ và kim loại Y(s) nhúng trong dung dịch Y²⁺ ở điều kiện chuẩn thì phát biểu nào sau đây đúng?
a) Trong pin (III), tại cực (+) diễn ra quá trình oxi hóa Z.
b) Trong pin (III), cực anode là Y(s).
c) Ba pin sẽ có sức điện động giảm theo thứ tự: Pin (I) > Pin (II) > Pin (III).
d) Tính khử của kim loại giảm dần Z > X > Y.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Tiến hành thí nghiệm sau:
(1) Sục khí CO₂ dư vào dung dịch Ca(OH)₂.
(2) Cho dung dịch NaOH dư vào dung dịch Ba(HCO₃)₂.
(3) Đun sôi một mẫu nước có tính cứng tạm thời.
(4) Cho dung dịch KHSO₄ vào dung dịch Ba(OH)₂.
Khi kết thúc phản ứng, số thí nghiệm thu được kết tủa là bao nhiêu?
Câu 2. Hyaluronic acid (HA) là thành phần chính của nhiều sản phẩm làm đẹp, lớp đệm cấp ẩm, ngăn ngừa lão hóa. Hyaluronic acid (HA) có công thức cấu tạo như hình bên. Hãy cho biết mỗi mắt xích của hyaluronic acid có bao nhiêu nguyên tử H?
[Structure of a repeating unit of Hyaluronic acid is shown]
Câu 3. Theo quy ước, một đơn vị đo nồng độ của dung dịch được tính bằng số milimol Ca²⁺ hoặc Mg²⁺ trong 1,0 Lít nước. Một loại nước cứng chưa đồng thời các ion Ca²⁺, HCO₃⁻ và Cl⁻. Để làm mềm 20 Lít nước cứng đó cần dùng vừa đủ 100 mL dung dịch chứa NaOH 0,2M và Na₃PO₄ 0,2M, thu được nước mềm (không chứa Ca²⁺). Số đơn vị độ cứng của nước cứng đó là bao nhiêu?
Câu 4. Trong quá trình bảo quản, một mẫu muối FeSO₄.7H₂O bị oxi hóa bởi oxygen trong không khí (oxi hóa trong không khí), người ta tiến hành như sau: Hòa tan toàn bộ X trong dung dịch loãng chứa 0,035 mol H₂SO₄ loãng, thu được 100 mL dung dịch Y. Tiến hành hai thí nghiệm với Y:
Thí nghiệm 1: Cho lượng dư dung dịch BaCl₂ vào 20 mL dung dịch Y, thu được 2,33 gam kết tủa.
Thí nghiệm 2: Thêm dung dịch H₂SO₄ (loãng, dư) vào 20 mL dung dịch Y, thu được dung dịch Z. Nhỏ từ từ dung dịch KMnO₄ 0,03 M vào Z đến khi phản ứng vừa đủ thì hết 18 mL.
Xác định giá trị của a?
Câu 5. Nung 25 gam một mẫu quặng malachite có thành phần chính là Cu(OH)₂.CuCO₃ (còn lại là tạp chất trơ) trong không khí đến khối lượng không đổi, theo sơ đồ phản ứng:
Cu(OH)₂.CuCO₃ → CuO + H₂O + CO₂
Cho toàn bộ lượng chất rắn thu được (gồm CuO và tạp chất trơ) vào cốc thủy tinh, sau đó cho từ từ dung dịch H₂SO₄ 19,6% vào cốc cho đến khi chất rắn không tan thêm được nữa thì dừng lại, lọc bỏ tạp chất trơ thu được dung dịch X. Làm lạnh toàn bộ dung dịch X xuống 10°C thu được dung dịch Y có nồng độ 14,16% và tách ra 25 gam tinh thể CuSO₄.5H₂O. Biết x% là phần trăm theo khối lượng của Cu trong 25 gam mẫu quặng malachite trên. Tính giá trị của x. (Làm tròn kết quả đến hàng đơn vị).
Câu 6. Một trong các phương pháp dùng để loại bỏ ion iron trong nguồn nước nhiễm iron là sử dụng lượng vôi vừa đủ để tăng pH của nước nhiễm kết tủa ion iron khi có mặt oxygen, theo sơ đồ phản ứng:
Fe²⁺ + OH⁻ → Fe(OH)₂
Fe(OH)₂ + O₂ + H₂O → Fe(OH)₃
Một mẫu nước có hàm lượng iron cao gấp n lần so với ngưỡng cho phép quy định là 0,30 mg/L (theo QCVN01-1:2018/BYT). Giả thiết iron trong mẫu nước trên chỉ tồn tại ở hai dạng là Fe²⁺ và Fe³⁺ với tỉ lệ mol Fe²⁺ : Fe³⁺ = 1 : 3. Cần tối thiểu 149,85 gam Ca(OH)₂ để kết tủa hoàn toàn lượng iron trong 8 m³ mẫu nước trên. Giá trị của n là bao nhiêu?
Mục đích tổ chức kỳ thi Đại học năm 2025 là gì?
Căn cứ theo quy chế hiện hành của Bộ Giáo dục và Đào tạo và các văn bản hướng dẫn tổ chức kỳ thi Đại học năm 2025, mục đích của kỳ thi là:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo yêu cầu của chương trình giáo dục phổ thông.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục của địa phương và cả nước, làm cơ sở điều chỉnh nội dung, phương pháp dạy học trong nhà trường.
Thí sinh thi Đại học năm 2025 có bắt buộc thi môn Hóa học không?
Theo quy định hiện hành của Bộ Giáo dục và Đào tạo và hướng dẫn tổ chức kỳ thi tốt nghiệp Đại học năm 2025, thí sinh dự thi phải thực hiện như sau:
– Thi 3 môn bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
– Ngoài ra, thí sinh phải chọn một trong hai bài thi tổ hợp: Khoa học Tự nhiên (gồm các môn Vật lí, Hóa học, Sinh học) hoặc Khoa học Xã hội (gồm các môn Lịch sử, Địa lí, Giáo dục công dân – dành cho học sinh học chương trình giáo dục phổ thông).
Trong số các môn thi, Hóa học là một trong ba môn thuộc bài thi tổ hợp Khoa học Tự nhiên, thí sinh chỉ phải thi môn Hóa học nếu chọn tổ hợp này, không phụ thuộc vào mục đích xét tuyển đại học.
Như vậy, kỳ thi Đại học năm 2025 không bắt buộc thí sinh phải thi môn Hóa học, việc thi môn này phụ thuộc vào lựa chọn bài thi tổ hợp của thí sinh.




