Đề thi thử Đại học 2025 môn Hóa học – Trường THPT Sơn Tây là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT, nằm trong chương trình Đề thi vào Đại học.
Đề thi được xây dựng sát với cấu trúc đề minh họa 2025 của Bộ GD&ĐT, bao phủ đầy đủ các chuyên đề trọng tâm như: Este – Lipit, Amin – Amino axit, Kim loại, Phi kim, Cacbohiđrat và Hóa học đại cương. Với hệ thống câu hỏi rõ ràng, phân hóa tốt, đề giúp học sinh rèn kỹ năng tư duy, phản xạ nhanh và làm quen với áp lực thời gian trong phòng thi.
Hãy cùng Dethitracnghiem.vn khám phá đề thi này và luyện tập thật hiệu quả để bứt phá điểm số trong kỳ thi THPT Quốc gia 2025!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 THPT SƠN TÂY
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Cho alcohol có công thức cấu tạo sau: CH₃-CH(CH₃)-CH₂-CH₂-CH₂-OH. Tên theo danh pháp thay thế của alcohol đó là
A. 4-methylpentan-1-ol.
B. 3-methylbutan-2-ol.
C. 2-methylbutan-3-ol.
D. 1,1-dimethylpropan-3-ol.
Câu 2. Một loại than đá dùng cho nhà máy nhiệt điện có chứa 2% sulfur. Nếu mỗi ngày nhà máy đốt hết 100 tấn than thì một năm (365 ngày) khối lượng sulfur dioxide thải vào khí quyển là
A. 5365 tấn.
B. 1460 tấn.
C. 7154 tấn.
D. 7300 tấn.
Câu 3. Cho phổ khối lượng của một hợp chất hữu cơ A như hình vẽ: 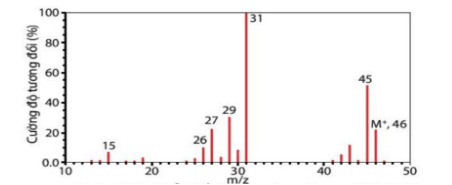 Hợp chất hữu cơ A có thể là
Hợp chất hữu cơ A có thể là
A. C₂H₆O₂.
B. C₂H₂.
C. CH₃Cl.
D. C₂H₆O.
Câu 4. Phản ứng giữa sulfur dioxide và oxygen là tỏa nhiệt:
2SO₂(g) + O₂(g) → 2SO₃(g) ΔrHo₂⁹⁸ = -197 kJ
Giá trị biến thiên enthalpy của phản ứng SO₂(g) → SO₃(g) + 1/2 O₂(g) là
A. -197 kJ.
B. -98,5 kJ.
C. +98,5 kJ.
D. +197 kJ.
Câu 5. Công thức hóa học của đinitrogen oxide là
A. NO.
B. NH₃.
C. NO₂.
D. N₂O.
Câu 6. Khi uống rượu có lẫn methanol, methanol có trong rượu được chuyển hóa ở gan tạo thành formic acid gây ngộ độc cho cơ thể, làm suy giảm thị lực và có thể gây mù. Formic acid có công thức cấu tạo là
A. HCOOH.
B. HCHO.
C. CH₃OH.
D. CH₃COOH.
Câu 7. Trong các chất sau, chất nào thuộc loại phenol?
A. CH₃CH₂OH
B. OH–C₆H₄–CH₃
C. COOH–C₆H₄–CH₃
D. OH–CH₂–C₆H₅
Câu 8. Trong các chất sau đây, chất nào có nhiệt độ sôi cao nhất?
A. CH₃CH₂OH
B. CH₃COOH
C. CH₃CHO
D. CH₃CH₂CH₂CH₃
Câu 9. Khi trùng hợp CF₂=CF₂ thu được hợp chất có tên gọi là teflon. Hợp chất teflon có đặc tính khá bền vững với nhiệt, không thấm nước và giúp giảm ma sát. Vì vậy người ta ứng dụng teflon làm
A. thuốc trừ sâu bệnh
B. thuốc giảm đau
C. chất chống dính trên chảo
D. thuốc gây mê
Câu 10. Phản ứng nào dưới đây không phải phản ứng oxi hóa – khử?
A. Cl₂ + 2NaOH → NaCl + NaClO + H₂O
B. CaCO₃ → CaO + CO₂
C. 4Fe(OH)₂ + O₂ → 2Fe₂O₃ + 4H₂O
D. 2KClO₃ → 2KCl + 3O₂
Câu 11. Cho dãy các chất: glucose, cellulose, saccharose, tinh bột, maltose. Số chất trong dãy tham gia phản ứng tráng gương là
A. 5
B. 4
D. 3
C. 2
Câu 12. Cho 0,1 mol hỗn hợp X gồm hai aldehyde no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng tác dụng với lượng dư dung dịch AgNO₃ trong NH₃, đun nóng thu được 32,4 gam Ag. Công thức của hai aldehyde trong X là
A. CH₃CHO và C₂H₅CHO
B. HCHO và C₂H₅CHO
C. C₂H₅CHO và C₃H₇CHO
D. HCHO và CH₃CHO
Câu 13. Ester được tạo thành từ phản ứng ester hoá giữa acetic acid và ethanol có công thức nào sau đây?
A. CH₃COOC₂H₅
B. CH₃COOCH₃
C. CH₃COOC₃H₇
D. C₂H₅COOCH₃
Câu 14. Xà phòng hóa hoàn toàn m gam triglyceride X trong dung dịch NaOH, thu được 9,2 gam glycerol và 88,8 gam muối. Phân tử khối của X là
A. 832
B. 884
C. 860
D. 890
Câu 15. Một hồ bơi tiêu chuẩn khi có độ pH trong nước khoảng từ 7,2 – 7,8. Mất cân bằng pH là một trong những vấn đề thường gặp ở nhiều hồ bơi. Trong trường hợp pH hồ bơi quá thấp sẽ gây kích ứng da và mắt cho người bơi. Để làm tăng pH của nước hồ bơi, hóa chất thường được sử dụng là
A. NaCl
B. H₂SO₄
C. Na₂CO₃
D. HCl
Câu 16. Khối lượng glucose cần dùng để điều chế 1 lít rượu 40° (khối lượng riêng của ethanol là 0,8 g/mL) với hiệu suất 45% là
A. 1391,3 gam
B. 626,09 gam
C. 1252,2 gam
D. 281,74 gam
Câu 17. Nguyên tử có 16p, 18n, 16e → Z và A là
A. 8 và 16
B. 16 và 32
C. 16 và 34
D. 32 và 50
Câu 18. Tiến hành chuẩn độ dung dịch NaOH chưa biết nồng độ (biết nồng độ dung dịch HCl khoảng gần 0,1 M) bằng dung dịch chuẩn HCl 0,1 M với chất chỉ thị phenolphtalein như sau:
Bước 1: Dùng pipette lấy 10 mL dung dịch HCl 0,1 M cho vào bình tam giác, thêm 1 – 2 giọt phenolphtalein.
Bước 2: Cho dung dịch NaOH vào burette, điều chỉnh dung dịch trong burette về mức 0.
Bước 3: Mở khóa burette, nhỏ từng giọt dung dịch NaOH xuống bình tam giác (lắc đều trong quá trình chuẩn độ) cho đến khi dung dịch xuất hiện màu hồng nhạt (bền trong khoảng 10 giây) thì dừng chuẩn độ.
Bước 4: Ghi lại thể tích dung dịch NaOH đã dùng.
Cho các phát biểu sau:
(a) Phương pháp này để xác định nồng độ dung dịch base hoặc dung dịch acid chưa biết nồng độ.
(b) Thí nghiệm cần lặp lại ít nhất 3 lần, lấy giá trị trung bình của 3 lần chuẩn độ.
(c) Khi kết thúc chuẩn độ, thể tích dung dịch NaOH đã sử dụng là 12,5 mL thì nồng độ NaOH ban đầu là 0,08 M.
(d) Ở bước 4, đọc thể tích dung dịch NaOH trên vạch burette mắt nhìn hướng từ trên xuống.
Số phát biểu đúng là
A. 2.
B. 1.
C. 4.
D. 3.
PHẦN II. Thí sinh trả lời các câu 1 đến câu 4. Trong mỗi ý a), b), c), d), thí sinh chọn đúng hoặc sai.
Câu 1. Hỗn hợp A gồm glucose và tinh bột. Chia hỗn hợp làm 2 phần bằng nhau:
Phần 1: Khuấy trong nước, lọc lấy dung dịch cho phản ứng với dung dịch AgNO₃ trong NH₃ thu được 2,16 gam Ag.
Phần 2: Đun nóng với dung dịch H₂SO₄ loãng. Hỗn hợp sau phản ứng được trung hòa bởi dung dịch NaOH, sau đó cho toàn bộ sản phẩm tác dụng với dung dịch AgNO₃ trong dung dịch NH₃ thu được 6,48 gam Ag.
a) Người ta lấy lượng tinh bột bằng 1/4 tinh bột có trong A đem điều chế ra ethyl alcohol, hiệu suất toàn quá trình đạt 80% thì thu được 0,032 mol alcohol.
b) Ở phần 2, mục đích của NaOH thêm vào là để trung hòa lượng acid dư sau phản ứng thủy phân tinh bột.
c) Khối lượng glucose có trong A là 1,8 gam.
d) Tổng khối lượng tinh bột và glucose trong A là 10,08 gam.
Câu 2. Oxi hóa hoàn toàn chất A chỉ tạo thành CO₂ và H₂O.
a) Trên phổ IR của A thấy có hấp thụ ở 1720 cm⁻¹ chứng tỏ trong phân tử chất A có thể có nhóm chức carboxylic acid hoặc ester hoặc ketone hoặc aldehyde.
b) Trong thành phần chất A chắc chắn có C, H và O.
c) Để nhận sự có mặt của H₂O, người ta dẫn sản phẩm qua ống chứa Cu(OH)₂ khan.
d) Phân tử khối của A luôn là số chẵn.
Câu 3. Cấu trúc của một loại triglyceride (X) được biểu diễn như sau:
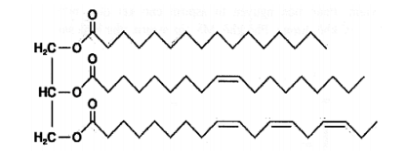
a) Thể tích khí hydrogen (ở đkc) cần dùng để chuyển hóa 128,1 gam (X) thành bơ nhân tạo là 20,8236 lít, biết hiệu suất của quá trình chuyển hóa đạt 80%.
b) (X) thuộc loại chất béo lỏng vì trong thành phần có các acid béo không no chiếm ưu thế.
c) Khi thủy phân (X) trong môi trường acid thu được sản phẩm có chứa acid béo omega-6 và omega-9.
d) Khi để lâu ngoài không khí, (X) bị khử chậm bởi oxygen tạo thành hợp chất có mùi khó chịu.
Câu 4. Cho sơ đồ phản ứng sau:
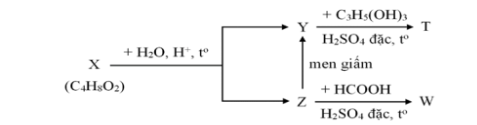
X –(+H₂, H⁺, t°)–> Y –(t°)–> Z
Y –(men giấm)–> T
Z –(+C₂H₅OH)–> W
Z –(+HCOOH, H₂SO₄ đặc, t°)–> V
(C₄H₆O₂) for Z]
Biết rằng X, Y, Z, T, W là các hợp chất hữu cơ khác nhau; T chỉ chứa một loại nhóm chức.
a) Z có trong thành phần của nước rửa tay khô có tác dụng diệt khuẩn.
b) Y có trong thành phần của giấm ăn.
c) Phần trăm khối lượng của O trong T là 36,36%.
d) Công thức phân tử của W là C₂H₄O₂.
PHẦN III. Câu hỏi yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Cho salicylic acid (2-hydroxybenzoic acid) phản ứng với acetic anhydride, thu được acetylsalicylic acid (o-CH₃COO-C₆H₄-COOH) dùng làm thuốc giảm đau (aspirin). Để phản ứng hoàn toàn với 43,2 gam acetylsalicylic acid cần vừa đủ V lít dung dịch KOH 1 M. Giá trị của V là bao nhiêu lít?
Câu 2. Nung nóng m gam hỗn hợp X gồm Mg, Al và Cu trong O₂ dư, thu được 15,1 gam hỗn hợp Y gồm các oxide. Hòa tan hết Y bằng lượng vừa đủ dung dịch gồm HCl 0,5M và H₂SO₄ 0,5M, thu được dung dịch chứa 36,6 gam muối trung hòa. Biết các phản ứng xảy ra hoàn toàn. Tính giá trị của m?
Câu 3. Cho các chất:
Có bao nhiêu chất khi bị oxi hóa bởi CuO tạo ra sản phẩm có nhóm chức aldehyde?
Câu 4. Cho phương trình hóa học của các phản ứng được đánh số thứ tự từ 1 tới 4 dưới đây:
(1) CH₃ – CH = O + 2[Ag(NH₃)₂]OH → CH₃ – COONH₄ + 2Ag + 3NH₃ + H₂O
(2) CH₃ – CH = O + 3I₂ + 4NaOH → CHI₃↓ + H-COONa + 3NaI + 3H₂O
(3) C₆H₁₂O₆ enzyme→ 2C₂H₅OH + 2CO₂
(4) (C₆H₁₀O₅)n + nH₂O enzyme→ nC₆H₁₂O₆
Gán số thứ tự phương trình hóa học của các phản ứng theo tên gọi: Phản ứng với thuốc thử Tollens, phản ứng lên men rượu, phản ứng tạo iodoform, phản ứng thủy phân và sắp xếp theo trình tự thành dãy bốn số (ví dụ: 1234, 4321,…).
Câu 5. Hỗn hợp X gồm CH₃COOH và C₂H₅COOH (tỉ lệ mol 2:1). Lấy 6,4 gam hỗn hợp X tác dụng với 5,75 gam C₂H₅OH (có xúc tác H₂SO₄ đặc) thu được b gam hỗn hợp ester (hiệu suất bằng 80%, các acid phản ứng với tốc độ như nhau). Giá trị của b bằng bao nhiêu?
Câu 6. Một dung dịch có chứa các ion: Na⁺ (0,2 mol), Mg²⁺ (0,1 mol), Ca²⁺ (0,05 mol), NO₃⁻ (0,15 mol) và Cl⁻ (x mol). Tính giá trị của x?
Mục đích tổ chức kỳ thi Đại học năm 2025 là gì?
Căn cứ theo quy chế hiện hành của Bộ Giáo dục và Đào tạo và các văn bản hướng dẫn tổ chức kỳ thi Đại học năm 2025, mục đích của kỳ thi là:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo yêu cầu của chương trình giáo dục phổ thông.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục của địa phương và cả nước, làm cơ sở điều chỉnh nội dung, phương pháp dạy học trong nhà trường.
Thí sinh thi Đại học năm 2025 có bắt buộc thi môn Hóa học không?
Theo quy định hiện hành của Bộ Giáo dục và Đào tạo và hướng dẫn tổ chức kỳ thi tốt nghiệp Đại học năm 2025, thí sinh dự thi phải thực hiện như sau:
– Thi 3 môn bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
– Ngoài ra, thí sinh phải chọn một trong hai bài thi tổ hợp: Khoa học Tự nhiên (gồm các môn Vật lí, Hóa học, Sinh học) hoặc Khoa học Xã hội (gồm các môn Lịch sử, Địa lí, Giáo dục công dân – dành cho học sinh học chương trình giáo dục phổ thông).
Trong số các môn thi, Hóa học là một trong ba môn thuộc bài thi tổ hợp Khoa học Tự nhiên, thí sinh chỉ phải thi môn Hóa học nếu chọn tổ hợp này, không phụ thuộc vào mục đích xét tuyển đại học.
Như vậy, kỳ thi Đại học năm 2025 không bắt buộc thí sinh phải thi môn Hóa học, việc thi môn này phụ thuộc vào lựa chọn bài thi tổ hợp của thí sinh.




