Đề thi thử Đại học 2025 môn Hóa học trường THPT Thuận Thành là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Đề thi được biên soạn bởi trường THPT Thuận Thành – một trong những trường có truyền thống học tập tốt tại địa phương, với mục tiêu giúp học sinh lớp 12 luyện tập và làm quen với cấu trúc đề thi chuẩn hóa của Bộ GD&ĐT. Đề thi bao quát toàn bộ chương trình hóa học THPT, đặc biệt nhấn mạnh vào các chuyên đề Este – Lipit, Amin – Amino axit – Protein, Kim loại và hợp chất, Phản ứng oxi hóa – khử, Cân bằng hóa học – điện phân, bài tập đồ thị và nhận biết hóa chất.
Những kiến thức trọng tâm học sinh cần chuẩn bị để làm tốt đề này:
- Thành thạo các dạng bài nhận biết, chuỗi phản ứng và bài toán hỗn hợp.
- Áp dụng nhuần nhuyễn các phương pháp giải nhanh: bảo toàn khối lượng, bảo toàn electron, bảo toàn nguyên tố.
- Rèn kỹ năng đọc dữ liệu và phân tích bảng – biểu đồ trong câu hỏi mang tính ứng dụng thực tiễn.
Hãy cùng Dethitracnghiem.vn tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 5 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐẠI HỌC MÔN HÓA HỌC NĂM 2025 THPT THUẬN THÀNH






Phần I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Cho cấu tạo của phân tử ethylene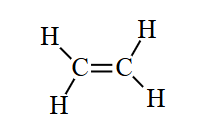 Chọn phát biểu sai
Chọn phát biểu sai
A. Trong phân tử ethylene, các góc liên kết xấp xỉ 120⁰.
B. Carbon có hóa trị IV.
C. Tổng số liên kết sigma trong phân tử ethylene là 5.
D. C₂H₄ có đồng phân hình học.
Câu 2. Cho 15,75 gam một carboxylic acid (X) tác dụng vừa đủ với 350 mL dung dịch KOH 1M. X là?
A. HCOOH.
B. CH₃COOH.
C. HOOC-CH₂-COOH.
D. HOOC- COOH.
Câu 3. Cho các chất mạch không phân nhánh có công thức sau: C₄H₉OH (1), C₃H₇COOH (2), CH₃COOC₂H₅ (3). Dãy các chất được sắp xếp theo chiều tăng dần nhiệt độ sôi là
A. (3)<(2)<(1).
B. ((1)<(2)<(3).
C. (2)<(3)<(1).
D. (3)<(1)<(2).
Câu 4. Chất nào sau đây thuộc loại chất béo:
A. (CH₃COO)₃C₃H₅.
B. (C₁₆H₃₃COO)₂C₂H₄.
C. (C₁₅H₃₁COO)₃C₃H₇.
D. (C₁₇H₂₉COO)₃C₃H₅.
Câu 5. Xét trạng thái cân bằng của một phản ứng thuận nghịch. Khi đó
A. Cả phản ứng thuận và phản ứng nghịch đều tạm ngừng xảy ra.
B. Tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
C. Nồng độ các chất trong hệ phản ứng bằng nhau.
D. Tổng khối lượng các chất tham gia phản ứng bằng tổng khối lượng các chất sản phẩm.
Câu 6. Sulfuric acid là một hóa chất quan trọng trong công nghiệp, được dùng để sản suất phân bón, khai khoáng, chế biến dầu mỏ … Trong công nghiệp sulfuric acid được sản xuất với nồng độ từ 70% đến 98% từ sulfur, bằng quá trình tiếp xúc và thiết bị phản ứng dòng liên tục qua 3 giai đoạn sau đây:
Giai đoạn 1: Đốt sulfur với không khí khô và sạch tạo ta chất X.
Giai đoạn 2: Nung X với oxygen dư trong lò tầng ở 450⁰C-500⁰C, có V₂O₅ xúc tác thu được chất Y.
Giai đoạn 3: Dùng chất Z để hấp thụ Y, tạo ra chất T rồi cho T kết hợp với lượng nước vừa đủ tạo ra H₂SO₄ có nồng độ như yêu cầu sản xuất.
Chất Z và chất T nêu trên lần lượt là:
A. H₂SO₄ đặc và oleum.
B. H₂SO₄ loãng và oleum.
C. H₂O và H₂SO₄ > 98%
D. H₂O và oleum.
Câu 7. Sử dụng 1 tạ chất béo trung tính chứa 65% tristearin, còn lại là tripalmitin về khối lượng để sản xuất xà phòng. Loại xà phòng tạo ra này chứa 72% là muối potassium của acid béo, còn lại là các chất phụ gia như: tạo màu, tạo hương thơm, tạo bọt, tạo độ rắn…. Biết mỗi bánh xà phòng nặng 150 gam. Số bánh xà phòng thu được là
A. 968 bánh.
B. 1010 bánh.
C. 1008 bánh.
D. 956 bánh.
Câu 8. Cho alkanol tác dụng với alkanoic acid có H₂SO₄ đặc làm xúc tác tạo ra ester có công thức phân tử chung là:
A. \( \text{C}_n\text{H}_{2n}\text{O}_2. (n \ge 2) \)
B. \( \text{C}_n\text{H}_{2n-2}\text{O}_2. (n \ge 2) \)
C. \( \text{C}_n\text{H}_{2n}\text{O}_2. (n \ge 1) \)
D. \( \text{C}_n\text{H}_{2n+2}\text{O}_2. (n \ge 2) \)
Câu 9. Trong công nghiệp, NH₃ được sản xuất trong tháp tiếp xúc, theo phương trình hóa học sau:
N₂ + 3H₂ ⇌ 2NH₃. ΔrH = -91,8 kJ.
(Quá trình này thực hiện ở 450⁰ – 500⁰C, dưới áp suất 250 atm – 300 atm, có Fe xúc tác).
Khi phản ứng đang ở trạng thái cân bằng, tác động nào sau đây làm cân bằng chuyển dịch theo chiều thuận.
A. Thêm chất xúc tác.
B. Tăng nhiệt độ.
C. Tăng áp suất.
D. Giảm áp suất.
Câu 10. Chất X thỏa mãn các điều kiện sau: Khi nhúng quỳ tím vào dung dịch chất X thấy quỳ chuyển màu đỏ. X có phản ứng tráng bạc. Tên gọi của X là:
A. formic acid.
B. acetaldehyde.
C. acetic acid.
D. formaldehyde.
Câu 11. Khi cho quỳ tím vào dung dịch nào sau đây, quỳ sẽ chuyển thành màu xanh
A. Na₂CO₃.
B. NaF.
C. FeCl₃.
D. NaNO₃.
Câu 12. Xà phòng hóa hoàn toàn một triglyceride (X) bằng dung dịch KOH vừa đủ, thu được 9,2 gam glycerol và 88,2 gam muối của một acid béo no. Tên gọi của X là:
A. trilaurin.
B. triolein.
C. tripalmitin.
D. tristearin.
Câu 13. Trong hợp chất hữu cơ nhất thiết phải chứa nguyên tố nào?
A. oxygen.
B. nitrogen.
C. carbon.
D. hydrogen.
Câu 14. Phát biểu đúng về chất béo.
A. Chứa ba chức ester.
B. Hydrogen hóa tristearin ở điều kiện thích hợp thu được triolein.
C. Tan tốt trong nước.
D. Khi thủy phân trong môi trường kiềm chỉ tạo chi tạo một muối.
Câu 15. Phenol (C₆H₅−OH ) và ethanol (C₂H₅OH) đều tác dụng với chất nào sau đây
A. Na (s).
B. CH₃−OH (l).
C. NaOH (aq).
D. CH₃−COOH (l).
Câu 16. Những vùng đất bị nhiễm phèn, do trong keo đất chứa nhiều ion Al³⁺, Fe³⁺ và NH₄⁺, làm cho pH của đất thấp, cây lúa kém phát triển. Người ta thường dùng chất nào sau đây bón cho đất để tăng pH của đất.
A. CaCO₃ (bột).
B. CaO (bột).
C. NH₄NO₃ (viên nhỏ).
D. CaSO₄ (bột).
Câu 17. Nhóm các khí nào sau đây trong không khí khi vượt quá mức cho phép sẽ gây ra hiện tượng mưa acid:
A. H₂; CO; CH₄.
B. NH₃; H₂S; O₃.
C. CO₂; O₃; N₂O.
D. SO₂; NO; NO₂.
Câu 18. Chất nào sau đây là dẫn xuất halogen của hydrocarbon?
A. CH₃−MgCl.
B. CH₃−CO−Cl.
C. CHCl₃.
D. Cl−CH₂−CH₂−OH.
Phần II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 6. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Đốt cháy hoàn toàn 8,8 gam hợp chất hữu cơ A đơn chức, có MA ≤ 60 gam/mol, thu được 0,4 mol CO₂ và 0,4 mol H₂O.
a) Công thức phân tử của A là C₂H₄O₂
b) Từ A có thể điều chế được acetic acid bằng một phản ứng trực tiếp
c) Số mol O₂ đã tham gia phản ứng là 0,5 mol
d) Vì sản phẩm cháy có \( n_{\text{CO}_2} = n_{\text{H}_2\text{O}} \) nên A là hợp chất hữu cơ no đơn chức, mạch hở
Câu 2. Trong dung dịch muối AlCl₃, tồn tại các cân bằng hóa học sau:
Al³⁺ + 3H₂O ⇌ Al(OH)₃ + 3H⁺ (1)
Khi thêm hỗn hợp KIO₃ và KI vào dung dịch AlCl₃ thì xảy ra phương trình hóa học:
IO₃⁻ + 5 I⁻ + 6H⁺ → 3I₂ + 3H₂O (2)
a) Khi thêm hỗn hợp KIO₃ và KI vào dung dịch AlCl₃ thì cân bằng (1) chuyển dịch theo chiều thuận, tạo thành Al(OH)₃ dạng keo màu trắng.
b) Trong phòng thí nghiệm, để tránh sự thủy phân của Al³⁺ trong dung dịch người ta thường thêm vài giọt dung dịch acid mạnh.
c) Khi cho dung dịch AlCl₃ tác dụng với lượng dư dung dịch NaOH cũng thu được kết tủa Al(OH)₃ dạng keo màu trắng.
d) Dung dịch muối AlCl₃ có pH > 7.
Câu 3. Hàng nghìn các dẫn xuất halogen được tách ra từ nhiều loại sinh vật biển khác nhau như rong, tảo biển, san hô,… Chúng có các hoạt tính sinh học rất quý giá như khả năng điều trị bệnh hung thư và nhiều bệnh khác. Cho công thức cấu tạo của dẫn xuất halogen Laurencia như sau: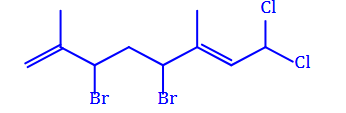 Dẫn xuất halogen tách ra từ tảo biển đỏ chi Laurencia có tác dụng chống ung thư vòm họng
Dẫn xuất halogen tách ra từ tảo biển đỏ chi Laurencia có tác dụng chống ung thư vòm họng
a) Phần trăm khối lượng của nguyên tố bromine trong dẫn xuất halogen trên bằng 43,8356%.
b) Công thức phân tử của dẫn xuất halogen là C₁₁H₁₆ClBr₂.
c) Dẫn xuất halogen trên có tên là 1,1-dichloro-4,6-dibromo-3,7-dimethylocta-1,6-diene.
d) Số liên kết pi (π) trong phân tử dẫn xuất halogen trên bằng 1.
Câu 4. Cho salicylic acid (hay 2-hydroxybenzoic acid) phản ứng với methyl alcohol có mặt sulfuric acid làm xúc tác, thu được methyl salicylate (C₈H₈O₃) dùng làm chất giảm đau (có trong miếng dán giảm đau khi vận động hoặc chơi thể thao).
a) Phản ứng giữa salicylic acid với methyl alcohol có mặt H₂SO₄ đặc làm xúc tác là phản ứng thuận nghịch.
b) Nhiệt độ sôi của methyl salicylate cao hơn của salicylic acid.
c) 1 mol methyl salicylate có thể tác dụng tối đa với 1 mol NaOH.
d) Công thức cấu tạo của salicylic acid là o-HO-C₆H₄-COOH.
Phần III. Câu hỏi trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Ammonia là một chất khí, không màu và có mùi khai. Phân tử ammonia gồm một nguyên tử nitrogen liên kết với ba nguyên tử hydrogen tạo thành hình chóp với đáy là ba nguyên tử hydrogen. Ammonia cũng là hóa chất quan trọng, được sử dụng rộng rãi trong nhiều ngành công nghiệp khác nhau. Cho công thức Lewis và dạng hình học của ammonia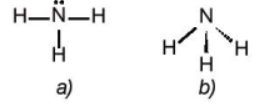 Trong công nghiệp, ammonia được điều chế bằng phản ứng nhiệt hóa học sau
Trong công nghiệp, ammonia được điều chế bằng phản ứng nhiệt hóa học sau
N₂(g) + 3H₂(g) ⇌ 2NH₃(g) ΔrH⁰₂₉₈ = −91,8kJ
Cho các phát biểu sau
(1) Các nguyên tử trong phân tử ammonia đều có lớp vỏ electron thỏa mãn quy tắc octet.
(2) Phản ứng tổng hợp ammonia là phản ứng tỏa nhiệt.
(3) Số oxi hóa của nitrogen trong phân tử ammonia bằng +3.
(4) Khí ammonia tan tốt trong nước vì ammonia có tính base.
Có bao nhiêu phát biểu đúng
Câu 2. Formic acid là một chất lỏng, mùi xốc mạnh và gây bỏng da, acid này được chưng cất lần đầu từ loài kiến lửa có tên là Formicarufa. Nếu một con kiến lửa chứa 3,75.10⁻³ ml formic acid, biết khi kiến cắn sẽ tiêm 80% lượng formic acid có trong cơ thể. Để làm giảm lượng formic acid trong vết cắn, bác sĩ thường dùng thuốc có chứa thành phần là sodium hydrogencarbonate (NaHCO₃). Tính khối lượng sodium hydrogencarbonate (miligam) cần dùng để trung hoà hoàn toàn lượng formic acid từ vết một con kiến cắn một lần? (biết khối lượng riêng của formic acid là 1,22 g/cm³) (làm tròn kết quả đến phần trăm).
Câu 3. Chỉ số pH của các dịch trong cơ thể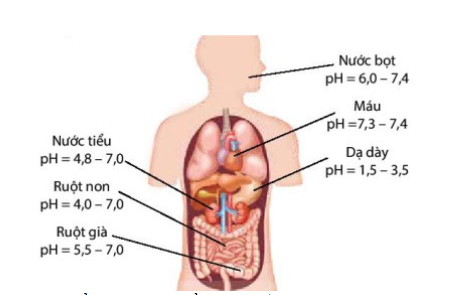
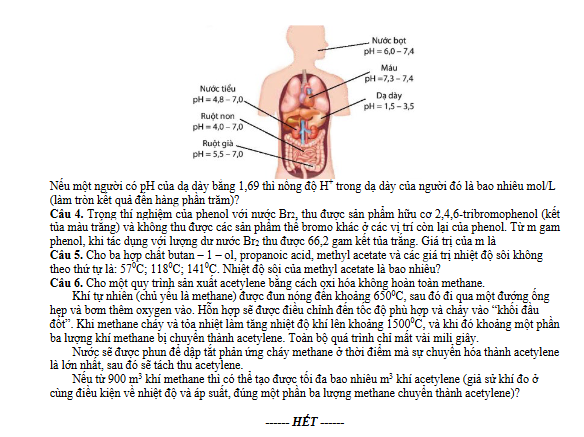
Nếu một người có pH của dạ dày bằng 1,69 thì nồng độ H⁺ trong dạ dày của người đó là bao nhiêu mol/L (làm tròn kết quả đến hàng phần trăm)?
Câu 4. Trong thí nghiệm của phenol với nước Br₂, thu được sản phẩm hữu cơ 2,4,6-tribromophenol (kết tủa màu trắng) và không thu được các sản phẩm thế bromo khác ở các vị trí còn lại của phenol. Từ m gam phenol, khi tác dụng với lượng dư nước Br₂ thu được 66,2 gam kết tủa trắng. Giá trị của m là
Câu 5. Cho ba hợp chất butan – 1 – ol, propanoic acid, methyl acetate và các giá trị nhiệt độ sôi không theo thứ tự là: 57⁰C; 118⁰C; 141⁰C. Nhiệt độ sôi của methyl acetate là bao nhiêu?
Câu 6. Cho một quy trình sản xuất acetylene bằng cách oxi hóa không hoàn toàn methane. Khí tự nhiên (chủ yếu là methane) được đun nóng đến khoảng 650⁰C, sau đó đi qua một đường ống hẹp và bơm thêm oxygen vào. Hỗn hợp sẽ được điều chỉnh đến tốc độ phù hợp và chảy vào “khối đầu đốt”. Khí methane cháy và tỏa nhiệt làm tăng nhiệt độ khi lên khoảng 1500⁰C, và khi đó khoảng một phần ba lượng khí methane bị chuyển thành acetylene. Toàn bộ quá trình chỉ mất vài mili giây. Nước sẽ được phun để dập tắt phản ứng cháy methane ở thời điểm mà sự chuyển hóa thành acetylene là lớn nhất, sau đó sẽ tách thu acetylene.
Từ 900 m³ khí methane thì có thể tạo được tối đa bao nhiêu m³ khí acetylene (giả sử khí đo ở cùng điều kiện về nhiệt độ và áp suất, đúng một phần ba lượng methane chuyển thành acetylene)?
Mục đích tổ chức kỳ thi Tốt nghiệp THPT năm 2025 là gì?
Căn cứ vào các văn bản chỉ đạo và hướng dẫn của Bộ Giáo dục và Đào tạo, kỳ thi Tốt nghiệp THPT năm 2025 được tổ chức nhằm các mục tiêu chính sau:
– Đánh giá kết quả học tập của học sinh sau 12 năm theo chương trình giáo dục phổ thông mới.
– Lấy kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh cho các trường đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục của các địa phương và toàn quốc, từ đó điều chỉnh nội dung và phương pháp giảng dạy trong nhà trường.
Thí sinh thi tốt nghiệp THPT năm 2025 có bắt buộc phải thi môn Hóa học không?
Theo quy định hiện hành của Bộ GD&ĐT, thí sinh dự thi Tốt nghiệp THPT năm 2025 phải tham gia ba bài thi bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
Ngoài ra, thí sinh cần chọn một trong hai bài thi tổ hợp:
– Tổ hợp Khoa học Tự nhiên (KHTN): gồm các môn Vật lí, Hóa học, Sinh học.
– Tổ hợp Khoa học Xã hội (KHXH): gồm các môn Lịch sử, Địa lí, Giáo dục công dân (áp dụng với học sinh chương trình giáo dục phổ thông hiện hành).
Trong bài thi tổ hợp KHTN, môn Hóa học là một trong ba môn thành phần. Tuy nhiên, thí sinh không bắt buộc phải thi môn Hóa học, trừ khi đăng ký thi tổ hợp KHTN để xét tốt nghiệp hoặc xét tuyển đại học, cao đẳng vào các ngành yêu cầu môn này.
Do đó, Đề thi thử tốt nghiệp THPT 2025 môn Hóa học – Trường THPT Thuận Thành là tài liệu ôn luyện hữu ích dành cho các học sinh lựa chọn tổ hợp KHTN. Đề thi giúp các em củng cố kiến thức, đánh giá năng lực hiện tại và nâng cao kỹ năng làm bài, từ đó chuẩn bị thật tốt cho kỳ thi chính thức sắp tới.




