Đề thi thử đánh giá năng lực môn Hóa học 2025 – Đề số 1 là một trong những đề thi thuộc Trắc nghiệm thi thử Tốt nghiệp THPT trong chương trình Tổng hợp đề thi thử môn Hóa học THPT.
Đây là dạng đề thi được Bộ Giáo dục và Đào tạo công bố nhằm giúp học sinh lớp 12 định hướng ôn tập đúng trọng tâm cho kỳ thi tốt nghiệp THPT môn Hóa học năm 2025. Đề minh họa này mang tính chất tham khảo nhưng có độ sát với đề thi thật rất cao, phản ánh rõ cấu trúc, mức độ phân hóa, và dạng câu hỏi có thể gặp trong kỳ thi chính thức.
Các kiến thức cốt lõi để giải được đề thi bao gồm:
- Hóa học lớp 12 chiếm tỉ trọng lớn, với các chương như: Este – Lipit, Amin – Amino axit – Protein, Polime, Cấu tạo phân tử, Phản ứng oxi hóa – khử, Kim loại và phi kim.
- Một phần kiến thức lớp 11, chủ yếu ở chương trình Hóa học hữu cơ và vô cơ cơ bản (axit, bazơ, muối…).
- Các câu hỏi thường xoay quanh các kỹ năng tính toán hóa học, viết phương trình phản ứng, nhận diện chất, biện luận hóa học, cùng với vận dụng thí nghiệm thực tiễn.
Hãy cùng Dethitracnghiem.vn tìm hiểu về đề thi này và tham gia làm kiểm tra ngay lập tức!
- Số trang: 4 trang
- Hình thức: 70% trắc nghiệm – 30% vận dụng
- Thời gian làm bài: 50 phút (không kể thời gian phát đề)
ĐỀ THI THỬ ĐÁNH GIÁ NĂNG LỰC MÔN HÓA HỌC NĂM 2025 – ĐỀ SỐ 1








PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1: Liên kết kim loại là liên kết được hình thành do
A. các electron tự do chuyển động quanh vị trí cân bằng giữa nguyên tử kim loại và ion dương kim loại ở các nút mạng.
B. sự cho và nhận electron giữa các nguyên tử kim loại.
C. sự góp chung electron giữa các nguyên tử kim loại.
D. lực hút tĩnh điện của ion dương kim loại này với nguyên tử kim loại.Tính chất nào sau đây không phải là tính chất chung của kim loại?
Câu 2: Lactic acid là một chất có một trong nhiều thực phẩm. Khi tập luyện thể thao quá độ, cơ thể sản sinh ra Lactic acid gây đau nhức cơ bắp. Công thức cấu tạo của lactic acid như hình bên. Trong phân tử lactic acid có các nhóm chức nào sau đây?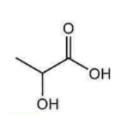
A. Alcohol và carboxylic.
B. Ester và alcohol.
C. Ketone và alcohol.
D. Alcohol và aldehyde.
Câu 3: Cho sơ đồ mô tả cơ chế giặt rửa của xà phòng như sau: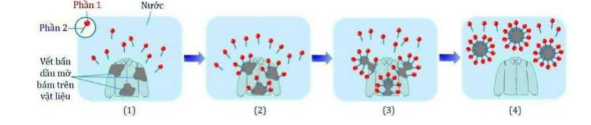 Phát biểu nào sau đây là đúng?
Phát biểu nào sau đây là đúng?
A. Phần 1 là phần kị nước, phần 2 là phần ưa nước.
B. Nếu sử dụng xà phòng với nước cứng (chứa nhiều ion Ca²⁺, Mg²⁺) thì cũng không ảnh hưởng đến chất lượng vải, đồng thời làm tăng tác dụng giặt rửa của xà phòng.
C. Phân tử xà phòng có khả năng xâm nhập vào vết bẩn dầu mỡ nhờ gốc kị nước.
D. Xà phòng bị thủy phân trong môi trường kiềm.
Câu 4: Cho các phát biểu sau:
(a) Có thể dùng nước bromine để phân biệt glucose và fructose.
(b) Trong môi trường acid, glucose và fructose có thể chuyển hoá lẫn nhau.
(c) Có thể phân biệt glucose và fructose bằng phản ứng với dung dịch AgNO₃ trong NH₃.
(d) Trong dung dịch, glucose và fructose đều hoà tan Cu(OH)₂ cho dung dịch màu xanh lam.
Số phát biểu đúng là :
A. 5.
B. 2.
C. 4.
D. 3.
Câu 5: Cho hai nguyên tử X và Y có số hiệu nguyên tử (Z) lần lượt là 9 và 20. Chọn phát biểu đúng :
A. X và Y liên kết với nhau bằng liên kết ion, tạo ra phân tử YX₂.
B. X và Y liên kết với nhau bằng liên kết ion, tạo ra phân tử X₂Y.
C. X và Y liên kết với nhau bằng liên kết cộng hóa trị, tạo ra phân tử XY₂.
D. X và Y liên kết với nhau bằng liên kết kim loại, tạo ra phân tử X₂Y.
Câu 6: Polymer nào sau đây không được dùng làm chất dẻo?
A. Polyisoprene.
B. Poly(vinyl chloride).
C. Polystyrene.
D. Poly(phenol formaldehyde).
Câu 7: Phân tử saccharose được cấu tạo gồm
A. 1 đơn vị α-glucose và 1 đơn vị β-glucose liên kết với nhau bằng liên kết 1,2-glycoside.
B. 2 đơn vị α-glucose liên kết với nhau bằng liên kết 1,2-glycoside.
C. 1 đơn vị α-glucose và 1 đơn vị β-fructose liên kết với nhau bằng liên kết 1,4-glycoside.
D. 1 đơn vị α-glucose và 1 đơn vị β-fructose liên kết với nhau bằng liên kết 1,2-glycoside.
Câu 8: Công thức cấu tạo thu gọn của ethylmethylamine là
A. CH₃NHCH₃.
B. CH₃CH₂NHCH₂CH₃.
C. CH₃NHCH₂CH₂CH₃.
D. CH₃CH₂NHCH₃.
Câu 9: Chất nào sau đây thuộc loại polysaccharide?
A. Glucose.
B. Saccharose.
C. Maltose.
D. Cellulose.
Câu 10: Thành phần chính của xà phòng là
A. muối của acid béo.
B. muối của acid vô cơ.
C. muối sodium hoặc potassium của acid béo.
D. muối sodium hoặc potassium của acid.
Câu 11: Chọn phát biểu sai :
A. Các α-amino acid tạo nên các loại protein cho cơ thể sống.
B. Amino acid là hợp chất hữu cơ tạp chức.
C. Các dung dịch amino acid đều làm giấy quỳ tím chuyển sang màu đỏ.
D. Amino acid có tính chất lưỡng tính.
Câu 12: Một thí nghiệm được mô tả như hình dưới đây: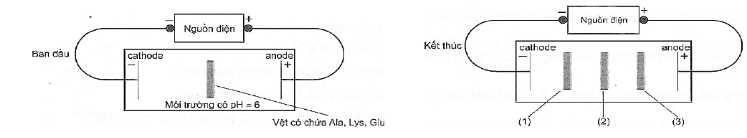 Thứ tự các amino acid ứng các vệt được đánh dấu (1), (2), (3) là
Thứ tự các amino acid ứng các vệt được đánh dấu (1), (2), (3) là
A. Glu, Ala, Lys.
B. Lys, Ala, Glu.
C. Ala, Lys, Glu.
D. Lys, Glu, Ala.
Câu 13: Dãy gồm các chất đều không tan trong nước ở 20°C là
A. BaCO₃, CaCO₃, SrCO₃.
B. MgSO₄, CaSO₄, SrSO₄.
C. MgCl₂, CaCl₂, SrCl₂.
D. Mg(NO₃)₂, Ca(NO₃)₂, Sr(NO₃)₂.
Câu 14: Một số loại thực vật chỉ phát triển tốt ở môi trường có pH phù hợp, việc nghiên cứu pH của đất rất quan trọng trong nông nghiệp. Một số loại cây trồng phù hợp với đất có giá trị pH cho trong bảng sau: Phân đạm NH₄NO₃ thích hợp để bón liên tục trong thời gian dài cho đất trồng các loại cây nào sau đây?
Phân đạm NH₄NO₃ thích hợp để bón liên tục trong thời gian dài cho đất trồng các loại cây nào sau đây?
A. Cải thảo và hành tây.
B. Chè và thanh long.
C. Cải thảo, hành tây và chè.
D. Cải thảo, hành tây, chè và thanh long.
Câu 15: Thực hiện các thí nghiệm:
(a) nhúng thanh zinc (Zn) vào dung dịch H₂SO₄ loãng;
(b) nhúng thanh iron (Fe) có tạp chất copper (Cu) vào dung dịch H₂SO₄ loãng;
(c) nhúng thanh aluminium (Al) có lớp silver (Ag) phủ kín bề mặt vào dung dịch HCl ;
(d) nhúng thanh iron (Fe) tráng thiếc (Sn) bị xước sâu vào tới lớp iron vào dung dịch H₂SO₄ loãng ;
(đ) miếng gang (chứa Fe và C) để trong không khí ẩm.
Số thí nghiệm xảy ra sự ăn mòn điện hóa là
A. 3.
B. 4.
C. 5.
D. 6.
Câu 16: Cho các phát biểu :
(a) Trong phân tử của các alkane chỉ có các liên kết đơn.
(b) Trong phân tử của các alkene chỉ có 1 liên kết pi (π).
(c) Tất cả các alkyne đều phản ứng với dung dịch AgNO₃ trong NH₃ tạo kết tủa màu vàng.
(d) Toluene có phản ứng với dung dịch KMnO₄ ở nhiệt độ thường.
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 17: Một pin điện hoá được thiết lập từ hai điện cực tạo bởi hai cặp oxi hoá – khử là M²⁺/M và Ag⁺/Ag.
Cho biết: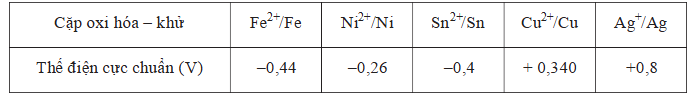 Nếu M là một trong số các kim loại: Fe, Ni, Sn, Cu thì sức điện động chuẩn lớn nhất của pin bằng bao nhiêu volt (V)?
Nếu M là một trong số các kim loại: Fe, Ni, Sn, Cu thì sức điện động chuẩn lớn nhất của pin bằng bao nhiêu volt (V)?
A. 1,56.
B. 1,06.
C. 1,24.
D. 1,14.
Câu 18: Cho hai kim loại X và Y với thế điện cực chuẩn là E°X²⁺/X = -1,18 V và E°Y²⁺/Y = -0,25 V.
Cho các phát biểu :
(a) Tính oxi hóa của Y²⁺ > X²⁺;
(b) Tính khử X > Y ;
(c) Có thể xảy ra phản ứng : X + Y²⁺ → X²⁺ + Y;
(d) Pin điện hóa X-Y có anode là điện cực làm bằng kim loại X.
Số phát biểu đúng là
A. 3.
B. 4.
C. 5.
D. 6.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào cốc thủy tinh chịu nhiệt khoảng 5 gam dầu dừa và 10 mL dung dịch NaOH 4%.
Bước 2: Đun sôi nhẹ hỗn hợp, liên tục khuấy đều bằng đũa thủy tinh khoảng 30 phút và thỉnh thoảng thêm nước cất để giữ cho thể tích hỗn hợp không đổi. Để nguội hỗn hợp.
Bước 3: Rót vào hỗn hợp 15 – 20 mL dung dịch NaCl bão hòa, nóng, khuấy nhẹ rồi để yên.
a) Sau bước 3, thấy có lớp chất rắn màu trắng nổi lên là glycerol.
YCCĐ: Thực hiện được (hoặc quan sát video) thí nghiệm về phản ứng xà phòng hóa chất béo.
b) Vai trò của dung dịch NaCl bão hòa ở bước 3 là để tách muối sodium của acid béo ra khỏi hỗn hợp.
c) Ở bước 2, nếu không thêm nước cất thì hỗn hợp bị cạn khô thì phản ứng thủy phân không xảy ra.
d) Trong công nghiệp, phản ứng ở thí nghiệm trên được ứng dụng để sản xuất xà phòng và glycerol.
Câu 2. Poly(methyl methacrylate) được viết tắt là PMMA, là một loại nhựa nhiệt dẻo trong suốt thường được sử dụng ở dạng tấm, miếng như một vật liệu nhẹ, khó bể vỡ để thay thế cho thủy tinh.
a) Đun nóng methyl methacrylate với dung dịch NaOH thu được muối và alcohol.
b) Một phân tử methyl methacrylate có 2 liên kết pi (π).
c) PMMA được điều chế bằng phản ứng trùng ngưng.
d) Để sản xuất được 10 tấn PMMA bằng phản ứng trùng hợp methyl methacrylate cần sử dụng 12,5 tấn nguyên liệu methyl methacrylate? Biết hiệu suất của phản ứng là 80%.
Câu 3. Tinh luyện đồng (Cu) bằng phương pháp điện phân được tiến hành như sau: Các khối đồng có độ tinh khiết thấp được gắn với cực dương (anode) của nguồn điện; các tấm đồng mỏng có độ tinh khiết cao được gắn với cực âm (cathode) của nguồn điện. Dung dịch điện phân là dung dịch CuSO₄. Sơ đồ bể điện phân như hình bên.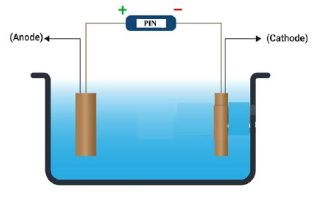
a) Tại anode chủ yếu xảy ra quá trình oxi hoá H₂O thành khí O₂ và H₂.
b) Các tạp chất không bị điện phân sẽ được giữ lại tại anode.
c) Nồng độ ion Cu²⁺ trong dung dịch không đổi trong quá trình điện phân.
d) Khối lượng Cu tan ra từ anode bằng khối lượng Cu bám vào cathode.
Câu 4. Các chất AgCl và Cr(OH)₃ không tan trong nước, nhưng trong dung dịch ammonia lại tạo ra những phức chất tan.
a) Trạng thái số oxi hóa thường gặp của chromium là +3, +6.
b) Biết số hiệu nguyên tử của Cr là 24. Ở trạng thái cơ bản, nguyên tử Cr có 6 electron độc thân.
c) Phức chất tạo bởi Cr(OH)₃ và NH₃ có công thức hóa học là Cr(NH₃)₆₃.
d) Trong phức chất [Ag(NH₃)₂]Cl, liên kết giữa NH₃ và Ag⁺ là liên kết cho nhận.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Điện phân nóng chảy hỗn hợp gồm Al₂O₃ (10%) và cryolite (90%) với anode là than cốc và cathode là than chì. Sau thời gian điện phân thu được 5,4 tấn Al tại cathode và hỗn hợp khí tại anode gồm CO₂ (80% theo thể tích) và CO (20% theo thể tích). Giả thiết không có thêm sản phẩm nào được sinh ra trong quá trình điện phân. Tính khối lượng carbon (theo tấn) đã bị oxi hoá tại anode. (Kết quả làm tròn đến hàng đơn vị).
Câu 2. Xà phòng hoá hoàn toàn 17,24 gam triglyceride cần vừa đủ dung dịch hòa tan 0,06 mol NaOH. Cô cạn dung dịch, sau phản ứng thu được khối lượng muối là bao nhiêu gam? (Kết quả làm tròn đến hàng phần mười).
Câu 3. Ứng với công thức phân tử là C₄H₉O₂ có bao nhiêu đồng phân đơn chức, mạch hở, có phản ứng với dung dịch NaOH tạo muối?
Câu 4. Cho các thí nghiệm sau :
(1) Cho aniline tác dụng nước bromine
(2) Cho dung dịch methyl amine tác dụng Cu(OH)₂ rắn
(3) Đun nóng Gly-Gly-Ala với dung dịch HCl lấy dư
(4) Cho hexamethylenediamine tác dụng với adipic acid để điều chế nylon-6,6.
Gán số thứ tự của các phản ứng xảy ra trong các quá trình trên theo tên gọi : thủy phân, thế, tạo phức, trùng ngưng và sắp xếp theo trình tự dãy 4 số (ví dụ : 2314 hoặc 1342…).
Câu 5. Ở điều kiện chuẩn, cần phải đốt cháy hoàn toàn bao nhiêu gam khí CH₄ để cung cấp nhiệt cho phản ứng nhiệt phân CaCO₃ tạo thành 56 gam CaO? Giả thiết hiệu suất các quá trình đều là 100%. Phương trình nhiệt của phản ứng nhiệt phân CaCO₃ và phản ứng đốt cháy CH₄ như sau:
(1) CaCO₃(s) → CaO(s) + CO₂(s) ∆rH°₂₉₈ = +178,29kJ
(2) CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(l) ∆rH°₂₉₈ = -890,36kJ
Câu 6. Ion calcium (Ca²⁺) cần thiết cho máu người hoạt động bình thường, chỉ số Ca²⁺ trong máu ở ngưỡng bình thường (đối với người trưởng thành) khoảng 8.6 – 10.2 mg/dL (2.1 – 2.6 mmol/L). Nồng độ Ca²⁺ không bình thường là dấu hiệu của bệnh. Để xác định nồng độ Ca²⁺, người ta lấy mẫu máu, làm kết tủa ion Ca²⁺ dưới dạng calcium oxalate (CaC₂O₄) rồi cho calcium oxalate tác dụng với dung dịch KMnO₄ trong môi trường acid. Sơ đồ phản ứng như sau: KMnO₄ + CaC₂O₄ + H₂SO₄ → MnSO₄ + CaSO₄ + K₂SO₄ + CO₂ + H₂O
Giả sử calcium oxalate kết tủa từ 1,00 mL máu người tác dụng vừa hết với 2,05 mL dung dịch KMnO₄ 4,88.10⁻⁴M. Tính số mg Ca²⁺ trên 100 mL máu của người đó.
Mục đích tổ chức kỳ thi Tốt nghiệp THPT năm 2025 là gì?
Căn cứ vào các văn bản chỉ đạo và hướng dẫn của Bộ Giáo dục và Đào tạo, kỳ thi Tốt nghiệp THPT năm 2025 được tổ chức với những mục đích chính như sau:
– Đánh giá kết quả học tập của học sinh sau 12 năm học theo chương trình giáo dục phổ thông mới.
– Sử dụng kết quả thi để xét công nhận tốt nghiệp trung học phổ thông và làm căn cứ tuyển sinh cho các cơ sở giáo dục đại học, cao đẳng.
– Góp phần đánh giá chất lượng giáo dục ở các địa phương và trên phạm vi toàn quốc, từ đó điều chỉnh nội dung và phương pháp dạy học trong nhà trường cho phù hợp.
Thí sinh thi tốt nghiệp THPT năm 2025 có bắt buộc phải thi môn Hóa học không?
Theo quy định của Bộ Giáo dục và Đào tạo, thí sinh dự thi Tốt nghiệp THPT năm 2025 phải tham gia ba bài thi bắt buộc: Toán, Ngữ văn và Ngoại ngữ.
Ngoài ra, thí sinh lựa chọn một trong hai bài thi tổ hợp:
– Tổ hợp Khoa học Tự nhiên (KHTN): gồm các môn Vật lí, Hóa học và Sinh học.
– Tổ hợp Khoa học Xã hội (KHXH): gồm các môn Lịch sử, Địa lí và Giáo dục công dân (đối với học sinh học chương trình GDPT).
Trong bài thi tổ hợp KHTN, môn Hóa học là một trong ba môn thành phần. Thí sinh không bắt buộc phải thi môn Hóa học nếu không chọn tổ hợp KHTN. Tuy nhiên, với những thí sinh chọn bài thi tổ hợp KHTN để xét tốt nghiệp hoặc có mục tiêu xét tuyển vào các ngành đại học, cao đẳng yêu cầu môn Hóa học thì việc thi môn này là cần thiết.
Vì vậy, Đề thi minh họa tốt nghiệp THPT 2025 môn Hóa học – Đề số 1 là tài liệu hữu ích dành cho thí sinh chọn tổ hợp KHTN. Đề thi giúp các em ôn tập kiến thức, rèn luyện kỹ năng làm bài và làm quen với cấu trúc đề thi, từ đó chuẩn bị tốt nhất cho kỳ thi chính thức.




